Herpesvirus spojený se sarkomem kapózy - Kaposis sarcoma-associated herpesvirus - Wikipedia
| Lidský gammaherpesvirus 8 | |
|---|---|
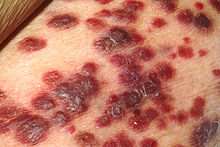 | |
| Kaposiho sarkom | |
| Klasifikace virů | |
| (bez hodnocení): | Virus |
| Oblast: | Duplodnaviria |
| Království: | Heunggongvirae |
| Kmen: | Peploviricota |
| Třída: | Herviviricetes |
| Objednat: | Herpesvirales |
| Rodina: | Herpesviridae |
| Rod: | Rhadinovirus |
| Druh: | Lidský gammaherpesvirus 8 |
Herpetický virus spojený s Kaposiho sarkomem (KSHV) je devátý známý člověk herpesvirus; jeho formální název podle Mezinárodní výbor pro taxonomii virů (ICTV) je Lidský gammaherpesvirus 8nebo HHV-8 ve zkratce.[1] Stejně jako ostatní herpesviry se jeho neformální názvy používají zaměnitelně s formálním názvem ICTV. Tento virus způsobuje Kaposiho sarkom, rakovina běžně se vyskytující v AIDS pacienti,[2] stejně jako primární výpotkový lymfom,[3] Multicentrická Castlemanova choroba spojená s HHV-8 a Syndrom zánětlivých cytokinů KSHV.[4] Je to jeden ze sedmi v současnosti známých lidských rakovinových virů, nebo onkoviry.[2] I po tolika letech objevování KSHV / HHV8 není znám žádný lék na KSHV související s tumorigenezí.
Dějiny
V roce 1872 Moritz Kaposi popsal nádor cév[5] (původně nazývaný „idiopatický mnohočetný pigmentovaný sarkom kůže“), který byl od té doby pojmenován stejnojmenně Kaposiho sarkom (KS). KS bylo zpočátku považováno za neobvyklý nádor židovské a středomořské populace, dokud se později nezjistilo, že je extrémně běžný u subsaharské populace Afriky. To vedlo k prvním návrhům v padesátých letech minulého století, že tento nádor může být způsoben virem. S nástupem AIDS Epidemie na počátku 80. let nastala náhlá obnova KS postihující primárně homosexuální a bisexuální pacienty s AIDS, přičemž tento nádor mělo až 50% hlášených pacientů s AIDS - mimořádná míra predispozice k rakovině.
Pečlivá analýza epidemiologických údajů Valerie Beral, Thomas Peterman a Harold Jaffe,[6] vedl tyto vyšetřovatele k návrhu, že KS je způsoben neznámým sexuálně přenosným virem, který zřídka způsobuje nádory, pokud se hostitel nestane imunosuprimovaný, jako v AIDS.[Citace je zapotřebí ]

Již v roce 1984 vědci uvedli, že v KS nádorech byly zkoumány struktury podobné herpesviru elektronová mikroskopie. Vědci hledali agenta způsobujícího KS a jako možnou příčinu bylo navrženo více než 20 agentů cytomegalovirus a HIV sám. Patogen byl nakonec identifikován v roce 1994 Yuan Chang a Patrick S.Moore, tým manželky a manžela v Columbia University, izolací fragmentů DNA z a herpesvirus nalezen v KS nádoru u pacienta s AIDS.[7][8][9] Chang a Moore použili reprezentativní rozdílová analýza, nebo RDA, najít KSHV porovnáním KS nádorové tkáně od pacienta s AIDS s jeho vlastní nepostiženou tkání. Myšlenkou tohoto experimentu bylo, že pokud virus způsobí KS, genomová DNA ve dvou vzorcích by měla být přesně identická, s výjimkou DNA patřící viru. Ve svém počátečním experimentu RDA izolovali dva malé fragmenty DNA, které představovaly méně než 1% skutečného virového genomu. Tyto fragmenty byly podobné (ale stále odlišné) od známých herpevirových sekvencí, což naznačuje přítomnost nového viru. Počínaje těmito fragmenty byl tento výzkumný tým schopen sekvenovat celý genom viru o necelé dva roky později.[Citace je zapotřebí ]
Objev tohoto herpesvirus vyvolal značnou polemiku a vědecké boje, dokud nebyly shromážděny dostatečné údaje, které ukazují, že KSHV byl skutečně původcem Kaposiho sarkomu.[10] O viru je nyní známo, že je to rozšířená infekce lidí žijících v subsaharské Africe; střední úrovně infekce se vyskytují ve středomořských populacích (včetně Libanonu, Saúdské Arábie, Itálie a Řecka) a nízké úrovně infekce se vyskytují ve většině populací v severní Evropě a Severní Americe. Homosexuální a bisexuální muži jsou náchylnější k infekci (stále neznámými způsoby sexuálního přenosu), zatímco virus se v rozvojových zemích přenáší nesexuálními způsoby.[Citace je zapotřebí ]
Virologie
KSHV je a herpesvirus, a je to velký dvouvláknový DNA virus s proteinovým potahem, který balí své nukleové kyseliny, nazývaný kapsid, který je poté obklopen amorfní proteinovou vrstvou zvanou tegument a nakonec uzavřeny v lipidovém obalu částečně odvozeném z buněčné membrány. KSHV má genom což je přibližně 165 000 bází nukleových kyselin. KSHV je a rhadinovirus, rod Herpes pozoruhodný, protože ukradl řadu genů z hostitelských buněk, včetně v případě genů KSHV, které kódují doplněk -vazebný protein, IL-6, BCL-2, cyklin -D, a Receptor spojený s G proteinem, interferonový regulační faktor a Flice inhibiční protein (FLIP ), stejně jako proteiny syntézy DNA včetně dihydrofolát reduktáza, thymidinkináza, thymidylát syntetáza DNA polymeráza a mnoho dalších. I když žádný jiný lidský nádorový virus nedisponuje stejnými geny, jiné nádorové viry se zaměřují na stejné buněčné dráhy, což ukazuje, že na základní úrovni se zdá, že všechny nádorové viry napadají stejné buněčné kontrolní dráhy, tzv. Nádorové supresorové dráhy.[Citace je zapotřebí ]
Po infekci virus vstupuje do lymfocytů prostřednictvím makropinozomy kde zůstává v latentním („tichém“) stavu. Pouze podmnožina genů, které jsou kódovány v oblasti asociované s latencí KSHV (KLAR), je exprimována během latence, včetně nukleárního antigenu spojeného s latencí (LANA), vFLIP, vCyclin a 12 mikroRNA. Latence je charakteristickým znakem všech dosud známých etiologií souvisejících s KSHV, včetně veškeré onkogeneze spojené s KSHV. Ukázalo se, že jak genové kódující proteiny, tak nekódující gen (microRNA) kódovaný v oblasti KLAR, jsou důležité pro tumorigenezi spojenou s KSHV. Ke studiu funkcí mikroRNA byl předními vědci v oboru zaveden podrobný protokol bacmidové mutageneze a kompletní sada buněčných linií nesoucích deleční mutanty mikroRNA, které jsou dostupné jako zdroj pro všechny mezinárodní výzkumné pracovníky působící v oblasti virů - související rakovina.[11] Navíc v jiné studii bylo prokázáno, že vFLIP a vCyclin interferují se signální cestou TGF-β nepřímo indukováním onkogenního hostitelského klastru mir17-92.[12] Tato pozorování představují nový mechanismus, který může být důležitý pro KSHV tumorigenezi a angiogenezi, charakteristický znak KS. Vývoj klíčových nástrojů, jako je kompletní sada 12 mikroRNA delečních mutantů, je důležitým vývojem při studiu funkcí genu KLAR v kontextu tumorigeneze spojené s KSHV [13] Rozhodující pro vstup KSHV [14] je EPH receptor A2,[15] Hod.,[16] TSG101[17] a pár Integriny, jehož totožnost ještě nebyla potvrzena.[18] Virus existuje jako kruhový kousek DNA nazývaný epizom a k replikaci používá strojní zařízení buněčné replikace. LANA je jediný virový protein, který je vyžadován pro replikaci virové DNA během latence. Virový epizom se po vstupu do jádra hostitelské buňky chromatinizuje.[19] LANA svazuje virovou DNA na buněčné chromozomy, inhibuje p53 a retinoblastomový protein a potlačuje virové geny potřebné pro plnou produkci a shromáždění viru („lytická replikace“). Proč pouze část podmnožiny virových genů exprimovaných během latence není zcela objasněna. Ukázalo se však, že expresi genů asociovanou s latencí lze částečně vysvětlit charakteristickým epigenetickým stavem, který epizom KSHV získává během latence. LANA hraje důležitou roli během latence. Je prokázáno, že reguluje jak hostitelské, tak virové přepisy a váže se na několik aktivních promotorů včetně hostitelských promotorů během latence.[20] Ve stejné studii bylo také prokázáno, že LANA se sdružuje s hostitelským strojním hSET1, který vytváří značky H3K4me3.[20] Přesný mechanismus, proč oblast KLAR zůstává aktivní během latence, však není znám. Rovněž se ukazuje, že různé signály, jako je zánět, mohou vyprovokovat virus k vstupu do lytické replikace. Když dojde k lytické replikaci, virový epizom se začne replikovat ve formě lineárních molekul DNA, které jsou zabaleny do virových částic, které jsou vyloučeny z buňky , k infikování nových buněk nebo k přenosu na nového hostitele. Když virus vstoupí do lytické replikace, mohou být z jedné buňky vyrobeny tisíce virových částic, což obvykle vede ke smrti infikované buňky.[Citace je zapotřebí ]
Virový genom sestává z ~ 145 kbasové dlouhé jedinečné oblasti kódující všechny exprimované virové geny, která je ohraničena ~ 20–30 kbázami terminálních repetičních sekvencí.[21] Každá terminální opakovací jednotka má délku 801 bp, má 85% obsah G + C a je orientována opakujícím se způsobem hlava-ocas. Během latence závisí genom viru na replikačním aparátu hostitele a replikuje se jako uzavřený kruhový epizom („plazmid“) s použitím sekvencí v terminálních repeticích jako počátek replikace. Když se virus reaktivuje na lytickou replikaci, předpokládá se, že genom viru je replikován jako spojitá lineární molekula mimo epizom (tzv. Model klouzavého kruhu). Jakmile se každý jednotkový genom replikuje, je rozřezán v oblasti terminální repetice a poté zabalen do virové částice (virion). Virus se poté obalí lipidovou membránou, když prochází jádrem a cytoplazmou a opouští buňku. Zatímco tedy genom KSHV je kruhový v jádru latentně infikovaných buněk, je zabalen do infekčních virů jako lineární molekula. Jakmile virus nově infikuje buňku, dojde k vylučování lipidové membrány a virion putuje do jádra. Virový genom se uvolňuje tam, kde se recirkuluje špatně pochopeným procesem, který, jak se zdá, zahrnuje homologní rekombinace.[Citace je zapotřebí ]
Primární virový protein odpovědný za přechod mezi latentní a lytickou replikací je známý jako aktivátor aktivace replikace ORF50 (RTA). Když podmínky buněčné signalizace aktivují generování RTA, aktivuje to syntézu stereotypní kaskády sekundárních a terciárních virových proteinů, které nakonec vytvářejí složky virové kapsidy a také enzymy syntézy DNA potřebné k replikaci genomu viru.[22]
Patofyziologie
Mechanismy, kterými se virus stahuje, nejsou dobře známy. Zdraví jedinci mohou být nakaženi virem a nevykazují žádné známky nebo příznaky kvůli schopnosti imunitního systému udržovat infekci pod kontrolou. Infekce se týká zejména: imunokompromitovaný. U pacientů s rakovinou, kteří dostávají chemoterapii, u pacientů s AIDS a u pacientů po transplantaci orgánů, existuje vysoké riziko, že budou vykazovat známky infekce.[Citace je zapotřebí ].
Nedávný pokrok v sekvenčních technologiích odhalil, že virus je během latence chromatinizován. Rovněž se ukázalo, že virus kódovaný mikroRNA manipuluje a interaguje nejen s hostitelskou mRNA, ale také dereguluje hostitelskou dlouhou nekódující RNA (lncRNA).[23] V poslední době jsou cirkulární RNA (circRNA) nedávno objeveny jak v EBV, tak v KSHV [24][25][26]
Infekce tímto virem je považována za celoživotní, ale zdravý imunitní systém udrží virus pod kontrolou. Mnoho lidí infikovaných KSHV nikdy nevykazuje žádné příznaky. Kaposiho sarkom nastává, když u někoho, kdo byl infikován KSHV, došlo ke snížení imunity v důsledku AIDS, lékařského ošetření nebo velmi zřídka stárnutí.
KSHV je známý původce čtyř onemocnění:[4][27]
- Kaposiho sarkom - angioproliferativní nádor, který může zahrnovat kůži (nejčastěji), lymfatické uzliny nebo vnitřnosti,
- Multicentrická Castlemanova choroba spojená s HHV-8 - a lymfoproliferativní porucha,
- Primární výpotkový lymfom - agresivní lymfom spojený s KSHV zahrnující B-buňky, které jsou nezralé plazmatické buňky nazývané plazmablasty a považovány za jeden typ lymfoidní novotvary s plasmablastickou diferenciací,
- Syndrom zánětlivých cytokinů KSHV - syndrom s příznaky podobnými MCD, ale bez související patologie.
Epidemiologie
V 70. letech je celosvětová prevalence HHV-8 2 až 10%.[28] Séroprevalence HHV-8 se výrazně geograficky liší a míra infekce v zemích severní Evropy, jihovýchodní Asie a Karibiku se pohybuje mezi 2–4%,[29] ve středomořských zemích přibližně 10% a v zemích subsaharské Afriky přibližně 40%.[30] V Jižní Americe je míra infekce obecně nízká, ale vysoká Amerindians.[31] I v rámci jednotlivých zemí lze pozorovat významné rozdíly v různých regionech, přičemž míra infekce v roce činila přibližně 19,2% Sin-ťiang ve srovnání s přibližně 9,5% v roce 2006 Hubei, Čína.[32] Ačkoli se trvale ukazuje, že séroprevalence se s věkem lineárně zvyšuje,[32][33][34][35] země s vysokou mírou infekce mohou zaznamenat vyšší séroprevalenci u mladších věkových skupin.[36] Úroveň vzdělání prokázala inverzní korelaci s mírou infekce.[33][34] Jedinci infikovaní HIV-1 nebo genitálními bradavicemi jsou obecně pravděpodobnější koinfikováni HHV-8.[30][32][37]
V zemích s nízkou séroprevalencí je HHV-8 primárně omezen na pacienty s AIDS a KS.[38] V zemích s vysokou séroprevalencí je infekce v dětství častá,[39] což naznačuje pravděpodobnost přenos z matky na dítě slinami.[40][41] V Zambijský průzkumu, všechny děti s KS měly matky, které byly pozitivní na HHV-8, zatímco ne všechny děti, jejichž matky měly KS, byly pozitivní na HHV-8.[42] V dalším zambijském průzkumu bylo 13,8% dětí séropozitivních na HHV-8 ve věku 4 let.[43] Ukázalo se, že séroprevalence se významně neliší z důvodu pohlaví nebo rodinného stavu.[35]
Vývoj
The poslední společný předek Odhaduje se, že tohoto viru ve Středomoří, Íránu a čínském Sin-ťiangu se vyvinulo před 29 872 lety (95% nejvyšší hustota pravděpodobnosti 26 851–32 760 let).[44] poslední společný předek virů izolovaných v Sin-ťiangu byl před 2037 lety (95% nejvyšší hustota pravděpodobnosti před 1843–2229 lety). Vzhledem k historickým vazbám mezi Středozemním mořem a Sin-ťiangem během římský období se zdá pravděpodobné, že tento virus byl do Sin-ťiangu zaveden podél Hedvábná stezka. Míra mutace byla odhadnuta na 3,44 × 10−6 substituce na místo za rok (95% nejvyšší hustota pravděpodobnosti 2,26 × -6 až 4,71 × 10−6). Globální distribuce různých genotypů KSHV a potenciální přenosová cesta však vyžadují další studie.[Citace je zapotřebí ]
Typizace izolátů je založena na variabilním membránovém proteinu K1. Je rozpoznáno šest typů (A-F).[45]
Prevence
Vzhledem k tomu, že osoby infikované KSHV asymptomaticky způsobí virus, měl by být opatrný sexuální partneři mít nechráněný sex a aktivity, při nichž by se během sexuální aktivity mohly sdílet sliny. Obezřetná rada je používat kondomy v případě potřeby a vyhnout se hluboké líbání s partnery s infekcemi KSHV a HIV nebo jejichž stav není znám. Krevní testy k detekci protilátek proti viru existují.[Citace je zapotřebí ]
Léčba
Kaposiho sarkom je obvykle lokalizovaný nádor, který lze léčit buď chirurgicky, nebo lokálním ozařováním. Chemoterapie léky, jako jsou liposomální antracykliny nebo paclitaxel mohou být použity, zejména pro invazivní onemocnění. Antivirotika, jako jsou ganciklovir, které se zaměřují na replikaci herpesvirů, jako je KSHV, byly použity k úspěšné prevenci rozvoje Kaposiho sarkomu,[46] ačkoli jakmile se nádor vyvine, jsou tyto léky málo nebo vůbec nepoužitelné. U pacientů s AIDS-KS je nejúčinnější terapie vysoce aktivní antiretrovirová léčba ke snížení infekce HIV.[47] Pacienti s AIDS dostávající adekvátní léčbu proti HIV mohou mít až 90% snížení výskytu Kaposiho sarkomu.
Ačkoli KSHV ovlivňuje imunitní systém hostitele, existuje velká šance pro klinický zásah, aby se tato změna obnovila. Jednou výzvou je inhibice nadměrné exprese cílové buňky potlačující imunitu. Při dlouhodobé stimulaci zánětu není cílová buňka schopna reagovat, což vede k vyčerpání fenotypu. Aktivační imunoterapie může oživit a zlepšit funkci imunitních buněk. Ve srovnání s jinými imunoterapiemi jsou terapie zaměřeny na anti-programovaný protein buněčné smrti 1 (PD-1 ) / naprogramovaný ligand smrti 1 (PD-L1 ) měl velký úspěch. Kvůli infekci KSHV zvyšují monocyty expresi PD-1, což je inhibiční molekula, a způsobují imunitní únik u mnoha typů nádorů. V NK buňkách pacientů s KS-HIV je vysoká exprese PD-1 a způsobuje vyčerpaný fenotyp. Protilátka anti-PD-1, (nivolumab nebo pembrolizumab ), prokázal významný protinádorový účinek. Nivolumab v současné době probíhá v klinické studii fáze I a Pembrolizumab prokázal svou funkci při léčbě pacientů s HIV a KS ve fázi I a je ve fázi II léčby. Lék na analog thalidomidu - Pomalidomid byl také udělen FDA v roce 2011. Bylo prokázáno, že pomalidomid obnovuje expresi MHC-1, které pomáhají buňkám zobrazovat intracelulární proteiny cytotoxickým T buňkám a také mohou potlačovat expresi PD-L1 a zvyšovat zabíjení CD8 + T buněk.[48]
Geny KSHV
KSHV kóduje ~ 90 genů a více nekódujících RNA, jako jsou mikroRNA.[49] Geny "ORF" jsou pojmenovány na základě polohy genomu homologních genů v prvním popsaném rhadinoviru, herpesvirus saimiri. Geny „K“ jsou pro KSHV jedinečné, některé geny KSHV mají dobře charakterizované funkce, zatímco jiné zůstávají necharakterizované.
ORF2 - dihydrofolát reduktáza
ORF8 - gB - obálka glykoprotein podílí se na virovém vstupu
ORF9 - Pol8 - DNA polymeráza potřebné pro replikaci virové DNA
ORF10 - reguluje export RNA a odpovědi na IFN typu I
ORF16 - vBcl2
ORF18, ORF24, ORF30, ORF31, ORF34, ORF66 - virové transkripční faktory potřebné pro expresi pozdních genů
ORF21 - vTK - thymidinkináza
ORF22 - gH - obálka glykoprotein podílí se na virovém vstupu
ORF23 - necharakterizovaný
ORF25, ORF26 a ORF65 - kapsid bílkoviny
ORF33 - podílí se na tvorbě virových částic
ORF34 - nejasná funkce
ORF35 - nejasná funkce, mutant neexprimuje rané virové geny
ORF36 - vPK - virová proteinová kináza s více rolemi v replikačním cyklu
ORF37 - SOX - protein s dvojí funkcí - DNase aktivita vyžadovaná pro balení genomu a RNáza aktivita reguluje expresi hostitelského genu
ORF38 - podílí se na tvorbě virových částic
ORF39 - gM - obálka glykoprotein
ORF40 a ORF41 - helikáza a primase - Replikace DNA
ORF42 - necharakterizovaný
ORF45 - tegument protein, váže a brání defosforylaci p90 ribozomálních S6 kináz (RSK) a ERK pro modulaci ERK / RSK MAPK signální dráha
ORF47 - gL - obalový glykoprotein podílející se na vstupu viru
ORF49 - může být vyžadován pro expresi virového genu
ORF50 - RTA, aktivátor replikace a transkripce - hlavní transkripční faktor, který řídí lytickou reaktivaci KSHV
ORF52 - KicGAS - tegument protein potřebný pro tvorbu virionů a inhibici cGAS Snímání DNA
ORF53 - gN - obalový glykoprotein
ORF55 - necharakterizovaný
ORF57 - MTA - reguluje stabilitu RNA, export a translaci virových genů
ORF59 - PF – 8 - faktor procesivity polymerázy, doplňková podjednotka virové DNA polymerázy
ORF67 a ORF69 - jaderný výstup
ORF70 - thymidylát syntáza
ORF72 - vCyklin
ORF73 - LANA, jaderný antigen spojený s latencí - během latence svazuje genom na chromozom, také reguluje expresi hostitelského genu. Cytoplazmatická forma LANA může inhibovat aktivaci imunitních odpovědí.
ORF74 - vGPCR
ORF75 - FGARAT
PÁNEV, polyadenylovaný jaderný RNA - nekódující lineární a kruhové RNA
miRNA (mirKs) - virové mikroRNA exprimované během latence k regulaci proliferace a buněčné smrti
K1 - podílí se na onkogenezi
K2 - Interleukin 6 homolog, Q2HRC7
K3 a K5 - ubikvitin E3 ligázy - regulovat prezentaci antigenu
K4 - vCCL2 - chemokin
K4.1 - vCCL3 - chemokin
K8 - transkripční represor - moduluje chromatin
K8.1 - obálka glykoprotein
K9 - vIRF 1, virální interferonový regulační faktor 1
K10 - vIRF 4. Kruhová RNA (circRNA ) je také generován z toho místo.
K10.5 - vIRF3 / LANA2 - vyjádřeno během latence v B buňky
K11 - vIRF 2
K12 - kaposin
K13 - vFLIP
Viz také
- Oncovirus (virus rakoviny)
- 22. mezinárodní seminář o herpesviru s karposi sarkomem (KSHV) a souvisejících látkách, 30. června - 3. července 2019, New York City, USA
Reference
- ^ „Seznam hlavních druhů ICTV 2018b.v2“. Mezinárodní výbor pro taxonomii virů. Citováno 13. června 2019.
- ^ A b Boshoff, C .; Weiss, R. (2002). „Malignity související s AIDS“. Nature Reviews Cancer. 2 (5): 373–382. doi:10.1038 / nrc797. PMID 12044013. S2CID 13513517.
- ^ Cesarman, E .; Chang, Y .; Moore, P. S .; Said, J. W .; Knowles, D. M. (1995). „Kaposiho sarkom - související sekvence DNA podobné herpesviru v lymfomech založených na tělních dutinách souvisejících s AIDS“. New England Journal of Medicine. 332 (18): 1186–1191. doi:10.1056 / NEJM199505043321802. PMID 7700311.
- ^ A b Goncalves, Priscila H .; Ziegelbauer, Joseph; Uldrick, Thomas S .; Yarchoan, Robert (2017). „Rakovina spojená s herpesvirusem Kaposiho sarkomu a související nemoci“. Curr Opin HIV AIDS. 12 (1): 47–56. doi:10.1097 / COH.0000000000000330. PMC 6311702. PMID 27662501.
- ^ Kaposi, M (1872). „Idiopathisches multiples Pigmentsarkom der Haut“. Archiv für Dermatologie und Syfilis. 4 (2): 265–273. doi:10.1007 / BF01830024. S2CID 31438763.
Přeloženo v Kaposi, M (2008). "Idiopatický mnohočetný pigmentovaný sarkom kůže". CA: Časopis o rakovině pro klinické lékaře. 32 (6): 342–347. doi:10.3322 / canjclin.32.6.342. S2CID 72037330. - ^ Beral V, Peterman TA, Berkelman RL, Jaffe HW (1990). „Kaposiho sarkom u osob s AIDS: pohlavně přenosná infekce?“. Lanceta (Vložený rukopis). 335 (8682): 123–8. doi:10.1016 / 0140-6736 (90) 90001-L. PMID 1967430. S2CID 35639169.
- ^ Chang, Y .; Cesarman, E .; Pessin, M. S .; Lee, F .; Culpepper, J .; Knowles, D. M .; Moore, P. S. (1994). "Identifikace sekvencí DNA podobných herpesviru v Kaposiho sarkomu spojeném s AIDS". Věda. 266 (5192): 1865–1869. Bibcode:1994Sci ... 266.1865C. doi:10.1126 / science.7997879. PMID 7997879.
- ^ Moore PS, Chang Y (květen 1995). „Detekce sekvencí DNA podobných herpesviru v Kaposiho sarkomu u pacientů s HIV infekcí i bez ní“. The New England Journal of Medicine. 332 (18): 1181–5. doi:10.1056 / NEJM199505043321801. PMID 7700310. S2CID 13465834.
- ^ Antman, K .; Chang, Y. (2000). „Kaposiho sarkom“. New England Journal of Medicine. 342 (14): 1027–1038. doi:10.1056 / NEJM200004063421407. PMID 10749966.
- ^ Boshoff C, Weiss RA (květen 2000). „Řešení sporů ohledně Kaposiho sarkomu“. Journal of the National Cancer Institute. 92 (9): 677–679. doi:10.1093 / jnci / 92.9.677. PMID 10793096.
- ^ Jain, Vaibhav; Plaisance-Bonstaff, Karlie; Sangani, Rajnikumar; Lanier, Curtis; Dolce, Alexander; Hu, Jianhong; Brulois, Kevin; Haecker, Irina; Turner, Peter; Renne, Rolf; Krueger, Brian (19. února 2016). „Sada nástrojů pro výzkum miRNA u herpesviru: Konstrukce kompletní sady delečních mutantů KSHV miRNA“. Viry. 8 (2): 54. doi:10,3390 / v8020054. ISSN 1999-4915. PMC 4776209. PMID 26907327.
- ^ Choi, HS; Jain, V; Krueger, B; Marshall, V; Kim, CH; Shisler, JL; Whitby, D; Renne, R (2015). „Kaposiho sarkom asociovaný herpesvirus (KSHV) indukuje onkogenní miR-17-92 klastr a down-reguluje signalizaci TGF-β“. PLOS patogeny. 11 (11): e1005255. doi:10.1371 / journal.ppat.1005255. PMC 4636184. PMID 26545119.
- ^ Jain, V; Plaisance-Bonstaff, K; Sangani, R; Lanier, C; Dolce, A; Hu, J; Brulois, K; Haecker, I; Turner, P; Renne, R; Krueger, B (19. února 2016). „Sada nástrojů pro výzkum miRNA u herpesviru: Konstrukce kompletní sady delečních mutantů KSHV miRNA“. Viry. 8 (2): 54. doi:10,3390 / v8020054. PMC 4776209. PMID 26907327.
- ^ Kumar, Binod; Chandran, Bala (14. listopadu 2016). „Vstup KSHV a obchodování s cílovými buňkami - únos buněčných signálních drah, aktinu a membránové dynamiky“. Viry. 8 (11): 305. doi:10,3390 / v8110305. ISSN 1999-4915. PMC 5127019. PMID 27854239.
- ^ Neipel F, Fleckenstein B, Hahn A a kol. (Červen 2012). „Efrinový receptor tyrosinkináza A2 je buněčný receptor pro herpesvirus spojený s Kaposiho sarkomem“. Přírodní medicína. 18 (6): 961–968. doi:10,1038 / nm.2805. PMC 3645317. PMID 22635007.
- ^ Veettil, Mohanan Valiya; Kumar, Binod; Ansari, Mairaj Ahmed; Dutta, Dipanjan; Iqbal, Jawed; Gjyshi, Olsi; Bottero, Virginie; Chandran, Bala (duben 2016). „Složka ESCRT-0 Hrs podporuje makropinocytózu herpetického viru spojeného s Kaposiho sarkomem v lidských dermálních mikrovaskulárních endoteliálních buňkách“. Journal of Virology. 90 (8): 3860–3872. doi:10.1128 / JVI.02704-15. ISSN 1098-5514. PMC 4810545. PMID 26819309.
- ^ Kumar, Binod; Dutta, Dipanjan; Iqbal, Jawed; Ansari, Mairaj Ahmed; Roy, Arunava; Chikoti, Leela; Pisano, Gina; Veettil, Mohanan Valiya; Chandran, Bala (říjen 2016). „Protein ESCRT-I Tsg101 hraje roli v post-makropinocytovém obchodování a infekci endoteliálních buněk herpesvirusem spojeným s Kaposiho sarkomem“. PLOS patogeny. 12 (10): e1005960. doi:10.1371 / journal.ppat.1005960. ISSN 1553-7374. PMC 5072609. PMID 27764233.
- ^ Campadelli-Fiume G, Collins-McMillen D a kol. (Červenec 2016). "Integriny jako receptory herpersviru a mediátory hostitelského signalosomu". Roční přehled virologie. 3 (1): 215–236. doi:10.1146 / annurev-virology-110615-035618. PMID 27501260.
- ^ Purushothaman a kol. (Únor 2016). "KSHV replikace a údržba genomu". Hranice v mikrobiologii. 7: 54. doi:10.3389 / fmicb.2016.00054. PMC 4740845. PMID 26870016.
- ^ Russo JJ, Bohenzky RA, Chien MC a kol. (Prosinec 1996). "Nukleotidová sekvence herpesviru spojeného s Kaposiho sarkomem (HHV8)". Sborník Národní akademie věd Spojených států amerických. 93 (25): 14862–7. Bibcode:1996PNAS ... 9314862R. doi:10.1073 / pnas.93.25.14862. PMC 26227. PMID 8962146.
- ^ Bu W, Palmeri D, Krishnan R a kol. (Listopad 2008). „Identifikace přímých transkripčních cílů lytického přepojovacího proteinu kapsiho sarkomu asociovaného s herpes viry Rta podmíněnou nukleární lokalizací“. Journal of Virology. 82 (21): 10709–23. doi:10.1128 / JVI.01012-08. PMC 2573185. PMID 18715905.
- ^ Sethuraman, S; Gay, LA; Jain, V; Haecker, I; Renne, R (červenec 2017). „na microRNA závislá a nezávislá deregulace dlouhých nekódujících RNA onkogenním herpesvirem“. PLOS patogeny. 13 (7): e1006508. doi:10.1371 / journal.ppat.1006508. PMC 5531683. PMID 28715488.
- ^ Toptan, T; Abere, B; Nalesnik, MA; Swerdlow, SH; Ranganathan, S; Lee, N; Shair, KH; Moore, PS; Chang, Y (11. září 2018). „Kruhové DNA nádorové viry vytvářejí kruhové RNA“. Sborník Národní akademie věd Spojených států amerických. 115 (37): E8737 – E8745. doi:10.1073 / pnas.1811728115. PMC 6140489. PMID 30150410.
- ^ Tagawa, T; Gao, S; Koparde, VN; Gonzalez, M; Spouge, JL; Serquiña, AP; Lurain, K; Ramaswami, R; Uldrick, TS; Yarchoan, R; Ziegelbauer, JM (11. prosince 2018). „Objev Kaposiho sarkomu, kódovaného herpesvirem, cirkulárních RNA a lidské antivirové cirkulární RNA“. Sborník Národní akademie věd Spojených států amerických. 115 (50): 12805–12810. doi:10.1073 / pnas.1816183115. PMC 6294913. PMID 30455306.
- ^ Ungerleider, NA; Jain, V; Wang, Y; Maness, NJ; Blair, RV; Alvarez, X; Midkiff, C; Kolson, D; Bai, S; Roberts, C; Moss, WN; Wang, X; Serfecz, J; Seddon, M; Lehman, T; Ma, T; Dong, Y; Renne, R; Tibbetts, SA; Flemington, EK (15. března 2019). „Srovnávací analýza kruhových RNA repertoárů gammaherpesviru: konzervované a jedinečné virové kruhové RNA“. Journal of Virology. 93 (6). doi:10.1128 / JVI.01952-18. PMC 6401440. PMID 30567979.
- ^ Chen BJ, Chuang SS (březen 2020). „Lymfoidní novotvary s plazmablastickou diferenciací: komplexní přehled a diagnostické přístupy“. Pokroky v anatomické patologii. 27 (2): 61–74. doi:10.1097 / PAP.0000000000000253. PMID 31725418.
- ^ Gallo, Robert C. (12.12.1998). „Záhady Kaposiho sarkomu“. Věda. 282 (5395): 1837–1839. doi:10.1126 / science.282.5395.1837. ISSN 0036-8075. PMID 9874635.
- ^ Zhang, Tiejun; Wang, Linding (2016). „Epidemiologie herpetického viru spojeného s Kaposiho sarkomem v Asii: výzvy a příležitosti“. Journal of Medical Virology. 89 (4): 563–570. doi:10.1002 / jmv.24662. ISSN 0146-6615. PMID 27531516.
- ^ A b Chatlynne, L. G .; Ablashi, D. V. (1999). "Seroepidemiologie Kaposiho sarkomu asociovaného herpesviru (KSHV)". Semináře z biologie rakoviny. 9 (3): 175–85. doi:10.1006 / scbi.1998.0089. PMID 10343069.
- ^ Mohanna, S; Maco, V; Bravo, F; Gotuzzo, E (2005). „Epidemiologie a klinické charakteristiky klasického Kaposiho sarkomu, séroprevalence a variant lidského herpesviru 8 v Jižní Americe: kritický přehled staré nemoci“. International Journal of Infection Diseases. 9 (5): 239–50. doi:10.1016 / j.ijid.2005.02.004. PMID 16095940.
- ^ A b C Fu, B; Sun, F; Li, B; Yang, L; Zeng, Y; Sun, X; Xu, F; Rayner, S; Guadalupe, M; Gao, S. J .; Wang, L (2009). „Séroprevalence herpesviru spojeného s Kaposiho sarkomem a rizikové faktory v čínském Sin-ťiangu“. Journal of Medical Virology. 81 (8): 1422–31. doi:10.1002 / jmv.21550. PMC 2755560. PMID 19551832.
- ^ A b Pelser, C; Vitale, F; Whitby, D; Graubard, B. I .; Messina, A; Gafà, L; Brown, E. E.; Anderson, L. A .; Romano, N; Lauria, C; Goedert, J. J. (2009). „Socioekonomické a další korelace séroprevalence herpesviru spojené s kaposiho sarkomem u starších dospělých na Sicílii“. Journal of Medical Virology. 81 (11): 1938–44. doi:10,1002 / jmv.21589. PMC 2784645. PMID 19777527.
- ^ A b Wang, H; Liu, J; Dilimulati; Li, L; Ren, Z; Wen, H; Wang, X (2011). "Séroprevalence a rizikové faktory kaposiho sarkomu spojené s herpesvirovou infekcí u obecné populace Uygurů z jižní a severní oblasti Sin-ťiangu v Číně". Virology Journal. 8: 539. doi:10.1186 / 1743-422X-8-539. PMC 3266657. PMID 22168313.
- ^ A b Olsen, S. J .; Chang, Y; Moore, P. S .; Biggar, R. J .; Melbye, M (1998). „Zvýšení séroprevalence herpesviru spojené s Kaposiho sarkomem s věkem v endemické oblasti vysoce Kaposiho sarkomu, Zambie v roce 1985“. AIDS. 12 (14): 1921–5. doi:10.1097/00002030-199814000-00024. PMID 9792393. S2CID 1734745.
- ^ Wawer, M. J .; Eng, S. M .; Serwadda, D; Sewankambo, N. K.; Kiwanuka, N; Li, C; Gray, R. H. (2001). „Prevalence herpesviru spojeného s Kaposiho sarkomem ve srovnání s vybranými pohlavně přenosnými chorobami u dospívajících a mladých dospělých ve venkovské oblasti Rakai v Ugandě“. Pohlavně přenosné nemoci. 28 (2): 77–81. doi:10.1097/00007435-200102000-00003. PMID 11234789. S2CID 7592869.
- ^ Klaskala, W; Brayfield, B. P .; Kankasa, C; Bhat, G; West, J. T .; Mitchell, C. D .; Wood, C (2005). „Epidemiologické charakteristiky infekce lidským herpesvirem-8 u velké populace prenatálních žen v Zambii“. Journal of Medical Virology. 75 (1): 93–100. doi:10.1002 / jmv.20242. PMID 15543582.
- ^ Kourí, V; Eng, S. M .; Rodríguez, M. E.; Resik, S; Orraca, O; Moore, P. S .; Chang, Y (2004). „Séroprevalence herpesviru spojeného s Kaposiho sarkomem v různých populacích na Kubě“. Revista Panamericana de Salud Pública. 15 (5): 320–5. doi:10,1590 / s1020-49892004000500006. PMID 15231079.
- ^ Schulz, T. F. (2000). „Herpesvirus spojený s Kaposiho sarkomem (lidský herpesvirus 8): Epidemiologie a patogeneze“. The Journal of Antimicrobial Chemotherapy. 45 Suppl T3 (90004): 15–27. doi:10.1093 / jac / 45.suppl_4.15. PMID 10855768.
- ^ Mesri, Enrique A .; Cesarman, Ethel; Boshoff, Chris (říjen 2010). „Herpetický virus Kaposiho sarkomu / lidský herpesvirus-8 (KSHV / HHV8) a onkogeneze Kaposiho sarkomu“. Recenze přírody. Rakovina. 10 (10): 707. doi:10.1038 / nrc2888. PMID 20865011.
- ^ Brayfield, B. P .; Phiri, S; Kankasa, C; Muyanga, J; Mantina, H; Kwenda, G; West, J. T .; Bhat, G; Marx, D. B .; Klaskala, W; Mitchell, C. D .; Wood, C (2003). „Postnatální infekce lidským herpesvirem 8 a virem lidské imunodeficience typu 1 u matek a kojenců ze Zambie“. The Journal of Infectious Diseases. 187 (4): 559–68. doi:10.1086/367985. PMID 12599072.
- ^ On, J; Bhat, G; Kankasa, C; Chintu, C; Mitchell, C; Duan, W; Wood, C (1998). „Séroprevalence lidského herpesviru 8 u zambijských žen v plodném věku bez Kaposiho sarkomu (KS) a párů matka-dítě s KS“. The Journal of Infectious Diseases. 178 (6): 1787–90. doi:10.1086/314512. PMID 9815235.
- ^ Minhas, V; Crabtree, K. L .; Chao, A; m'Soka, T. J .; Kankasa, C; Bulterys, M; Mitchell, C. D .; Wood, C (2008). „Infekce v raném dětství lidským herpesvirem 8 v Zambii a role koinfekce virem lidské imunodeficience typu 1 ve vysoce endemické oblasti“. American Journal of Epidemiology. 168 (3): 311–20. doi:10.1093 / aje / kwn125. PMC 2727264. PMID 18515794.
- ^ Liu Z, Fang Q, Zuo J, Minhas V, Wood C, He N, Zhang T (2017) Byl Kaposiho herpesvirus spojený se sarkomem zaveden do Číny starou Silk Road? Evoluční perspektiva. Arch Virol
- ^ Jary A, Leducq V, Desire N, Petit H, Palich R, Joly V, Canestri A, Gothland A, Lambert-Niclot S, Surgers L, Amiel C, Descamps D, Spano JP, Katlama C, Calvez V, Marcelin AG ( 2020) Nová varianta herpesviru spojená s sarkomem Kaposiho u mužů, kteří mají sex s muži spojenými s těžkými patologiemi. J Infect Dis
- ^ Martin DF, Kuppermann BD, Wolitz RA, Palestine AG, Li H, Robinson CA (duben 1999). „Perorální ganciklovir pro pacienty s cytomegalovirovou retinitidou léčené implantátem gancikloviru. Studijní skupina Roche Ganciclovir“. The New England Journal of Medicine. 340 (14): 1063–70. doi:10.1056 / NEJM199904083401402. PMID 10194235.
- ^ Yarchoan, R .; Tosato, G .; Malý, R. F. (2005). „Přehled terapie: Malignity související s AIDS - vliv antivirové terapie na patogenezi a léčbu“. Onkologie klinické klinické praxe v přírodě. 2 (8): 406–415, kvíz 415. doi:10.1038 / ncponc0253. PMID 16130937. S2CID 23476060.
- ^ Broussard, Grant; Damania, Blossom (07.02.2020). "KSHV: Imunitní modulace a imunoterapie". Hranice v imunologii. 10. doi:10,3389 / fimmu.2019.03084. ISSN 1664-3224. PMC 7025529. PMID 32117196.
- ^ Samols MA, Hu J, Skalsky RL, Renne R (červenec 2005). „Klonování a identifikace shluku mikroRNA v oblasti spojené s latencí herpesviru spojeného s Kaposiho sarkomem“. Journal of Virology. 79 (14): 9301–5. doi:10.1128 / JVI.79.14.9301-9305.2005. PMC 1168752. PMID 15994824.
Další čtení
- Edelman DC (2005). „Lidský herpesvirus 8 - nový lidský patogen“. Virology Journal. 2: 78. doi:10.1186 / 1743-422X-2-78. PMC 1243244. PMID 16138925.
externí odkazy
- Lidský herpesvirus-8: Související zdroje HIV InSite
- Výroční seminář KSHV 22. mezinárodní seminář o herpetickém viru karposi sarkomu (KSHV) a souvisejících agentech, 30. června - 3. července 2019, New York City, USA
