Genom - Genome
| Část série na |
| Genetika |
|---|
 |
| Klíčové komponenty |
| Historie a témata |
| Výzkum |
| Personalizovaná medicína |
| Personalizovaná medicína |

V polích molekulární biologie a genetika, a genom je veškerý genetický materiál organismu. Skládá se z DNA (nebo RNA v RNA viry ). Genom zahrnuje oba geny (dále jen kódující oblasti ) a nekódující DNA,[1] stejně jako mitochondriální DNA[2] a chloroplastová DNA. Studie genomu se nazývá genomika.
Původ termínu
Termín genom byla vytvořena v roce 1920 uživatelem Hans Winkler,[3] profesor botanika na Univerzita v Hamburku, Německo. Oxfordský slovník naznačuje, že název je směsicí slov gen a chromozóm.[4] Nicméně viz omics pro důkladnější diskusi. Několik souvisejících -ome slova již existovala, jako např biome a oddenek, tvořící slovník, do kterého genom zapadá systematicky.[5]
Sekvenování a mapování
Sekvence genomu je úplný seznam nukleotidy (A, C, G a T pro genomy DNA), které tvoří vše chromozomy jedince nebo druhu. V rámci druhu je drtivá většina nukleotidů mezi jednotlivci identická, ale pro pochopení genetické rozmanitosti je nutné sekvenování více jedinců.

V roce 1976 Walter Fiers na Univerzita v Gentu (Belgie) jako první zavedla úplnou nukleotidovou sekvenci virového RNA-genomu (Bakteriofág MS2 ). Další rok, Fred Sanger dokončil první sekvenci DNA-genomu: Fág Φ-X174, z 5386 párů bází.[6] První úplné genomové sekvence ze všech tří domén života byly uvolněny během krátké doby v polovině 90. let: Prvním bakteriálním genomem, který měl být sekvenován, byl genom Haemophilus influenzae, vyplněný týmem v Institut pro genomický výzkum v roce 1995. O několik měsíců později byl dokončen první eukaryotický genom se sekvencemi 16 chromozomů začínajících kvasinek Saccharomyces cerevisiae publikováno jako výsledek úsilí vedeného Evropou zahájeného v polovině 80. let. První sekvence genomu pro archaeon, Methanococcus jannaschii, byla dokončena v roce 1996, opět Ústavem pro genomický výzkum.
Vývoj nových technologií dramaticky zlevnil a usnadnil sekvenování genomu a počet kompletních sekvencí genomu rychle roste. The Americké národní instituty zdraví udržuje jednu z několika komplexních databází genomických informací.[7] Mezi tisíce dokončených projektů sekvenování genomu patří projekty pro rýže, a myš, Rostlina Arabidopsis thaliana, puffer ryby a bakterie E-coli. V prosinci 2013 vědci nejprve sekvenovali celý genom a neandrtálec, vyhynulý druh lidé. Genom byl extrahován z špička kosti 130 000 let starého neandertálce nalezeného v a Sibiřská jeskyně.[8][9]
Nové technologie sekvenování, jako např masivní paralelní řazení také otevřely vyhlídky na sekvenování osobního genomu jako diagnostický nástroj, jak je průkopníkem Manteia Predictive Medicine. Hlavním krokem k dosažení tohoto cíle bylo dokončení plný genom z James D. Watson, jeden ze spoluobjevitelů struktury DNA.[10]
Zatímco sekvence genomu uvádí pořadí každé DNA báze v genomu, mapa genomu identifikuje orientační body. Mapa genomu je méně podrobná než sekvence genomu a pomáhá při navigaci po genomu. The Projekt lidského genomu byl organizován do mapa a do sekvence the lidský genom. Zásadním krokem v projektu bylo vydání podrobné genomové mapy autorem Jean Weissenbach a jeho tým v Genoskop v Paříži.[11][12]
Referenční genom sekvence a mapy se nadále aktualizují, odstraňují chyby a objasňují oblasti s vysokou alelickou složitostí.[13] Klesající cena genomového mapování je povolena genealogický weby, které ji nabízejí jako službu,[14] do té míry, do jaké může člověk podrobit svůj genom crowdsourcing vědecké snahy jako např DNA.LAND na New York Genome Center,[15] příklad obou úspory z rozsahu a ze dne občanská věda.[16]
Virové genomy
Virové genomy mohou být složeny z RNA nebo DNA. Genomy RNA viry může být buď jednovláknová RNA nebo dvouřetězcová RNA a může obsahovat jednu nebo více samostatných molekul RNA (segmenty: monopartitový nebo multipartitový genom). DNA viry mohou mít jednořetězcové nebo dvouřetězcové genomy. Většina genomů viru DNA se skládá z jediné lineární molekuly DNA, ale některé jsou tvořeny kruhovou molekulou DNA.[17]Existuje také virová RNA zvaná jednovláknová RNA: slouží jako templát pro syntézu mRNA[18] a jednořetězcová RNA: slouží jako templát pro syntézu DNA.
Virová obálka[19] je vnější vrstva membrány, kterou virové genomy používají pro vstup do hostitelské buňky. Některé třídy virové DNA a RNA sestávají z virové obálky, zatímco jiné nikoli.
| Třída / rodina | Obálka? |
|---|---|
| Dvouvláknová DNA | |
| Adenovirus | Ne |
| Papilomavirus | Ne |
| Polyomavirus | Ne |
| Herpesvirus | Ano |
| Neštovice | Ano |
| Jednořetězcová DNA | |
| Parvovirus | Ne |
| Dvouvláknová RNA | |
| Reovirus | Ne |
| Jednořetězcová RNA | |
| Picornavirus | Ne |
| Koronavirus | Ano |
| Flavivirus | Ano |
| Togavirus | Ano |
| Jednořetězcová RNA: Slouží jako templát pro syntézu mRNA | |
| Filovirus | Ano |
| Orthomyxovirus | Ano |
| Paramyxovirus | Ano |
| Rhabdovirus | Ano |
| Single-Stranded RNA: Slouží jako templát pro syntézu DNA | |
| Retrovirus | Ano |
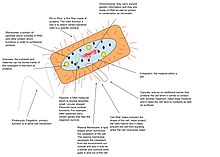
Prokaryotické genomy
Prokaryoty a eukaryoty mají DNA genomy. Archaea a většina bakterií mají jediný kruhový chromozom,[20] některé bakteriální druhy však mají lineární nebo více chromozomů.[21][22] Pokud se DNA replikuje rychleji, než se dělí bakteriální buňky, může být v jedné buňce přítomno více kopií chromozomu a pokud se buňky dělí rychleji, než je možné replikovat DNA, je zahájena vícenásobná replikace chromozomu, než dojde k rozdělení, umožňující dceřiným buňkám zdědit úplné genomy a již částečně replikované chromozomy. Většina prokaryot má ve svých genomech velmi málo opakující se DNA.[23] Někteří však symbiotické bakterie (např. Serratia symbiotica ) mají snížené genomy a vysoký podíl pseudogenů: pouze ~ 40% jejich DNA kóduje proteiny.[24][25]
Některé bakterie mají pomocný genetický materiál, který je také součástí jejich genomu, který je přenášen plazmidy. K tomu slovo genom by neměl být používán jako synonymum chromozóm.
Eukaryotické genomy
Eukaryotické genomy se skládají z jednoho nebo více lineárních chromozomů DNA. Počet chromozomů se velmi liší Jack jumper mravenci a nepohlavní nemotoda,[26] z nichž každý má pouze jeden pár, na a druhy kapradin který má 720 párů.[27] Typická lidská buňka má dvě kopie každé z 22 autosomy, jeden zděděný od každého rodiče, plus dva pohlavní chromozomy, což je diploidní. Gamety, jako jsou vajíčka, spermie, spory a pyl, jsou haploidní, což znamená, že nesou pouze jednu kopii každého chromozomu.
Kromě chromozomů v jádře, organel, jako je chloroplasty a mitochondrie mít vlastní DNA. O mitochondriích se někdy říká, že mají svůj vlastní genom, který se často označuje jako „mitochondriální genom "DNA nalezená v chloroplastu může být označována jako"plastom Stejně jako bakterie, z nichž pocházejí, mají mitochondrie a chloroplasty kruhový chromozom.
Na rozdíl od prokaryot mají eukaryota organizaci exon-intron proteinů kódujících geny a variabilní množství opakující se DNA. U savců a rostlin tvoří většinu genomu repetitivní DNA.[28]
Sekvence kódování
Sekvence DNA, které nesou pokyny k výrobě proteinů, se označují jako kódující sekvence. Podíl genomu obsazeného kódujícími sekvencemi se velmi liší. Větší genom nemusí nutně obsahovat více genů a podíl neopakující se DNA klesá spolu s rostoucí velikostí genomu u komplexních eukaryot.[28]

Nekódující sekvence
Mezi nekódující sekvence patří introny, sekvence pro nekódující RNA, regulační oblasti a opakující se DNA. Nekódující sekvence tvoří 98% lidského genomu. V genomu existují dvě kategorie repetitivní DNA: tandemové opakování a proložené opakování.[29]
Tandem se opakuje
Jsou volány krátké nekódující sekvence, které se opakují od hlavy k patě tandemové opakování. Mikrosatelity sestávající z 2-5 opakování základního páru, zatímco minisatelitní opakování jsou 30-35 bp. Tandemové repetice tvoří asi 4% lidského genomu a 9% genomu ovocné mušky.[30] Tandemové repetice mohou být funkční. Například, telomery jsou složeny z tandemové repetice TTAGGG u savců a hrají důležitou roli při ochraně konců chromozomu.
V ostatních případech může dojít k rozšíření počtu tandemových opakování v exonech nebo intronech choroba.[31] Například lidský gen huntingtin obvykle obsahuje 6–29 tandemových opakování nukleotidů CAG (kódujících polyglutaminový trakt). Výsledkem je expanze na více než 36 opakování Huntingtonova choroba neurodegenerativní onemocnění. Je známo, že dvacet lidských poruch je výsledkem podobných expanzí tandemových opakování v různých genech. Mechanismus, kterým proteiny s expandovanými polygulataminovými trakty způsobují smrt neuronů, není zcela objasněn. Jednou z možností je, že se proteiny nedokážou správně složit a zabránit degradaci, místo toho se hromadí v agregátech, které také sekvestrují důležité transkripční faktory, čímž mění genovou expresi.[31]
Tandemové repetice jsou obvykle způsobeny sklouznutím během replikace, nerovným křížením a genovou konverzí.[32]
Transponovatelné prvky
Transponovatelné prvky (TE) jsou sekvence DNA s definovanou strukturou, které jsou schopné změnit své umístění v genomu.[30][23][33] TE jsou kategorizovány buď jako TE třídy I, které se replikují mechanismem kopírování a vkládání, nebo TE třídy II, které lze z genomu vyříznout a vložit na nové místo.
Pohyb TE je hybnou silou evoluce genomu u eukaryot, protože jejich inzerce může narušit genové funkce, homologní rekombinace mezi TE může způsobit duplikace a TE může zamíchat exony a regulační sekvence na nová místa.[34]
Retrotranspozony
Retrotranspozony[35] se nacházejí většinou u eukaryot, ale nenacházejí se u prokaryot a retrotransposony tvoří velkou část genomů mnoha eukaryot. Retrotransposon je transponovatelný prvek, který se provádí prostřednictvím RNA středně pokročilí. Retrotranspozony[36] jsou složeny z DNA, ale jsou transkribovány do RNA pro transpozici, pak je transkript RNA zkopírován zpět do tvorby DNA pomocí specifického enzymu zvaného reverzní transkriptáza. Retrotransposony, které ve svém genu nesou reverzní transkriptázu, mohou spustit vlastní transpozici, ale geny, které nemají reverzní transkriptázu, musí používat reverzní transkriptázu syntetizovanou jiným retrotransposonem. Retrotranspozony mohou být transkribovány do RNA, které jsou poté duplikovány na jiném místě do genomu.[37] Retrotranspozony lze rozdělit na dlouhé opakování terminálu (LTRs) a nedlouhá opakování terminálu (Non-LTRs).[34]
Dlouhé opakování terminálu (LTR) jsou odvozeny ze starých retrovirových infekcí, takže kódují proteiny související s retrovirovými proteiny, včetně gag (strukturní proteiny viru), pol (reverzní transkriptáza a integráza), pro (proteáza) a v některých případech env (obálka) genů.[33] Tyto geny jsou ohraničeny dlouhými opakováními na obou 5 'a 3' koncích. Bylo hlášeno, že LTR se skládají z největší frakce ve většině rostlinných genomů a mohou odpovídat za obrovské rozdíly ve velikosti genomu.[38]
Non-long terminal repeats (Non-LTRs) jsou klasifikovány jako dlouho rozptýlené jaderné prvky (ŘÁDKY), krátké rozptýlené jaderné prvky (SINE) a prvky podobné Penelope (PLE). v Dictyostelium discoideum, do Non-LTR patří další prvky podobné DIRS. Non-LTR jsou široce rozšířeny v eukaryotických genomech.[39]
Dlouhé proložené prvky (LINE) kódují geny pro reverzní transkriptázu a endonukleázu, což z nich dělá autonomní transponovatelné prvky. Lidský genom má přibližně 500 000 ŘÁDKŮ, přičemž zaujímá přibližně 17% genomu.[40]
Krátké proložené prvky (SINE) jsou obvykle menší než 500 párů bází a jsou neautonomní, proto se při transpozici spoléhají na proteiny kódované LINE.[41] The Alu prvek je nejčastější SINE nalezený u primátů. Je to asi 350 bazických párů a zabírá asi 11% lidského genomu s přibližně 1 500 000 kopiemi.[34]
Transpozony DNA
Transpozony DNA kóduje enzym transpozázy mezi invertovanými terminálními opakováními. Když je exprimována, transpozáza rozpozná koncové invertované repetice, které lemují transposon, a katalyzuje jeho excizi a opětovné vložení do nového místa.[30] Tento mechanismus vyjmutí a vložení obvykle znovu vloží transpozony poblíž jejich původního umístění (do 100 kB).[34] Transpozony DNA se nacházejí v bakteriích a tvoří 3% lidského genomu a 12% genomu škrkavky C. elegans.[34]
Velikost genomu
Velikost genomu je celkový počet párů bází DNA v jedné kopii haploidního genomu. Velikost genomu se u různých druhů velmi liší. U lidí nukleární genom obsahuje přibližně 3,2 miliardy nukleotidů DNA, rozdělených na 24 lineárních molekul, nejkratší 50 000 000 nukleotidů na délku a nejdelší 260 000 000 nukleotidů, každý obsažený v jiném chromozomu.[42] Mezi morfologickou složitostí a velikostí genomu neexistuje jasná a konzistentní korelace prokaryoty nebo nižší eukaryoty.[28][43] Velikost genomu je do značné míry funkcí expanze a kontrakce opakujících se DNA prvků.
Vzhledem k tomu, že genomy jsou velmi složité, je jednou z výzkumných strategií snížení počtu genů v genomu na úplné minimum a stále musí dotyčný organismus přežít. Probíhá experimentální práce na minimálních genomech pro jednobuněčné organismy i na minimálních genomech pro mnohobuněčné organismy (viz Vývojová biologie ). Práce je obojí in vivo a in silico.[44][45]
Zde je tabulka některých významných nebo reprezentativních genomů. Vidět # Viz také pro seznamy sekvenovaných genomů.
| Typ organismu | Organismus | Velikost genomu (základní páry ) | Cca. Ne. genů | Poznámka | |
|---|---|---|---|---|---|
| Virus | Prasečí cirkovirus typ 1 | 1,759 | 1,8 kB | Nejmenší viry replikující se autonomně v eukaryotický buňky.[46] | |
| Virus | Bakteriofág MS2 | 3,569 | 3,5 kB | První sekvenovaný genom RNA[47] | |
| Virus | SV40 | 5,224 | 5,2 kB | [48] | |
| Virus | Fág Φ-X174 | 5,386 | 5,4 kB | První sekvenovaný genom DNA[49] | |
| Virus | HIV | 9,749 | 9,7 kB | [50] | |
| Virus | Fág λ | 48,502 | 48,5 kB | Často se používá jako vektor pro klonování rekombinantní DNA. | |
| Virus | Megavirus | 1,259,197 | 1,3 MB | Do roku 2013 největší známý virový genom.[54] | |
| Virus | Pandoravirus salinus | 2,470,000 | 2,47 MB | Největší známý virový genom.[55] | |
| Eukaryotický organela | Člověk mitochondrie | 16,569 | 16,6 kB | [56] | |
| Bakterie | Nasuia deltocephalinicola (kmen NAS-ALF) | 112,091 | 112 kB | 137 | Nejmenší známý nevirový genom. Symbiont z křískovití.[57] |
| Bakterie | Carsonella ruddii | 159,662 | 160 kB | An endosymbiont z psyllid hmyz | |
| Bakterie | Buchnera aphidicola | 600,000 | 600 kB | Endosymbiont z mšice[58] | |
| Bakterie | Wigglesworthia glossinidia | 700,000 | 700 kB | Symbiont ve střevech tsetse létat | |
| Bakterie – sinice | Prochlorococcus spp. (1,7 Mb) | 1,700,000 | 1,7 MB | 1,884 | Nejmenší známý genom sinice. Jeden z hlavních fotosyntetizátorů na Zemi.[59][60] |
| Bakterie | Haemophilus influenzae | 1,830,000 | 1,8 MB | První genom živého organismu sekvenován, červenec 1995[61] | |
| Bakterie | Escherichia coli | 4,600,000 | 4,6 MB | 4,288 | [62] |
| Bakterie - sinice | Nostoc punctiforme | 9,000,000 | 9 MB | 7,432 | 7432 otevřené čtecí rámce[63] |
| Bakterie | Solibacter usitatus (kmen Ellin 6076) | 9,970,000 | 10 MB | [64] | |
| Améboid | Polychaos dubium („Améba“ dubia) | 670,000,000,000 | 670 GB | Největší známý genom.[65] (Sporný)[66] | |
| Rostlina | Genlisea tuberosa | 61,000,000 | 61 MB | Nejmenší zaznamenaný kvetoucí rostlina genom, 2014.[67] | |
| Rostlina | Arabidopsis thaliana | 135,000,000[68] | 135 Mb | 27,655[69] | První rostlinný genom sekvenován, prosinec 2000.[70] |
| Rostlina | Populus trichocarpa | 480,000,000 | 480 MB | 73,013 | Sekvenován první genom stromu, září 2006[71] |
| Rostlina | Fritillaria assyriaca | 130,000,000,000 | 130 GB | ||
| Rostlina | Paris japonica (Japonský rodák, bledý okvětní lístek) | 150,000,000,000 | 150 GB | Největší známý rostlinný genom[72] | |
| Rostlina – mech | Physcomitrella patens | 480,000,000 | 480 MB | První genom a mechorost seřazeno, leden 2008.[73] | |
| Houba – droždí | Saccharomyces cerevisiae | 12,100,000 | 12,1 MB | 6,294 | Sekvenován první eukaryotický genom, 1996[74] |
| Houba | Aspergillus nidulans | 30,000,000 | 30 MB | 9,541 | [75] |
| Hlístice | Pratylenchus coffeae | 20,000,000 | 20 MB | [76] Nejmenší známý zvířecí genom[77] | |
| Hlístice | Caenorhabditis elegans | 100,300,000 | 100 MB | 19,000 | První mnohobuněčný zvířecí genom sekvenován, prosinec 1998[78] |
| Hmyz | Drosophila melanogaster (ovocný let) | 175,000,000 | 175 MB | 13,600 | Variace velikosti na základě napětí (175 - 180 MB; standardní y w kmen je 175Mb)[79] |
| Hmyz | Apis mellifera (včelí med) | 236,000,000 | 236 MB | 10,157 | [80] |
| Hmyz | Bombyx mori (hedvábná můra) | 432,000,000 | 432 MB | 14,623 | 14 623 předpovězených genů[81] |
| Hmyz | Solenopsis invicta (mravenec) | 480,000,000 | 480 MB | 16,569 | [82] |
| Savec | Mus musculus | 2,700,000,000 | 2,7 GB | 20,210 | [83] |
| Savec | Pan paniscus | 3,286,640,000 | 3,3 GB | 20,000 | Bonobo - odhadovaná velikost genomu 3,29 miliardy bp[84] |
| Savec | Homo sapiens | 3,000,000,000 | 3Gb | 20,000 | Homo sapiens velikost genomu odhadovaná na 3,2 Gbp v roce 2001[85][86] Počáteční sekvenování a analýza lidského genomu[87] |
| Pták | Gallus gallus | 1,043,000,000 | 1,0 GB | 20,000 | [88] |
| Ryba | Tetraodon nigroviridis (druh nafoukaných ryb) | 385,000,000 | 390 MB | Nejmenší známý genom obratlovců se odhaduje na 340 Mb[89][90] - 385 Mb.[91] | |
| Ryba | Protopterus aethiopicus (mramorovaný lungfish) | 130,000,000,000 | 130 GB | Největší známý genom obratlovců | |
Genomické změny
Všechny buňky organismu pocházejí z jedné buňky, takže se očekává, že budou mít identické genomy; v některých případech však vznikají rozdíly. Proces kopírování DNA během dělení buněk a expozice environmentálním mutagenům může vést k mutacím v somatických buňkách. V některých případech vedou takové mutace k rakovině, protože způsobují rychlejší dělení buněk a napadání okolních tkání.[92] U určitých lymfocytů v lidském imunitním systému V (D) J rekombinace generuje různé genomové sekvence, takže každá buňka produkuje jedinečnou protilátku nebo receptory T buněk.
V době redukční dělení buněk, diploidní buňky se dělí dvakrát za vzniku haploidních zárodečných buněk. Během tohoto procesu vede rekombinace k přeskupení genetického materiálu z homologních chromozomů, takže každá gameta má jedinečný genom.
Přeprogramování celého genomu
Přeprogramování celého genomu v myši prvotní zárodečné buňky zahrnuje epigenetický vymazání otisku vedoucí k totipotence. Přeprogramování je usnadněno aktivním Demetylace DNA, proces, který zahrnuje DNA oprava základní excize cesta.[93] Tato cesta se používá při mazání CpG methylace (5 mC) v prvotních zárodečných buňkách. Ke smazání 5 mC dochází jeho převodem na 5-hydroxymethylcytosin (5 hmC) poháněné vysokými hladinami deseti jedenácti dioxygenázových enzymů TET1 a TET2.[94]
Evoluce genomu
Genomy jsou více než součet organismů geny a mít vlastnosti, které mohou být měřeno a studoval bez odkazu na podrobnosti konkrétních genů a jejich produktů. Vědci porovnávají vlastnosti, jako je karyotyp (číslo chromozomu), velikost genomu, genový řád, zkreslení použití kodonů, a Obsah GC určit, jaké mechanismy mohly produkovat nejrůznější genomy, které dnes existují (nedávné přehledy viz Brown 2002; Saccone a Pesole 2003; Benfey a Protopapas 2004; Gibson a Muse 2004; Reese 2004; Gregory 2005).
Duplikace hrají hlavní roli při formování genomu. Duplikace se může pohybovat od rozšíření krátké tandemové opakování, k duplikaci shluku genů a až k duplikaci celých chromozomů nebo dokonce celé genomy. Taková zdvojení jsou pravděpodobně zásadní pro vytvoření genetické novinky.
Horizontální přenos genů je vysvětleno, jak často existuje extrémní podobnost mezi malými částmi genomů dvou organismů, které jsou jinak velmi vzdáleně příbuzné. Horizontální přenos genů se zdá být u mnoha běžný mikroby. Taky, eukaryotické buňky Zdá se, že došlo k přenosu nějakého genetického materiálu z jejich chloroplast a mitochondriální genomy k jejich jaderným chromozomům. Nedávná empirická data naznačují důležitou roli virů a subvirových RNA sítí, které představují hlavní hnací roli při generování genetické novinky a přirozené úpravy genomu.
V beletrii
Díla sci-fi ilustrují obavy ohledně dostupnosti sekvencí genomu.
Román Michaela Crichtona z roku 1990 Jurský park a následující film vyprávět příběh miliardáře, který vytvoří zábavní park klonovaných dinosaurů na vzdáleném ostrově, s katastrofálními následky. Genetik extrahuje DNA dinosaurů z krve starověkých komárů a vyplňuje mezery DNA z moderních druhů, aby vytvořil několik druhů dinosaurů. Teoretik chaosu je požádán, aby vydal svůj odborný názor na bezpečnost inženýrství ekosystému s dinosaury, a opakovaně varuje, že výsledky projektu budou nepředvídatelné a nakonec nekontrolovatelné. Tato varování o nebezpečích používání genomických informací jsou hlavním tématem knihy.
Film z roku 1997 Gattaca se odehrává ve futuristické společnosti, kde jsou genomy dětí konstruovány tak, aby obsahovaly nejideálnější kombinaci vlastností jejich rodičů, a metriky, jako je riziko srdečních onemocnění a předpokládaná délka života, jsou dokumentovány pro každou osobu na základě jejich genomu. Lidé počatí mimo eugenický program, známý jako „neplatní“, jsou diskriminováni a jsou zařazeni do podřadných povolání. Protagonistou filmu je In-Valid, který se snaží vzdorovat domnělé genetické přesile a dosáhnout svého snu pracovat jako vesmírný navigátor. Film varuje před budoucností, kde genomové informace podněcují předsudky a extrémní třídní rozdíly mezi těmi, kteří si mohou a nemohou dovolit geneticky upravené děti.[95]
Viz také
- Velikost bakteriálního genomu
- Kryokonzervace živočišných genetických zdrojů
- Prohlížeč genomu
- Překladač genomu
- Topologie genomu
- Celomanomová asociační studie
- Seznam sekvenovaných zvířecích genomů
- Seznam sekvenovaných archaeal genomů
- Seznam sekvenovaných bakteriálních genomů
- Seznam sekvenovaných eukaryotických genomů
- Seznam sekvenovaných genomů hub
- Seznam sekvenovaných rostlinných genomů
- Seznam sekvenovaných plastomů
- Seznam sekvenovaných protistických genomů
- Metagenomika
- Mikrobiom
- Molekulární epidemiologie
- Molekulárně patologická epidemiologie
- Molekulární patologie
- Sekvence nukleové kyseliny
- Pan-genom
- Přesná medicína
- Regulační gen
- Posloupnost
- Sekvenování celého genomu
Reference
- ^ Brosius, J (2009), „Fragmentovaný gen“, Annals of the New York Academy of Sciences, 1178 (1): 186–93, Bibcode:2009NYASA1178..186B, doi:10.1111 / j.1749-6632.2009.05004.x, PMID 19845638, S2CID 8279434
- ^ Ridley M (2006). Genom: autobiografie druhu ve 23 kapitolách (PDF). New York: Harperova trvalka. ISBN 978-0-06-019497-0. Archivovány od originál (PDF) dne 24. října 2018. Citováno 11. května 2016.
- ^ Winkler HL (1920). Verbreitung und Ursache der Parthenogenesis im Pflanzen- und Tierreiche. Jena: Verlag Fischer.
- ^ „definice genomu ve slovníku Oxford“. Citováno 25. března 2014.
- ^ Lederberg J, McCray AT (2001). "'Ome Sweet 'Omics - Genealogická pokladnice slov " (PDF). Vědec. 15 (7). Archivovány od originál (PDF) dne 29. září 2006.
- ^ „Vše o genech“. www.beowulf.org.uk.
- ^ „Domov genomu“. 8. prosince 2010. Citováno 27. ledna 2011.
- ^ Zimmer C. (18. prosince 2013). „Fosilní toe poskytuje kompletní neandertálský genom“. The New York Times. Citováno 18. prosince 2013.
- ^ Prüfer K, Racimo F, Patterson N, Jay F, Sankararaman S, Sawyer S a kol. (Leden 2014). „Kompletní sekvence genomu neandertálce z pohoří Altaj“. Příroda. 505 (7481): 43–49. Bibcode:2014Natur.505 ... 43P. doi:10.1038 / příroda12886. PMC 4031459. PMID 24352235.
- ^ Wade N (31. května 2007). „Genom DNA Pioneer je rozluštěn“. The New York Times. Citováno 2. dubna 2010.
- ^ „Co je to genom?“. Genomenewsnetwork.org. 15. ledna 2003. Citováno 27. ledna 2011.
- ^ NCBI_user_services (29. března 2004). „Informační přehled o mapování“. Archivovány od originál dne 19. července 2010. Citováno 27. ledna 2011.
- ^ Konsorcium pro genomové reference. „Sestavení genomu“. Citováno 23. srpna 2016.
- ^ Kaplan, Sarah (17. dubna 2016). „Jak vašich 20 000 genů určuje tolik divoce odlišných rysů?. The Washington Post. Citováno 27. srpna 2016.
- ^ Podívejte se na Hayden, Erika (2015). „Vědci doufají, že přilákají miliony lidí do‚ DNA.LAND'". Příroda. doi:10.1038 / příroda.2015.18514.
- ^ Zimmer, Carle. „Game of Genomes, Episode 13: Answers and Questions“. STAT. Citováno 27. srpna 2016.
- ^ Gelderblom, Hans R. (1996). Lékařská mikrobiologie (4. vydání). Galveston, TX: Lékařská pobočka University of Texas v Galvestonu.
- ^ Urry, Lisa A. (2016). Campbell Biology: sedmé vydání. New York: Hoboken: Pearson Higher Education. 403–404. ISBN 0134093410.
- ^ Urry, Lisa A (2016). Campbell Biology: sedmé vydání. New York: Hoboken: Pearson Higher Education. 403–404. ISBN 0134093410.
- ^ Samson RY, Bell SD (2014). "Biologie chromozomu archaea". Journal of Molecular Microbiology and Biotechnology. 24 (5–6): 420–27. doi:10.1159/000368854. PMC 5175462. PMID 25732343.
- ^ Chaconas G, Chen CW (2005). „Replikace lineárních bakteriálních chromozomů: Již se neodehrává v kruzích“. Bakteriální chromozom: 525–540. doi:10.1128 / 9781555817640.ch29. ISBN 9781555812324.
- ^ „Bakteriální chromozomy“. Mikrobiální genetika. 2002.
- ^ A b Koonin EV, Wolf YI (červenec 2010). „Omezení a plasticita ve vývoji genomu a molekulárního fenomu“. Recenze přírody. Genetika. 11 (7): 487–98. doi:10.1038 / nrg2810. PMC 3273317. PMID 20548290.
- ^ McCutcheon JP, Moran NA (listopad 2011). "Extrémní redukce genomu v symbiotických bakteriích". Recenze přírody. Mikrobiologie. 10 (1): 13–26. doi:10.1038 / nrmicro2670. PMID 22064560. S2CID 7175976.
- ^ Land M, Hauser L, Jun SR, Nookaew I, Leuze MR, Ahn TH, Karpinets T, Lund O, Kora G, Wassenaar T, Poudel S, Ussery DW (březen 2015). „Pohledy na 20 let sekvenování bakteriálního genomu“. Funkční a integrační genomika. 15 (2): 141–61. doi:10.1007 / s10142-015-0433-4. PMC 4361730. PMID 25722247.
- ^ „Vědci sledují nepohlavního malého červa, jehož linie sahá 18 milionů let zpět“. ScienceDaily. Citováno 7. listopadu 2017.
- ^ Khandelwal S (březen 1990). „Vývoj chromozomů v rodu Ophioglossum L.“. Botanical Journal of the Linnean Society. 102 (3): 205–17. doi:10.1111 / j.1095-8339.1990.tb01876.x.
- ^ A b C Lewin B (2004). Geny VIII (8. vydání). Horní sedlo, NJ: Pearson / Prentice Hall. ISBN 978-0-13-143981-8.
- ^ Stojanovic N, vyd. (2007). Výpočetní genomika: současné metody. Wymondham: Horizon Bioscience. ISBN 978-1-904933-30-4.
- ^ A b C Padeken J, Zeller P, Gasser SM (duben 2015). "Opakujte DNA v organizaci a stabilitě genomu". Aktuální názor na genetiku a vývoj. 31: 12–19. doi:10.1016 / j.gde.2015.03.009. PMID 25917896.
- ^ A b Usdin K (červenec 2008). „Biologické účinky jednoduchých tandemových opakování: poučení z nemocí z opakované expanze“. Výzkum genomu. 18 (7): 1011–19. doi:10.1101 / gr.070409.107. PMC 3960014. PMID 18593815.
- ^ Li YC, Korol AB, Fahima T, Beiles A, Nevo E (prosinec 2002). „Mikrosatelity: genomová distribuce, domnělé funkce a mutační mechanismy: přehled“. Molekulární ekologie. 11 (12): 2453–65. doi:10.1046 / j.1365-294X.2002.01643.x. PMID 12453231. S2CID 23606208.
- ^ A b Wessler SR (listopad 2006). "Transponovatelné prvky a vývoj eukaryotických genomů". Sborník Národní akademie věd Spojených států amerických. 103 (47): 17600–01. Bibcode:2006PNAS..10317600W. doi:10.1073 / pnas.0607612103. PMC 1693792. PMID 17101965.
- ^ A b C d E Kazazian HH (březen 2004). "Mobilní prvky: ovladače evoluce genomu". Věda. 303 (5664): 1626–32. Bibcode:2004Sci ... 303.1626K. doi:10.1126 / science.1089670. PMID 15016989. S2CID 1956932.
- ^ "Transposon | genetika". Encyklopedie Britannica. Citováno 5. prosince 2020.
- ^ Sanders, Mark Frederick (2019). Genetická analýza: třetí vydání integrovaného přístupu. New York: Pearson, stále se učí a mastering. p. 425. ISBN 9780134605173.
- ^ Deininger PL, Moran JV, Batzer MA, Kazazian HH (prosinec 2003). "Mobilní prvky a evoluce genomu savců". Aktuální názor na genetiku a vývoj. 13 (6): 651–58. doi:10.1016 / j.gde.2003.10.013. PMID 14638329.
- ^ Kidwell MG, Lisch DR (březen 2000). "Prenosné prvky a vývoj hostitelského genomu". Trendy v ekologii a evoluci. 15 (3): 95–99. doi:10.1016 / S0169-5347 (99) 01817-0. PMID 10675923.
- ^ Richard GF, Kerrest A, Dujon B (prosinec 2008). „Srovnávací genomika a molekulární dynamika opakování DNA u eukaryot“. Recenze mikrobiologie a molekulární biologie. 72 (4): 686–727. doi:10.1128 / MMBR.00011-08. PMC 2593564. PMID 19052325.
- ^ Cordaux R, Batzer MA (říjen 2009). „Dopad retrotranspozonů na evoluci lidského genomu“. Recenze přírody. Genetika. 10 (10): 691–703. doi:10.1038 / nrg2640. PMC 2884099. PMID 19763152.
- ^ Han JS, Boeke JD (srpen 2005). „LINE-1 retrotranspozony: modulátory kvantity a kvality genové exprese savců?“. BioEssays. 27 (8): 775–84. doi:10.1002 / bies.20257. PMID 16015595. S2CID 26424042.
- ^ "Lidský genom". Citováno 19. srpna 2016.
- ^ Gregory TR, Nicol JA, Tamm H, Kullman B, Kullman K, Leitch IJ, Murray BG, Kapraun DF, Greilhuber J, Bennett MD (leden 2007). „Databáze velikosti eukaryotického genomu“. Výzkum nukleových kyselin. 35 (Problém s databází): D332–38. doi:10.1093 / nar / gkl828. PMC 1669731. PMID 17090588.
- ^ Glass JI, Assad-Garcia N, Alperovich N, Yooseph S, Lewis MR, Maruf M, Hutchison CA, Smith HO, Venter JC (leden 2006). „Esenciální geny minimální bakterie“. Sborník Národní akademie věd Spojených států amerických. 103 (2): 425–30. Bibcode:2006PNAS..103..425G. doi:10.1073 / pnas.0510013103. PMC 1324956. PMID 16407165.
- ^ Forster AC, Church GM (2006). „Směrem k syntéze minimální buňky“. Molekulární systémy biologie. 2 (1): 45. doi:10.1038 / msb4100090. PMC 1681520. PMID 16924266.
- ^ Mankertz P (2008). „Molekulární biologie prasatových cirkovirů“. Živočišné viry: Molekulární biologie. Caister Academic Press. ISBN 978-1-904455-22-6.
- ^ Fiers W, Contreras R, Duerinck F, Haegeman G, Iserentant D, Merregaert J, Min Jou W, Molemans F, Raeymaekers A, Van den Berghe A, Volckaert G, Ysebaert M (duben 1976). "Kompletní nukleotidová sekvence bakteriofága MS2 RNA: primární a sekundární struktura replikázového genu". Příroda. 260 (5551): 500–07. Bibcode:1976 Natur.260..500F. doi:10.1038 / 260500a0. PMID 1264203. S2CID 4289674.
- ^ Fiers W, Contreras R, Haegemann G, Rogiers R, Van de Voorde A, Van Heuverswyn H, Van Herreweghe J, Volckaert G, Ysebaert M (květen 1978). "Kompletní nukleotidová sekvence DNA SV40". Příroda. 273 (5658): 113–20. Bibcode:1978Natur.273..113F. doi:10.1038 / 273113a0. PMID 205802. S2CID 1634424.
- ^ Sanger F, Air GM, Barrell BG, Brown NL, Coulson AR, Fiddes CA, Hutchison CA, Slocombe PM, Smith M (únor 1977). "Nukleotidová sekvence DNA bakteriofága phi X174". Příroda. 265 (5596): 687–95. Bibcode:1977 Natur.265..687S. doi:10.1038 / 265687a0. PMID 870828. S2CID 4206886.
- ^ "Virology - Virus lidské imunodeficience a AIDS, struktura: genom a proteiny HIV". Pathmicro.med.sc.edu. 1. července 2010. Citováno 27. ledna 2011.
- ^ Thomason L, Court DL, Bubunenko M, Costantino N, Wilson H, Datta S, Oppenheim A (duben 2007). "Rekombinace: genetické inženýrství v bakteriích pomocí homologní rekombinace". Současné protokoly v molekulární biologii. Kapitola 1: Jednotka 1.16. doi:10.1002 / 0471142727.mb0116s78. ISBN 978-0-471-14272-0. PMID 18265390. S2CID 490362.
- ^ Court DL, Oppenheim AB, Adhya SL (leden 2007). „Nový pohled na genetické sítě bakteriofága lambda“. Journal of Bacteriology. 189 (2): 298–304. doi:10.1128 / JB.01215-06. PMC 1797383. PMID 17085553.
- ^ Sanger F, Coulson AR, Hong GF, Hill DF, Petersen GB (prosinec 1982). "Nukleotidová sekvence DNA bakteriofága lambda". Journal of Molecular Biology. 162 (4): 729–73. doi:10.1016/0022-2836(82)90546-0. PMID 6221115.
- ^ Legendre M, Arslan D, Abergel C, Claverie JM (leden 2012). „Genomika megaviru a nepolapitelná čtvrtá doména života“. Komunikativní a integrativní biologie. 5 (1): 102–06. doi:10,4161 / cib.18624. PMC 3291303. PMID 22482024.
- ^ Philippe N, Legendre M, Doutre G, Couté Y, Poirot O, Lescot M, Arslan D, Seltzer V, Bertaux L, Bruley C, Garin J, Claverie JM, Abergel C (červenec 2013). „Pandoraviry: viry améby s genomy do 2,5 Mb dosahujícími parazitické eukaryoty“ (PDF). Věda. 341 (6143): 281–86. Bibcode:2013Sci ... 341..281P. doi:10.1126 / science.1239181. PMID 23869018. S2CID 16877147.
- ^ Anderson S, Bankier AT, Barrell BG, de Bruijn MH, Coulson AR, Drouin J, Eperon IC, Nierlich DP, Roe BA, Sanger F, Schreier PH, Smith AJ, Staden R, Young IG (duben 1981). "Pořadí a organizace lidského mitochondriálního genomu". Příroda. 290 (5806): 457–65. Bibcode:1981 Natur.290..457A. doi:10.1038 / 290457a0. PMID 7219534. S2CID 4355527.
- ^ Bennett GM, Moran NA (5. srpna 2013). „Malý, menší, nejmenší: počátky a vývoj starodávných duálních symbióz v hmyzu, který se živí floémem“. Biologie genomu a evoluce. 5 (9): 1675–88. doi:10.1093 / gbe / evt118. PMC 3787670. PMID 23918810.
- ^ Shigenobu S, Watanabe H, Hattori M, Sakaki Y, Ishikawa H (září 2000). "Sekvence genomu endocelulárního bakteriálního symbiontu mšic Buchnera sp. APS". Příroda. 407 (6800): 81–86. Bibcode:2000Natur.407 ... 81S. doi:10.1038/35024074. PMID 10993077.
- ^ Rocap G, Larimer FW, Lamerdin J, Malfatti S, Chain P, Ahlgren NA, et al. (Srpen 2003). „Divergence genomu ve dvou ekotypech Prochlorococcus odráží diferenciaci oceánských výklenků“. Příroda. 424 (6952): 1042–47. Bibcode:2003 Natur.424.1042R. doi:10.1038 / nature01947. PMID 12917642. S2CID 4344597.
- ^ Dufresne A, Salanoubat M, Partensky F, Artiguenave F, Axmann IM, Barbe V a kol. (Srpen 2003). „Sekvence genomu sinic Prochlorococcus marinus SS120, téměř minimální oxyfototrofní genom“. Sborník Národní akademie věd Spojených států amerických. 100 (17): 10020–25. Bibcode:2003PNAS..10010020D. doi:10.1073 / pnas.1733211100. PMC 187748. PMID 12917486.
- ^ Fleischmann RD, Adams MD, White O, Clayton RA, Kirkness EF, Kerlavage AR, Bult CJ, Tomb JF, Dougherty BA, Merrick JM (červenec 1995). „Náhodné sekvenování a shromáždění celého genomu Haemophilus influenzae Rd“. Věda. 269 (5223): 496–512. Bibcode:1995Sci ... 269..496F. doi:10.1126 / science.7542800. PMID 7542800. S2CID 10423613.
- ^ Blattner FR, Plunkett G, Bloch CA, Perna NT, Burland V, Riley M a kol. (Září 1997). „Kompletní genomová sekvence Escherichia coli K-12“. Věda. 277 (5331): 1453–62. doi:10.1126 / science.277.5331.1453. PMID 9278503.
- ^ Meeks JC, Elhai J, Thiel T, Potts M, Larimer F, Lamerdin J, Predki P, Atlas R (2001). „Přehled genomu Nostoc punctiforme, mnohobuněčné symbiotické sinice“. Fotosyntetický výzkum. 70 (1): 85–106. doi:10.1023 / A: 1013840025518. PMID 16228364. S2CID 8752382.
- ^ Challacombe JF, Eichorst SA, Hauser L, Land M, Xie G, Kuske CR (15. září 2011). Steinke D (ed.). „Biologické důsledky získávání a duplikace starých genů ve velkém genomu Candidatus Solibacter usitatus Ellin6076“. PLOS ONE. 6 (9): e24882. Bibcode:2011PLoSO ... 624882C. doi:10.1371 / journal.pone.0024882. PMC 3174227. PMID 21949776.
- ^ Parfrey LW, Lahr DJ, Katz LA (duben 2008). „Dynamická povaha eukaryotických genomů“. Molekulární biologie a evoluce. 25 (4): 787–94. doi:10.1093 / molbev / msn032. PMC 2933061. PMID 18258610.
- ^ ScienceShot: dosud největší genom Archivováno 11. října 2010 v Wayback Machine, komentáře: „Měření pro Amoeba dubia a další prvoky, u nichž se uvádí, že mají velmi velké genomy, bylo provedeno v 60. letech pomocí hrubého biochemického přístupu, který je nyní považován za nespolehlivou metodu pro přesné stanovení velikosti genomu.“
- ^ Fleischmann A, Michael TP, Rivadavia F, Sousa A, Wang W, Temsch EM, Greilhuber J, Müller KF, Heubl G (prosinec 2014). „Vývoj velikosti genomu a počtu chromozomů v rodu masožravých rostlin Genlisea (Lentibulariaceae), s novým odhadem minimální velikosti genomu v krytosemenných rostlinách“. Annals of Botany. 114 (8): 1651–63. doi:10.1093 / aob / mcu189. PMC 4649684. PMID 25274549.
- ^ "Shromáždění genomu". Informační zdroj Arabidopsis (TAIR).
- ^ "Podrobnosti - Arabidopsis thaliana - Genomy souboru 40". plants.ensembl.org.
- ^ Greilhuber J, Borsch T, Müller K, Worberg A, Porembski S, Barthlott W (listopad 2006). "Nejmenší krytosemenné genomy nalezené v lentibulariaceae s chromozomy o velikosti bakterií". Biologie rostlin. 8 (6): 770–77. doi:10.1055 / s-2006-924101. PMID 17203433.
- ^ Tuskan GA, Difazio S, Jansson S, Bohlmann J, Grigoriev I, Hellsten U a kol. (Září 2006). „Genom černého topolu, Populus trichocarpa (Torr. & Gray)“ (PDF). Věda. 313 (5793): 1596–604. Bibcode:2006Sci ... 313.1596T. doi:10.1126 / science.1128691. PMID 16973872. S2CID 7717980.
- ^ Pellicer J, Fay MF, Leitch IJ (15. září 2010). „Největší eukaryotický genom ze všech?“. Botanical Journal of the Linnean Society. 164 (1): 10–15. doi:10.1111 / j.1095-8339.2010.01072.x.
- ^ Lang D, Zimmer AD, Rensing SA, Reski R (říjen 2008). „Zkoumání biologické rozmanitosti rostlin: genom Physcomitrella a další“. Trendy ve vědě o rostlinách. 13 (10): 542–49. doi:10.1016 / j.tplantts.2008.07.002. PMID 18762443.
- ^ "Databáze genomu Saccharomyces". Yeastgenome.org. Citováno 27. ledna 2011.
- ^ Galagan JE, Calvo SE, Cuomo C, Ma LJ, Wortman JR, Batzoglou S a kol. (Prosinec 2005). "Sekvenování Aspergillus nidulans a srovnávací analýza s A. fumigatus a A. oryzae". Příroda. 438 (7071): 1105–15. Bibcode:2005 Natur.438.1105G. doi:10.1038 / příroda04341. PMID 16372000.
- ^ Leroy S, Bouamer S, Morand S, Fargette M (2007). "Velikost genomu háďátek parazitujících na rostlinách". Nematologie. 9 (3): 449–50. doi:10.1163/156854107781352089.
- ^ Gregory TR (2005). „Databáze velikostí zvířecích genomů“. Gregory, T.R. (2016). Databáze velikostí zvířecích genomů.
- ^ The C. elegans Konsorcium pro sekvenování (prosinec 1998). „Sekvence genomu hlístice C. elegans: platforma pro zkoumání biologie“. Věda. 282 (5396): 2012–18. Bibcode:1998Sci ... 282.2012.. doi:10.1126 / science.282.5396.2012. PMID 9851916. S2CID 16873716.
- ^ Ellis LL, Huang W, Quinn AM, Ahuja A, Alfrejd B, Gomez FE, Hjelmen CE, Moore KL, Mackay TF, Johnston JS, Tarone AM (červenec 2014). „Variace velikosti intrapopulačního genomu u D. melanogaster odráží variace a plastičnost životních dějin“. Genetika PLOS. 10 (7): e1004522. doi:10.1371 / journal.pgen.1004522. PMC 4109859. PMID 25057905.
- ^ Konsorcium pro sekvenování genomu včel včel (říjen 2006). „Pohledy na sociální hmyz z genomu včely Apis mellifera“. Příroda. 443 (7114): 931–49. Bibcode:2006Natur.443..931T. doi:10.1038 / nature05260. PMC 2048586. PMID 17073008.
- ^ Mezinárodní genom bource morušového (prosinec 2008). „Genom lepidopteranského modelového hmyzu, bource morušového Bombyx mori“. Hmyzí biochemie a molekulární biologie. 38 (12): 1036–45. doi:10.1016 / j.ibmb.2008.11.004. PMID 19121390.
- ^ Wurm Y, Wang J, Riba-Grognuz O, Corona M, Nygaard S, Hunt BG a kol. (Duben 2011). „Genom požárního mravence Solenopsis invicta“. Sborník Národní akademie věd Spojených států amerických. 108 (14): 5679–84. Bibcode:2011PNAS..108,5679W. doi:10.1073 / pnas.1009690108. PMC 3078418. PMID 21282665.
- ^ Church DM, Goodstadt L, Hillier LW, Zody MC, Goldstein S, She X a kol. (Květen 2009). Roberts RJ (ed.). "Biologie specifická pro rod odhalená hotovým genomovým shromážděním myši". PLOS Biology. 7 (5): e1000112. doi:10.1371 / journal.pbio.1000112. PMC 2680341. PMID 19468303.
- ^ „Pan paniscus (trpasličí šimpanz)“. nih.gov. Citováno 30. června 2016.
- ^ Eric Lander; et al. (15. února 2001). "Počáteční sekvenování a analýza lidského genomu". Příroda. 409 (6822): 860–921. doi:10.1038/35057062. PMID 11237011. Tabulka 8.
- ^ „Informační list o funkční a srovnávací genomice“. Ornl.gov. Archivovány od originál dne 20. září 2008.
- ^ Venter JC Adams MD, Myers EW, Li PW, Mural RJ, Sutton GG a kol. (Únor 2001). „Sekvence lidského genomu“. Věda. 291 (5507): 1304–51. Bibcode:2001Sci ... 291.1304V. doi:10.1126 / science.1058040. PMID 11181995.
- ^ Konsorcium pro sekvenování mezinárodního kuřecího genomu (prosinec 2004). „Sekvence a srovnávací analýza kuřecího genomu poskytují jedinečné pohledy na vývoj obratlovců“. Příroda. 432 (7018): 695–716. Bibcode:2004 Natur.432..695C. doi:10.1038 / nature03154. ISSN 0028-0836. PMID 15592404.
- ^ Roest Crollius H, Jaillon O, Dasilva C, Ozouf-Costaz C, Fizames C, Fischer C, Bouneau L, Billault A, Quetier F, Saurin W, Bernot A, Weissenbach J (červenec 2000). „Charakterizace a opakovaná analýza kompaktního genomu sladkovodních pufferů Tetraodon nigroviridis“. Výzkum genomu. 10 (7): 939–49. doi:10,1101 / gr. 10.7.939. PMC 310905. PMID 10899143.
- ^ Jaillon O, Aury JM, Brunet F, Petit JL, Stange-Thomann N, Mauceli E a kol. (Říjen 2004). „Duplikace genomu u teleostních ryb Tetraodon nigroviridis odhaluje časný proto-karyotyp obratlovců“. Příroda. 431 (7011): 946–57. Bibcode:2004 Natur.431..946J. doi:10.1038 / nature03025. PMID 15496914.
- ^ „Informace o projektu Tetraodon“. Archivovány od originál dne 26. září 2012. Citováno 17. října 2012.
- ^ Martincorena I, Campbell PJ (září 2015). "Somatická mutace v rakovině a normálních buňkách". Věda. 349 (6255): 1483–89. Bibcode:2015Sci ... 349.1483M. doi:10.1126 / science.aab4082. PMID 26404825. S2CID 13945473.
- ^ Hajkova P, Jeffries SJ, Lee C, Miller N, Jackson SP, Surani MA (červenec 2010). „Přeprogramování celého genomu v linii zárodečných myší znamená cestu základní excize opravy“. Věda. 329 (5987): 78–82. Bibcode:2010Sci ... 329 ... 78H. doi:10.1126 / science.1187945. PMC 3863715. PMID 20595612.
- ^ Hackett JA, Sengupta R, Zylicz JJ, Murakami K, Lee C, Down TA, Surani MA (leden 2013). „Dynamika demylace DNA Germline a mazání otisků prostřednictvím 5-hydroxymethylcytosinu“. Věda. 339 (6118): 448–52. Bibcode:2013Sci ... 339..448H. doi:10.1126 / science.1229277. PMC 3847602. PMID 23223451.
- ^ „Gattaca (film)“. Shnilá rajčata.
Další čtení
- Benfey P, Protopapas AD (2004). Základy genomiky. Prentice Hall.
- Brown TA (2002). Genomy 2. Oxford: Bios Scientific Publishers. ISBN 978-1-85996-029-5.
- Gibson G, Muse SV (2004). Primer genomové vědy (Druhé vydání.). Sunderland, Massachusetts: Sinauer Assoc. ISBN 978-0-87893-234-4.
- Gregory TR (2005). Evoluce genomu. Elsevier. ISBN 978-0-12-301463-4.
- Reece RJ (2004). Analýza genů a genů. Chichester: John Wiley & Sons. ISBN 978-0-470-84379-6.
- Saccone C, Pesole G (2003). Příručka srovnávací genomiky. Chichester: John Wiley & Sons. ISBN 978-0-471-39128-9.
- Werner E (prosinec 2003). „V biologii mnohobuněčných systémů in silico a minimálních genomech“. Objev drog dnes. 8 (24): 1121–27. doi:10.1016 / S1359-6446 (03) 02918-0. PMID 14678738.
externí odkazy
- UCSC Genome Browser - zobrazit genom a anotace pro více než 80 organismů.
- genomecenter.howard.edu
- Vytvořte molekulu DNA
- Některé srovnávací velikosti genomu
- DNA Interactive: The History of DNA Science
- DNA od začátku
- Vše o projektu lidského genomu —Z Genome.gov
- Databáze velikostí zvířecích genomů
- Plant genome size database
- GOLD:Genomes OnLine Database
- The Genome News Network
- NCBI Entrez Genome Project database
- NCBI Genome Primer
- Genové karty —an integrated database of human genes
- BBC News – Final genome 'chapter' published
- IMG (The Integrated Microbial Genomes system)—for genome analysis by the DOE-JGI
- GeKnome Technologies Next-Gen Sequencing Data Analysis —next-generation sequencing data analysis for Illumina a 454 Service from GeKnome Technologies.

