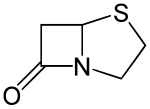
Penam - Penam
 | |
| Jména | |
|---|---|
| Název IUPAC (5R) -4-thia-l-azabicyklo [3.2.0] heptan-7-on | |
| Ostatní jména L-Aza-7-oxo-4-thiabicyklo [3.2.0] heptan | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Vlastnosti | |
| C5H7NÓS | |
| Molární hmotnost | 129.18 g · mol−1 |
| Související sloučeniny | |
Související sloučeniny | klavam |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |

Penams jsou primární skeletové struktury, které definují Penicilin podtřída širšího β-laktam rodina antibiotika a příbuzné sloučeniny. Jsou to bicyklické kruhové systémy obsahující β-laktamovou skupinu fúzovanou s pětičlenným členem thiazolidin prsten. [1] Kvůli deformaci kruhu a omezením amidové rezonance je struktura nestabilní a vysoce náchylná k katalytickému štěpení na amidové vazbě.[2] Benzylpenicilin (Penicilin G) je přírodní produkt mateřské látky, který obsahuje strukturu penamu.
Struktura a lepení
Penamy nemají pružné struktury, kvůli jejich složení tuhých malých kroužků. Čtyřčlenný kruh a pětičlenný kruh nejsou koplanární. Místo toho je struktura uzamčena v zúženém (tj. Ohnutém) tvaru kvůli pyramidové geometrii dusíku předmostí. Pyramidalizace (χ = 54 °) a kroucení vazby C-N (τ = 18 °) je způsobeno napětím z vyloučení osamělého páru z rovinnosti s cyklickými kruhy a elektrostatickými odpuzujícími účinky. Výsledkem je, že zkreslená vazba C-N způsobuje nesouosost orbitalů karbonylového uhlíku a dusíkového osamělého páru, které umožňují překrývání rezonance. Délka amidové vazby C-N je 1,406 Á a zobrazuje větší charakter jednoduché vazby než v necyklických terciárních amidech. Délka vazby C-O je 1,205 Á, což je méně než vazby CO v necyklických terciárních amidech.[3]
Vlastnosti
Stabilita
Celková termodynamická stabilita Penamu je založena na součtu napětí v kruhu destabilizační účinky (RSE) a amid rezonance stabilizační účinky (ARE). Protože destabilizační účinky daleko převyšují stabilizační účinky, jsou penamy termodynamicky nestabilní a reagují na nukleofilní reakce, které upřednostňují štěpení β-laktamového kruhu.[4]
Efekt kmenového kmene
Penamy jsou primárně destabilizovány z důvodu velkého úhlu a torzních napětí, která jsou spojena se čtyřčlenným β-laktamovým kruhem, jehož vnitřní úhly vazby jsou 90 °.[5] Na základě podobných kmenových energií pozorovaných v penamech a samostatných β-laktamových kruzích, kondenzovaný pětičlenný kruh pravděpodobně nepřispívá k celkovému účinku kmene na rozdíl od jeho šestičlenného protějšku v cefamech, který pomohl snížit kmenové napětí.[4] Výsledkem je, že reakce otevření kruhu, například hydrolýza, jsou termodynamicky příznivé pro jejich odlehčení tahu kruhu.[5]
Amidový rezonanční efekt
Penamy jsou stabilizovány amidovými rezonančními účinky. Na rozdíl od tradičních terciárních amidů, které delokalizují volný dusíkový pár na kyslík karbonylové skupiny a mají za následek dvojnou vazbu na vazbě CN, dochází k amidové rezonanci v penamu primárně mezi dusíkem a karbonylovým uhlíkem, což je částečně pozitivní díky indukčnímu účinku karbonylu kyslík. To je výsledkem překrývajících se interakcí mezi osamělým párem HOMO na dusíku a LUMO uhlíku. Avšak vzhledem k pyramidalizaci dusíku a zkreslené vazbě C-N je stupeň stabilizace amidové rezonance snížen, s ohledem na rovinné amidy, jako je β-laktamová část, které mají zarovnané orbitaly pro překrytí.[6][3]
Reakce
Penamy reagují na katalytické štěpení hydrolýzou, protože karbonylový uhlík má sklon k nukleofilním útokům.[5] To je pochopitelné jeho částečným pozitivním (elektrofilním) charakterem, který je výsledkem mírného odběru elektronové hustoty atomem karbonylového kyslíku a následkem toho nedostatek konjugace mezi dusíkovou a karbonylovou skupinou. Ačkoli amidové vazby jsou obvykle nereaktivní na štěpení kvůli svému částečnému charakteru dvojné vazby, pyramidalizace a zkreslení vazby C-N způsobují, že amidová vazba v penamech má charakter jednoduché vazby, což je více reaktivní na štěpení.[4][6][3] Štěpení vazby C-N je také termodynamicky příznivé, protože otevření β-laktamového kruhu snižuje napětí v kruhu. [5]
Katalyzované štěpení
Otevírání kruhů penamů může být katalyzováno kyselinou nebo zásadou hydrolýza. [4][6]V kyselých podmínkách působí voda jako nukleofil, který napadá elektrofilní uhlík karbonylové skupiny. Za základních podmínek působí hydroxid jako nukleofil. V enzymech působí hydroxylová skupina serinového zbytku jako nukleofil.[5] Bez ohledu na to, které nukleofilní druhy napadají elektrofilní uhlík karbonylové skupiny, se nukleofil váže a vytváří terciární uhlíkový meziprodukt. Elektrony se přenášejí z vazby C-N na atom dusíku, který působí jako odstupující skupina. Výsledkem je, že vazba C-N se odštěpí za vzniku karboxylové kyseliny a sekundárního aminu.[5]
Reference
- ^ Novak, Igor; Chua, Pei Juan (01.09.2006). "Výpočetní studie lékopisů: β-laktamy". The Journal of Physical Chemistry A. 110 (35): 10521–10524. doi:10.1021 / jp063162b. ISSN 1089-5639. PMID 16942059.
- ^ Patrick, Graham (2017-03-23), „5. Farmaceutika a léčivá chemie“, Organická chemie: velmi krátký úvod, Oxford University Press, s. 71–89, doi:10.1093 / actrade / 9780198759775.003.0005, ISBN 978-0-19-875977-5
- ^ A b C Glover, Stephen A .; Rosser, Adam A. (2012-06-14). "Spolehlivé stanovení amidicity v acyklických amidech a laktamech". The Journal of Organic Chemistry. 77 (13): 5492–5502. doi:10.1021 / jo300347k. ISSN 0022-3263. PMID 22646836.
- ^ A b C d Novak, Igor; Chua, Pei Juan (01.09.2006). "Výpočetní studie lékopisů: β-laktamy". The Journal of Physical Chemistry A. 110 (35): 10521–10524. doi:10.1021 / jp063162b. ISSN 1089-5639. PMID 16942059.
- ^ A b C d E F Patrick, Graham (2017-03-23), „5. Farmaceutika a léčivá chemie“, Organická chemie: velmi krátký úvod, Oxford University Press, s. 71–89, doi:10.1093 / actrade / 9780198759775.003.0005, ISBN 978-0-19-875977-5
- ^ A b C Hu, Feng; Lalancette, Roger; Szostak, Michal (08.03.2016). „Strukturální charakterizace N-alkylovaných zkroucených amidů: důsledky pro amidovou vazebnou rezonanci a štěpení N-C“. Angewandte Chemie International Edition. 55 (16): 5062–5066. doi:10.1002 / anie.201600919. ISSN 1433-7851. PMID 26953809.
| Tento biochemie článek je a pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
