Organoseleniová chemie - Organoselenium chemistry
Organoseleniové sloučeniny (nebo seleno-organické) jsou chemické sloučeniny obsahující uhlík -na-selen chemické vazby. Organoseleniová chemie je odpovídající věda zkoumající jejich vlastnosti a reaktivitu.[1][2][3][4] Selen patří k kyslíku a síře skupina 16 prvků nebo chalkogeny a lze očekávat podobnosti v chemii.
Selen může existovat s oxidační stav −2, +2, +4, +6. Se (II) je dominantní formou v organoseleniové chemii. Dolů ve sloupci skupiny 16 je pevnost vazby je stále slabší (234 kJ /mol pro vazbu C-S a 272 kJ / mol pro vazbu C-S) a délky vazby delší (C-Se 198 pm, C-S 181 pm a C-O 141 pm). Sloučenin selenu je více nukleofilní než odpovídající sloučeniny síry a také kyselější. The strK.A hodnoty XH2 jsou 16 pro kyslík, 7 pro síru a 3,8 pro selen. Na rozdíl od sulfoxidy, odpovídající selenoxidy jsou nestabilní v přítomnosti β-protonů a tato vlastnost je využívána mnoha organické reakce selenu, zejména při oxidacích selenoxidu a při eliminaci selenoxidu. Organoseleniové sloučeniny se nacházejí ve stopových úrovních v okolních vodách, půdách a sedimentech.[5]
První organoseleniová sloučenina, která byla izolována, byla diethyl selenid v roce 1836.[6][7]
Strukturní klasifikace organoseleniových sloučenin

- Selenoly (RSeH) jsou selenové ekvivalenty alkoholy a thioly. Tyto sloučeniny jsou relativně nestabilní a obecně mají nepříjemný zápach. Benzeneselenol (nazývaný také selenaphenol nebo PhSeH) je kyselější (pKA 5,9) než thiofenol (pKA 6.5) a také snadněji oxiduje na diselenid. Selenaphenol se připravuje redukcí difenyldiselenidu.[8]
- Diselenidy (R-Se-Se-R) jsou ekvivalenty selenu peroxidy a disulfidy. Jsou užitečnými skladovatelnými prekurzory reaktivnějších organoseleniových činidel, jako jsou selenoly a selanylhalogenidy. Nejznámější v organické chemii je difenyldiselenid, připravené z fenylmagnesiumbromid a selen následovanou oxidací produktu PhSeMgBr.[9]
- Selanyl halogenidy (R-Se-Cl, R-Se-Br) se připravují halogenací diselenidů. Bromací difenyldiselenidu se získá fenylselanylbromid (PhSeBr). Tyto sloučeniny jsou zdroji „PhSe+".
- Selenides (R − Se − R), také nazývaný selenoethery, jsou selenové ekvivalenty ethery a sulfidy. Jedním z příkladů je dimethylselenid ((CH3)2Se). Jedná se o nejčastější organoseleniové sloučeniny. Symetrické selenidy se obvykle připravují alkylací selenidových solí alkalických kovů, např. selenid sodný. Nesymetrické selenidy se připravují alkylací selenoátů. Tyto sloučeniny obvykle reagují jako nukleofily, např. s alkylhalogenidy (R'-X) dát selenoniové soli R'RRSe+X−. Dvojmocný selen může také interagovat s měkkými heteroatomy za vzniku hypervalentních center selenu.[7] Reagují také za určitých okolností jako elektrofily, např. s organolithium činidla (R'Li) do jedl komplex R'RRSe−Li+.
- Selenoxidy (R-Se (O) -R) jsou ekvivalenty selenu sulfoxidy. Mohou být dále oxidovány na selenony R-Se (O)2R, analogy selenu z sulfony.
- Seo-Selenoperoxoly (RSe-OH; dříve selenenové kyseliny) jsou meziprodukty při oxidaci selenolů. Vyskytují se v některých selenoenzymech, jako jsou glutathionperoxidáza.
- Seleninové kyseliny (RSe (O) OH) jsou analogy sloučeniny sulfinové kyseliny.
- Kyseliny peroxyseleninové (RSe (O) OOH) katalyzují epoxidace reakce a Baeyer-Villigerovy oxidace.
- Selenurany jsou hypervalentní organoseleniové sloučeniny, formálně odvozené od tetrahalogenidů, jako je SeCl4. Příklady jsou typu ArSeCl3.[10] Chloridy se získávají chlorací selenenylchlorid.
- Seleniranes jsou tříčlenné kruhy (rodič: C2H4Se) související s thiiranes ale na rozdíl od thiiranů jsou selenirany kineticky nestabilní a extrudují selen přímo (bez oxidace) za vzniku alkeny. Tato vlastnost byla použita v syntetické organické chemii.[11]
- Selones (R.2C = Se) jsou analogy selenu ketonů. Jsou vzácné kvůli jejich tendenci k oligomerizovat.[12] Diselenobenzochinon je stabilní jako kovový komplex.[13] Selenourea je příklad stabilní sloučeniny obsahující vazbu C = Se.
- Selenothioperoxidy (R-Se-S-R), sloučeniny s vazbami selen-síra, analogické k disulfidy.
Organoseleniové sloučeniny v přírodě
Selen, ve formě organoseleniových sloučenin, je základní mikroživina, jejíž absence ve stravě způsobuje srdeční sval a kostní dysfunkci. Organoseleniové sloučeniny jsou nezbytné pro buněčnou obranu před oxidačním poškozením a pro správné fungování imunitního systému. Mohou také hrát roli v prevenci předčasného stárnutí a rakoviny. Zdrojem Se používaným v biosyntéze je selenofosfát.
Glutathionoxidáza je enzym se selenolem v jeho aktivním místě. Organoseleniové sloučeniny byly nalezeny ve vyšších rostlinách. Například při analýze česneku technikou vysoce účinná kapalinová chromatografie zkombinováno s hmotnostní spektrometrie s indukčně vázanou plazmou (HPLC-ICP-MS), bylo zjištěno, že y-glutamyl-Se-methylselenocystein byl hlavní složkou obsahující Se, spolu s menším množstvím Se-methylselenocystein. Stopová množství dimethyl selenid a allyl methyl selenid se nacházejí v lidském dechu po konzumaci syrového česneku.[14]
Selenocystein a selenomethionin
Selenocystein, nazývaná dvacátá první aminokyselina, je nezbytná pro syntézu proteinů zaměřených na ribozomy v některých organismech.[15] Nyní je známo více než 25 proteinů obsahujících selen (selenoproteiny).[16] Většina enzymů závislých na selenu obsahuje selenocystein, který souvisí s cystein analogicky, ale se selenem nahrazujícím síru. Tento aminokyselina je kódovaný zvláštním způsobem pomocí DNA.
Selenomethionin je aminokyselina obsahující selenid, která se také vyskytuje přirozeně, ale je generována post-transkripční modifikací.
Organoseleniová chemie v organické syntéze
Organoseleniové sloučeniny jsou specializovaná, ale užitečná sbírka činidel užitečných v organické syntéze, ačkoli jsou obecně vyloučeny z procesů užitečných pro farmaceutika kvůli regulačním problémům. Jejich užitečnost závisí na určitých atributech, včetně (i) slabosti vazby C-Se a (ii) snadné oxidace dvojmocných sloučenin selenu.
Vinylové selenidy
Vinylové selenidy jsou organoseleniové sloučeniny, které hrají roli v organické syntéze, zejména při vývoji vhodných látek stereoselektivní cesty k funkcionalizovanému alkeny.[17] Ačkoli jsou zmíněny různé způsoby přípravy vinylových selenidů, užitečnější postup se soustředil na nukleofilní nebo elektrofilní organoselenium přidání do terminálu nebo interní alkyny.[18][19][20][21] Například nukleofilní adice selenofenolu na alkyny poskytuje přednostně Z-vinylové selenidy po delších reakčních dobách při teplotě místnosti. Reakce je rychlejší při vysoké teplotě; avšak směs Z- a E-vinylových selenidů byla získána v poměru téměř 1: 1.[22] Na druhé straně adukty závisí na povaze substituenty na trojná vazba. Naopak vinylové selenidy lze připravit palladium -katalyzovaná hydroselenace alkyny dovolit si Markovnikovův adukt s dobrými výnosy. S metodami přípravy vinylových selenidů ilustrovaných výše jsou spojena některá omezení; popsané postupy používají diorganoyl diselenidy nebo selenofenol jako výchozí materiály, které jsou těkavé a nestabilní a mají nepříjemný zápach. Příprava těchto sloučenin je také složitá.
Oxidace selenoxidu
Oxid seleničitý je užitečné v organická oxidace. Konkrétně SeO2 převede allylický methylenová skupina do odpovídající alkohol. Tuto reakci vyvolává řada dalších činidel.

Ve smyslu mechanismus reakce, SeO2 a allylový substrát reaguje prostřednictvím pericyklický proces začínající na en reakce který aktivuje vazbu C-H. Druhým krokem je [2,3] sigmatropní reakce. Oxidace zahrnující oxid seleničitý se často provádějí s katalytickým množstvím sloučeniny selenu a v přítomnosti a obětní katalyzátor nebo ko-oxidant jako je peroxid vodíku.
Seo2oxidace na bázi někdy poskytují karbonylové sloučeniny, jako je ketony,[23] β-Pinen[24] a cyklohexanon oxidace na 1,2-cyklohexandion.[25] Oxidace ketony mít a-methylenové skupiny poskytuje diketony. Tento typ oxidace oxidem seleničitým se nazývá Rileyova oxidace.[26]
Eliminace selenoxidu
V přítomnosti β-vodíku selenid poskytne eliminační reakce po oxidaci zanechat za sebou alken a a Seo-selenoperoxol. The Seo-selenoperoxol je vysoce reaktivní a není izolován jako takový. V eliminační reakci je všech pět zúčastněných reakčních center koplanární a proto je reakční stereochemie syn. Použitá oxidační činidla jsou peroxid vodíku, ozón nebo MCPBA. Tento typ reakce se často používá u ketony vedoucí k enones. Příkladem je eliminace acetylcyklohexanonu pomocí benzenselenylchlorid a hydrid sodný.[27]
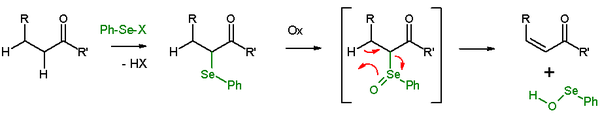
The Grieco eliminace je podobná eliminace selenoxidu pomocí o-nitrofenylselenokyanátu a tributylfosfinu, které způsobují eliminaci prvků H2Ó.
Funkcionalizace olefinů
V posledních dvou desetiletích[když? ] zvláštní pozornost byla věnována funkcionalizaci dvojných vazeb uhlík-uhlík s přídavkem elektrofilních organoseleniových sloučenin. Selanylační reakce je iniciována tvorbou seleniranových iontových meziproduktů z alkenů a selenového elektrofilu RSeX s následným zadním nukleofilním útokem, což vede k antiadičnímu produktu. K útoku nukleofilu dochází na atom uhlíku, který má stabilnější kladný náboj, obvykle nejvíce substituovaný atom uhlíku. Adiční reakce různých selenových elektrofilů s alkeny byly podrobně prozkoumány pomocí interních a externích nukleofilů.[28]
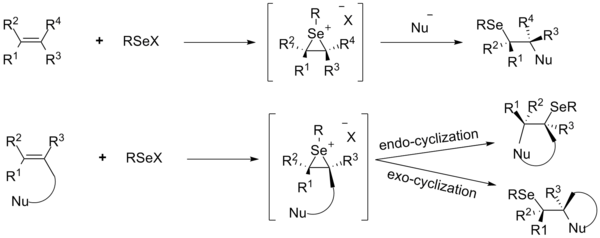
Reference
- ^ A. Krief, L. Hevesi, Organoseleniová chemie I. Transformace funkčních skupin., Springer, Berlín, 1988 ISBN 3-540-18629-8
- ^ S. Patai, Z. Rappoport (ed.), The Chemistry of Organic Selenium and Tellurium Compounds, John. Wiley and Sons, Chichester, sv. 1, 1986 ISBN 0-471-90425-2
- ^ Paulmier, C. Selenová činidla a meziprodukty v organické syntéze; Baldwin, J. E., Ed .; Pergamon Books Ltd .: New York, 1986 ISBN 0-08-032484-3
- ^ Freudendahl, Diana M .; Santoro, Stefano; Shahzad, Sohail A .; Santi, Claudio; Wirth, Thomas (2009). „Green Chemistry with Selenium Reagents: Development of Efficient Catalytic Reactions“. Angewandte Chemie International Edition. 48 (45): 8409–11. doi:10.1002 / anie.200903893. PMID 19802863.
- ^ Wallschläger, D .; Feldmann, F. (2010). Vznik, výskyt, význam a analýza organoseleniových a organoteluriových sloučenin v životním prostředí. Kovové ionty v biologických vědách. 7, Organometallics in Environment and Toxicology. Publikování RSC. 319–364. ISBN 978-1-84755-177-1.
- ^ Löwig, C. J. (1836). „Ueber schwefelwasserstoff — und selenwasserstoffäther“ [O sirovodíku a selenium vodíku etheru]. Annalen der Physik. 37: 550–553.
- ^ A b Mukherjee, Anna J .; Zade, Sanjio S .; Singh, Harkesh B .; Sunoj, Raghavan B. (2010). „Organoselenium Chemistry: Role of Intramolecular Interactions“. Chemické recenze. 110 (7): 4357–4416. doi:10.1021 / cr900352j. PMID 20384363.
- ^ Organické syntézy, Sb. Sv. 3, s. 771 (1955); Sv. 24, s. 89 (1944) Článek online.
- ^ Organické syntézy, Sb. Sv. 6, s. 533 (1988); Sv. 59, s. 141 (1979) Článek
- ^ Chemie hypervalentních sloučenin (1999) Kin-ya Akiba ISBN 978-0-471-24019-8
- ^ Odkaz Vývoj v chemii selenaheterocyklických sloučenin praktického významu v syntéze a léčivé biologii Arkivoc 2006 (JE-1901MR) Jacek Młochowski, Krystian Kloc, Rafał Lisiak, Piotr Potaczek a Halina Wójtowicz
- ^ Okazaki, R .; Tokitoh, N. (2000). „Těžké ketony, kongenery těžších prvků ketonu“. Účty chemického výzkumu. 33 (9): 625–630. doi:10.1021 / ar980073b. PMID 10995200.
- ^ Amouri, H .; Moussa, J .; Renfrew, A. K .; Dyson, P. J .; Rager, M. N .; Chamoreau, L.-M. (2010). „Objev, struktura a protinádorová aktivita iridiového komplexu diselenobenzochinonu“. Angewandte Chemie International Edition. 49 (41): 7530–7533. doi:10,1002 / anie.201002532. PMID 20602399.
- ^ Block, E. (2010). Česnek a další Allium: The Lore a věda. Royal Society of Chemistry. ISBN 978-0-85404-190-9.
- ^ Axley, M.J .; Böck, A .; Stadtman, T.C. (1991). "Katalytické vlastnosti Escherichia coli mutant formiátdehydrogenázy, ve kterém síra nahrazuje selen "". Proc. Natl. Acad. Sci. USA. 88 (19): 8450–8454. Bibcode:1991PNAS ... 88.8450A. doi:10.1073 / pnas.88.19.8450. PMC 52526. PMID 1924303.
- ^ Papp, L.V .; Lu, J .; Holmgren, A .; Khanna, K.K. (2007). „Od selenu po selenoproteiny: syntéza, identita a jejich role v lidském zdraví“. Antioxidanty a redoxní signalizace. 9 (7): 775–806. doi:10.1089 / ars.2007.1528. PMID 17508906.
- ^ Comasseto, João Valdir; Ling, Lo Wai; Petragnani, Nicola; Stefani, Helio Alexandre (1997). "Vinylické selenidy a teluridy - příprava, reaktivita a syntetické aplikace". Syntéza. 1997 (4): 373. doi:10.1055 / s-1997-1210.
- ^ Comasseto, J (1983). "Vinylové selenidy". Journal of Organometallic Chemistry. 253 (2): 131–181. doi:10.1016 / 0022-328X (83) 80118-1.
- ^ Zeni, Gilson; Stracke, Marcelo P .; Nogueira, Cristina W .; Braga, Antonio L .; Menezes, Paulo H .; Stefani, Helio A. (2004). "Hydroselenation of Alkynes by Lithium Butylselenolate: an Approach in the Synthesis of Vinylic Selenides". Organické dopisy. 6 (7): 1135–8. doi:10.1021 / ol0498904. PMID 15040741.
- ^ Dabdoub, M (2001). "Syntéza (Z) -1-fenylseleno-1,4-diorganyl-1-buten-3-inů: hydroselenace symetrických a nesymetrických 1,4-diorganyl-1,3-butadiynů". Čtyřstěn. 57 (20): 4271–4276. doi:10.1016 / S0040-4020 (01) 00337-4.
- ^ Doregobarros, O; Lang, E; Deoliveira, C; Peppe, C; Zeni, G (2002). „Indium (I) jodidem zprostředkovaná chemio-, regio- a stereoselektivní hydroselenace 2-alkyn-1-ol derivátů“. Čtyřstěn dopisy. 43 (44): 7921. doi:10.1016 / S0040-4039 (02) 01904-4.
- ^ Comasseto, J (1981). "Stereoselektivní syntéza vinylových selenidů". Journal of Organometallic Chemistry. 216 (3): 287–294. doi:10.1016 / S0022-328X (00) 85812-X.
- ^ Organické syntézy Sb. Sv. 9, s. 396 (1998); Sv. 71, s. 181 (1993) Online článek Archivováno 2005-10-24 na Wayback Machine
- ^ Organické syntézy Sb. Sv. 6, s. 946 (1988); Sv. 56, str. 25 (1977). Online článek Archivováno 2005-11-01 na Wayback Machine
- ^ Organické syntézy, Sb. Sv. 4, s. 229 (1963); Sv. 32, s. 35 (1952). Online článek Archivováno 2005-11-27 na Wayback Machine
- ^ Riley, Harry Lister; Morley, John Frederick; Přítel, Norman Alfred Child (1932). "255. Oxid seleničitý, nové oxidační činidlo. Část I. Jeho reakce s aldehydy a ketony". Journal of the Chemical Society (obnoveno): 1875. doi:10.1039 / JR9320001875.
- ^ Organické syntézy Sb. Sv. 6, s. 23 (1988); Sv. 59, s. 58 (1979) Článek online
- ^ Organoselenium Chemistry: Syntéza a reakce - Wiley Online Library. 2011. doi:10.1002/9783527641949. ISBN 9783527641949.
