Allylalkohol - Allyl alcohol
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Prop-2-en-1-ol | |
| Ostatní jména | |
| Identifikátory | |
3D model (JSmol ) | |
| 3DMet | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.003.156 |
| Číslo ES |
|
| KEGG | |
PubChem CID | |
| Číslo RTECS |
|
| UNII | |
| UN číslo | 1098 |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C3H6Ó | |
| Molární hmotnost | 58.080 g · mol−1 |
| Vzhled | bezbarvá kapalina[1] |
| Zápach | hořčičná[1] |
| Hustota | 0,854 g / ml |
| Bod tání | -129 ° C |
| Bod varu | 97 ° C (207 ° F; 370 K) |
| Mísitelný | |
| Tlak páry | 17 mmHg[1] |
| Kyselost (strK.A) | 15,5 (H2Ó)[2] |
| -36.70·10−6 cm3/ mol | |
| Nebezpečí | |
| Bezpečnostní list | Externí bezpečnostní list |
| Piktogramy GHS |     |
| Signální slovo GHS | Nebezpečí |
| H225, H301, H311, H315, H319, H331, H335, H400 | |
| P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P273, P280, P301 + 310, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P311, P312, P321, P322, P330, P332 + 313, P337 + 313, P361 | |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | 21 ° C (70 ° F; 294 K) |
| 378 ° C (712 ° F; 651 K) | |
| Výbušné limity | 2.5–18.0% |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
LC50 (střední koncentrace ) | 1000 ppm (savec, 1 hod) 76 ppm (krysa, 8 hodin) 207 ppm (myš, 2 hodiny) 1000 ppm (králík, 3,5 hodiny) 1 000 ppm (opice, 4 hodiny) 1060 ppm (krysa, 1 hod) 165 ppm (krysa, 4 hodiny) 76 ppm (krysa, 8 hodin)[3] |
| NIOSH (Limity expozice USA pro zdraví): | |
PEL (Dovolený) | 2 ppm[1] |
REL (Doporučeno) | TWA 2 ppm (5 mg / m3) ST 4 ppm (10 mg / m.)3) [kůže] [1] |
IDLH (Okamžité nebezpečí) | 20 ppm[1] |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
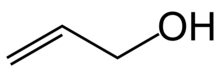
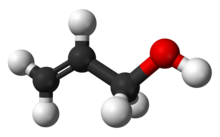
Allylalkohol (IUPAC název: prop-2-en-l-ol) je organická sloučenina s strukturní vzorec CH2= CHCH2ACH. Jako mnozí alkoholy, je to ve vodě rozpustná bezbarvá kapalina. Je toxičtější než typické malé alkoholy. Allylalkohol se používá jako surovina pro výrobu glycerolu, ale také se používá jako předzvěst mnoha specializovaných sloučenin, jako jsou nehořlavé materiály, sušící oleje, a změkčovadla.[4] Allylalkohol je nejmenším zástupcem allylický alkoholy.
Výroba
Allylalkohol lze získat mnoha způsoby. Poprvé byl připraven v roce 1856 Auguste Cahours a August Hofmann podle hydrolýza z allyljodid.[4] Allylalkohol dnes komerčně vyrábí Olin a Shell korporace hydrolýzou allylchlorid:
- CH2= CHCH2Cl + NaOH → CH2= CHCH2OH + NaCl
Allylalkohol lze také vyrobit přesmykem propylenoxid, reakce, která je katalyzována kamenec draselný při vysoké teplotě. Výhodou této metody ve srovnání s cestou allylchloridu je, že negeneruje sůl. Vyhýbat se také meziproduktům obsahujícím chloridy je "acetoxylace" sloučeniny propylen na allylacetát:
- CH2= CHCH3 + 1/2 O.2 + CH3COOH → CH2= CHCH2OCOCH3 + H2Ó
Hydrolýzou tohoto acetátu se získá allylalkohol. Alternativním způsobem propylen lze oxidovat na akrolein, který na hydrogenace dává alkohol.
Jiné metody
Allylalkohol lze v zásadě získat dehydrogenace z propanol. V laboratoři byl připraven reakcí glycerol s šťavelová nebo kyseliny mravenčí.[5][6] Allylalkoholy obecně lze připravit allylová oxidace z allyl sloučeniny podle oxid seleničitý.
Aplikace
Allylalkohol se převádí hlavně na glycidol, což je chemický meziprodukt při syntéze glycerol glycidylethery, estery a aminy. Z allylalkoholu se také připravuje řada polymerovatelných esterů, např. dialyl ftalát.[4]
Bezpečnost
Allylalkohol je toxičtější než příbuzné alkoholy. Jeho prahová mezní hodnota (TLV) je 2 ppm. Je to slzotvorce.[4]
Je klasifikován jako extrémně nebezpečná látka ve Spojených státech, jak je definováno v oddíle 302 USA Nouzové plánování a zákon o právu na znalost komunity (42 U.S.C. 11002) a podléhá přísným požadavkům na hlášení ze strany zařízení, která je vyrábějí, skladují nebo používají ve významných množstvích.[7]
Viz také
Reference
- ^ A b C d E F G h NIOSH Kapesní průvodce chemickými nebezpečími. "#0017". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (97. vydání). CRC Press. str. 5–88. ISBN 978-1498754286.
- ^ „Allylalkohol“. Koncentrace bezprostředně nebezpečné pro život a zdraví (IDLH). Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ A b C d Ludger Krähling; Jürgen Krey; Gerald Jakobson; Johann Grolig; Leopold Miksche (2002). "Allylové sloučeniny". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a01_425.
- ^ Oliver Kamm; C. S. Marvel (1941). „Allylalkohol“. Organické syntézy.; Kolektivní objem, 1, str. 42
- ^ Cohen, Julius (1900). Praktická organická chemie (2. vyd.). London: Macmillan and Co., Limited. str.96.
Praktická organická chemie Cohen Julius.
- ^ „40 C.F.R .: Dodatek A k části 355 - Seznam extrémně nebezpečných látek a jejich mezní hodnoty pro plánování“ (PDF) (1. července 2008 ed.). Vládní tiskárna. Archivovány od originál (PDF) 25. února 2012. Citováno 29. října 2011. Citovat deník vyžaduje
| deník =(Pomoc)
externí odkazy
- Mezinárodní karta chemické bezpečnosti 0095
- NIOSH Kapesní průvodce chemickými nebezpečími. "#0017". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- Národní institut pro kontrolu et sécurité (2004). "Alcool allylique. " Informační list č. 156. Paříž: INRS. (francouzsky)
- Veřejné informace o allylalkoholu ve státě Michigan
- Pokyny pro expozici na pracovišti

