Molekulární symetrie - Molecular symmetry
Molekulární symetrie v chemie popisuje symetrie předložit molekuly a klasifikace molekul podle jejich symetrie. Molekulární symetrie je základním pojmem v chemii, protože ji lze použít k předpovědi nebo vysvětlení mnoha molekulárních chemické vlastnosti, jako je jeho dipólový moment a je povoleno spektroskopické přechody K tomu je nutné klasifikovat stavy molekuly pomocí neredukovatelné reprezentace z tabulka znaků skupiny symetrie molekuly. Mnoho učebnic na univerzitní úrovni fyzikální chemie, kvantová chemie, spektroskopie a anorganická chemie věnujte kapitolu symetrii.[1][2][3][4][5][6]
Rámec pro studium molekulární symetrie poskytuje teorie skupin, a zejména neredukovatelné zastoupení teorie. Symetrie je užitečná při studiu molekulární orbitaly, s aplikacemi, jako je Hückel metoda, teorie pole ligandů a Vládne Woodward-Hoffmann. Dalším rámcem ve větším měřítku je použití krystalové systémy popsat krystalografické symetrie sypkých materiálů.
Existuje mnoho technik pro praktické hodnocení molekulární symetrie, včetně Rentgenová krystalografie a různé formy spektroskopie. Spektroskopická notace je založen na úvahách o symetrii.
Pojmy symetrie
Studium symetrie v molekulách využívá teorie skupin.
| Rotační osa (Cn) | Nesprávné rotační prvky (Sn) | ||
|---|---|---|---|
| Chirál Ne Sn | Achirál zrcadlové letadlo S1 = σ | Achirál inverzní centrum S2 = i | |
| C1 | 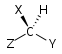 |  |  |
| C2 |  | 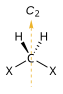 |  |
Elementy
Symetrii bodové skupiny molekuly lze popsat 5 typy prvek symetrie.
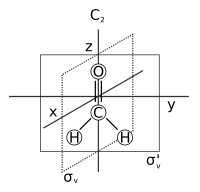
- Osa symetrie: osa, kolem které a otáčení podle vede k nerozeznání molekuly od originálu. Toto se také nazývá n-složit osa otáčení a zkráceně Cn. Příkladem je C.2 osa dovnitř voda a C.3 osa dovnitř amoniak. Molekula může mít více než jednu osu symetrie; ten s nejvyšším n se nazývá hlavní osa, a podle konvence je zarovnán s osou z v a Kartézský souřadnicový systém.
- Rovina symetrie: rovina odrazu, skrz kterou je generována identická kopie původní molekuly. Toto se také nazývá a zrcadlové letadlo a zkráceně σ (sigma = řecké „s“ z německého zrcadla „Spiegel“).[7] Voda má dvě z nich: jednu v rovině samotné molekuly a jednu kolmý k tomu. Rovina symetrie paralelní s hlavní osou je dabován vertikální (σproti) a jeden na něj kolmý horizontální (σh). Existuje třetí typ roviny symetrie: Pokud vertikální rovina symetrie navíc půlí úhel mezi dvěma 2násobnými osami otáčení kolmými na hlavní osu, rovina se dabuje vzepětí (σd). Rovinu symetrie lze také identifikovat podle kartézské orientace, např. (Xz) nebo (yz).
- Střed symetrie nebo inverzní centrum, zkráceně i. Molekula má střed symetrie, když pro jakýkoli atom v molekule existuje stejný atom diametrálně naproti tomuto středu ve stejné vzdálenosti od něj. Jinými slovy, molekula má střed symetrie, když body (x, y, z) a (−x, −y, −z) odpovídají stejným objektům. Například pokud je v nějakém bodě atom kyslíku (x, y, z), pak je v bodě atom kyslíku (−x, −y, −z). Atom ve středu inverze může nebo nemusí být. Příklady jsou xenon tetrafluorid kde inverzní centrum je na atomu Xe, a benzen (C6H6) kde střed inverze je ve středu prstence.
- Osa rotace a odrazu: osa, kolem které se otáčí , následovaný odrazem v rovině kolmé na ni, ponechává molekulu beze změny. Také se nazývá n-složit nesprávná osa otáčení, to je zkráceno Sn. Příklady jsou přítomny v čtyřboké tetrafluorid křemičitý, se třemi S.4 osy a rozložená konformace z etan s jedním S.6 osa. S1 osa odpovídá rovině zrcadla σ a S.2 osa je inverzní střed i. Molekula, která nemá žádný Sn osa pro libovolnou hodnotu n je a chirální molekula.
- Identita, zkráceně E, z německého „Einheit“, což znamená jednota.[8] Tento prvek symetrie jednoduše sestává ze žádné změny: každá molekula má tento prvek. I když se tento prvek zdá fyzicky triviální, musí být zahrnut do seznamu prvků symetrie, aby tvořily matematický skupina, jehož definice vyžaduje zahrnutí prvku identity. Říká se tomu, protože je to analogické k násobení jednou (jednota). Jinými slovy, E je vlastnost, kterou musí mít jakýkoli objekt bez ohledu na jeho vlastnosti symetrie.[9]
Operace
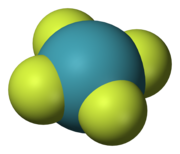
Těchto pět prvků symetrie k nim přidružilo pět typů operace symetrie, které ponechávají molekulu ve stavu nerozeznatelném od počátečního stavu. Někdy se odlišují od prvků symetrie znakem a stříška nebo háček. Tak, Ĉn je rotace molekuly kolem osy a Ê je operace identity. K prvku symetrie může být přidružena více než jedna operace symetrie. Například C4 osa náměstí xenon tetrafluorid (XeF4) molekula je spojena se dvěma Ĉ4 rotace (90 °) v opačných směrech a a Ĉ2 otáčení (180 °). Od Ĉ1 je ekvivalentní Ê, Ŝ1 na σ a Ŝ2 na „, všechny operace symetrie lze klasifikovat jako správné nebo nesprávné rotace.
U lineárních molekul je rotace ve směru hodinových ručiček nebo proti směru hodinových ručiček kolem osy molekuly o libovolný úhel Φ operací symetrie.
Skupiny symetrie
Skupiny
Operace symetrie molekuly (nebo jiného objektu) tvoří a skupina. V matematice je skupina množina s binární operace který splňuje čtyři vlastnosti uvedené níže.
V skupina symetrie, prvky skupiny jsou operace symetrie (nikoli prvky symetrie) a binární kombinace spočívá v použití první operace symetrie a potom druhé. Příkladem je posloupnost C.4 rotace kolem osy z a odraz v rovině xy, označený σ (xy) C4. Podle konvence je pořadí operací zprava doleva.
Skupina symetrie se řídí určujícími vlastnostmi jakékoli skupiny.
(1) uzavření vlastnictví:
Pro každou dvojici prvků X a y v G, produkt X*y je také v G.
(v symbolech, pro každé dva prvky X, y∈G, X*y je také v G ).
To znamená, že skupina je Zavřeno takže kombinace dvou prvků neprodukuje žádné nové prvky. Operace symetrie mají tuto vlastnost, protože posloupnost dvou operací vyprodukuje třetí stav nerozeznatelný od druhého a tedy od prvního, takže čistý účinek na molekulu je stále operace symetrie.
(2) asociativní vlastnictví:
Pro každého X a y a z v G, oba (X*y)*z a X*(y*z) výsledek se stejným prvkem v G.
(v symbolech, (X*y)*z = X*(y*z ) pro každého X, y, a z ∈ G)
(3) existence identity vlastnictví:
Musí existovat prvek (řekněme E ) v G takový produkt jakýkoli prvek G s E neprovádět žádnou změnu prvku.
(v symbolech, X*E=E*X= X pro každého X∈ G )
(4) existence inverze vlastnictví:
Pro každý prvek ( X ) v G, musí existovat prvek y v G takový produkt z X a y je prvek identity E.
(v symbolech, pro každého X∈G tady je y ∈ G takhle X*y=y*X= E pro každého X∈G )
The objednat skupiny je počet prvků ve skupině. U skupin malých objednávek lze vlastnosti skupiny snadno ověřit zvážením její tabulky složení, tabulky, jejíž řádky a sloupce odpovídají prvkům skupiny a jejichž položky odpovídají jejich produktům.
Skupiny bodů a skupiny permutace-inverze

Postupná aplikace (nebo složení) jedné nebo více operací symetrie molekuly má účinek ekvivalentní účinku jedné operace symetrie molekuly. Například C2 rotace následovaná σproti odraz je považován za σproti'operace symetrie: σproti*C2 = σproti'. („Operace A následovaná B do formy C“ se píše BA = C).[9] Kromě toho se sada všech operací symetrie (včetně této operace kompozice) řídí všemi vlastnostmi skupiny uvedenými výše. Tak (S,*) je skupina, kde S je množina všech operací symetrie určité molekuly a * označuje složení (opakovanou aplikaci) operací symetrie.
Tato skupina se nazývá bodová skupina této molekuly, protože množina operací symetrie ponechává alespoň jeden bod pevný (i když u některých symetrií zůstává pevná celá osa nebo celá rovina). Jinými slovy, skupina bodů je skupina, která shrnuje všechny operace symetrie, které mají všechny molekuly v dané kategorii.[9] Symetrii krystalu naopak popisuje a vesmírná skupina operací symetrie, která zahrnuje překlady ve vesmíru.
Jeden může určit operace symetrie skupiny bodů pro konkrétní molekulu zvážením geometrické symetrie jejího molekulárního modelu. Když však použijeme skupinu bodů ke klasifikaci molekulárních stavů, operace v ní nelze interpretovat stejným způsobem. Místo toho jsou operace interpretovány jako otáčení a / nebo odrážení vibronických (vibrační-elektronických) souřadnic[10] a tyto operace dojíždějí s vibronickým Hamiltonianem. Jsou to „operace symetrie“ pro tento vibronický hamiltonián. Skupina bodů se používá k klasifikaci symetrických vibronických vlastních stavů. Klasifikace symetrie rotačních úrovní, vlastních stavů plného (rotačně-vibrační-elektronického) hamiltoniánu, vyžaduje použití vhodné permutační-inverzní skupiny, jak je zavedeno Longuet-Higgins.[11]
Příklady skupin bodů
Přiřazením každé molekuly bodová skupina klasifikuje molekuly do kategorií s podobnými vlastnostmi symetrie. Například PCl3, POF3, XeO3a NH3 všechny sdílejí stejné operace symetrie.[12] Všichni mohou podstoupit operaci identity E, dvě různé C3 rotační operace a tři různé σproti rovinné odrazy beze změny jejich identity, takže jsou umístěny do jedné bodové skupiny, C3v, s objednávkou 6.[13] Podobně voda (H2O) a sirovodík (H2S) také sdílejí stejné operace symetrie. Oba podstoupí operaci identity E, jednu C.2 rotace a dvě σproti odrazy beze změny jejich identity, takže jsou oba umístěny do jedné bodové skupiny, C2v, s objednávkou 4.[14] Tento klasifikační systém pomáhá vědcům efektivněji studovat molekuly, protože chemicky příbuzné molekuly ve stejné bodové skupině mají tendenci vykazovat podobná vazebná schémata, diagramy molekulárních vazeb a spektroskopické vlastnosti.[9]
Společné skupiny bodů
Následující tabulka obsahuje seznam skupin bodů označených pomocí Schoenflies notace, což je běžné v chemii a molekulární spektroskopii. Popis struktury zahrnuje běžné tvary molekul, které lze vysvětlit pomocí Model VSEPR.
| Skupina bodů | Operace symetrie[15] | Jednoduchý popis typické geometrie | Příklad 1 | Příklad 2 | Příklad 3 |
| C1 | E | žádná symetrie, chirál | 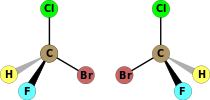 bromchlorfluormethan (oba enantiomery zobrazeno) | 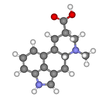 kyselina lysergová | 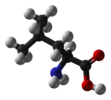 L-leucin a většina ostatních α-aminokyseliny až na glycin |
| Cs | E σh | zrcadlová rovina, žádná jiná symetrie | 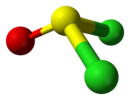 thionylchlorid |  kyselina chlorná | 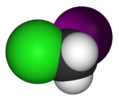 chlorjodmethan |
| Ci | E i | inverzní centrum | 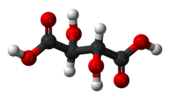 mezo-kyselina vinná | 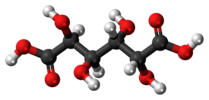 kyselina jablečná (mezo- kyselina galaktarová) | (S,R) 1,2-dibrom-1,2-dichlorethan (proti přizpůsobovatel) |
| C.V | E 2C∞Φ ∞σproti | lineární |  fluorovodík (a všechny ostatní heteronukleární rozsivkové molekuly ) |  oxid dusičitý (oxid dusný) |  kyselina kyanovodíková (kyanovodík) |
| D.H | E 2C∞Φ ∞σi i 2S∞Φ ∞C2 | lineární s inverzním středem |  kyslík (a všechny ostatní homonukleární rozsivkové molekuly ) | 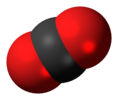 oxid uhličitý |  acetylén (ethyn) |
| C2 | E C.2 | „geometrie otevřené knihy,“ chirál |  peroxid vodíku |  hydrazin | 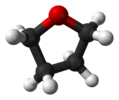 tetrahydrofuran (kroucená konformace) |
| C3 | E C.3 | vrtule, chirální |  trifenylfosfin |  triethylamin |  kyselina fosforečná |
| C2h | E C.2 i σh | rovinný s inverzním středem, bez svislé roviny |  trans -1,2-dichlorethylen | 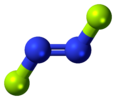 trans -dinitrogen difluorid |  trans -azobenzen |
| C3h | E C.3 C32 σh S3 S35 | vrtule |  kyselina boritá |  phloroglucinol (1,3,5-trihydroxybenzen) | |
| C2v | E C.2 σproti(xz) σproti„(yz) | úhlové (H2O) nebo houpačka (SF4) nebo tvar T (ClF3) |  voda |  tetrafluorid síry |  chlorfluorid |
| C3v | E 2C3 3σproti | trigonální pyramidální |  neinvertující amoniak |  oxychlorid fosforitý |  kobalt-tetrakarbonylhydrid, HCo (CO)4 |
| C4v | E 2C4 C2 2σproti 2σd | čtvercový pyramidální |  xenon oxytetrafluorid | 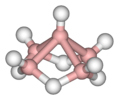 pentaboran (9), B5H9 | 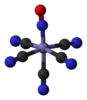 nitroprusidový anion [Fe (CN)5(NE)]2− |
| C5v | E 2C5 2C52 5σproti | komplex „dojicí stolice“ | 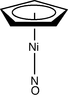 Ni (C.5H5)(NE) |  korrannulen | |
| D2 | E C.2(x) C.2(y) C.2(z) | kroucení, chirál | 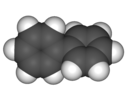 bifenyl (zkosená konformace) |  twistane (C10H16) | cyklohexanová kroucená konformace |
| D3 | E C.3(z) 3C2 | trojitá šroubovice, chirál |  Tris (ethylendiamin) kationt kobaltu (III) | 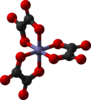 aniont tris (oxalato) železa (III) | |
| D2h | E C.2(z) C.2(y) C.2(X) i σ (xy) σ (xz) σ (yz) | rovinný s inverzním středem, svislou rovinou |  ethylen | 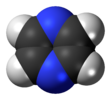 pyrazin | 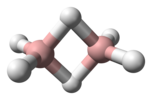 diboran |
| D3h | E 2C3 3C2 σh 2S3 3σproti | trigonální planární nebo trigonální bipyramidální |  fluorid boritý |  chlorid fosforečný | 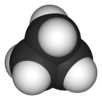 cyklopropan |
| D4h | E 2C4 C2 2C2„2C2" i 2S4 σh 2σproti 2σd | čtvercový rovinný |  xenon tetrafluorid |  anion oktachlorodimolybdenanu (II) | 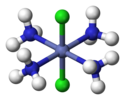 Trans- [CoIII(NH3)4Cl2]+ (kromě atomů vodíku) |
| D5h | E 2C5 2C52 5C2 σh 2S5 2S53 5σproti | pětiúhelníkový |  cyklopentadienylový anion | 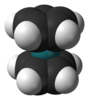 ruthenocene |  C70 |
| D6h | E 2C6 2C3 C2 3C2„3C2‘’ i 2S3 2S6 σh 3σd 3σproti | šestihranný | 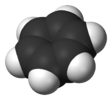 benzen |  bis (benzen) chrom |  koronen (C24H12) |
| D7h | E C.7 S7 7C2 σh 7σproti | sedmiúhelníkový |  tropylium (C7H7+) kation | ||
| D8h | E C.8 C4 C2 S8 i 8C2 σh 4σproti 4σd | osmiúhelníkový |  cyklooktatetraenid (C8H82−) anion |  uranocen | |
| D2d | E 2S4 C2 2C2„2σd | 90 ° otočení | 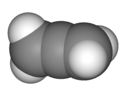 Allene |  tetranitrid tetrasulfur |  diboran (4) (vzrušený stav) |
| D3d | E 2C3 3C2 i 2S6 3σd | 60 ° kroucení |  etan (potácel se rotamer ) | 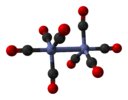 dikobalt oktakarbonyl (nepřemostěno izomer ) | 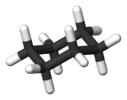 cyklohexanová konformace křesla |
| D4d | E 2S8 2C4 2S83 C2 4C2„4σd | 45 ° otočení |  síra (korunová konformace S8) |  dimangan dekakarbonyl (střídavý rotamer) | 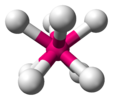 oktafluoroxenátový ion (idealizovaná geometrie) |
| D5 d | E 2C5 2C52 5C2 i 2S103 2S10 5σd | 36 ° kroucení |  ferrocen (střídavý rotamer) | ||
| S4 | E 2S4 C2 |  tetraphenylborate anion | |||
| Td | E 8C3 3C2 6S4 6σd | čtyřboká |  metan |  oxid fosforečný | 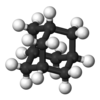 adamantan |
| Th | E 4C3 4C32 i 3C2 4S6 4S65 3σh | pyritohedron | |||
| Óh | E 8C3 6C2 6C4 3C2 i 6S4 8S6 3σh 6σd | osmistěn nebo krychlový |  fluorid sírový | 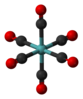 hexakarbonyl molybdenu |  kubánský |
| Jáh | E 12C5 12C52 20C3 15C2 i 12S10 12S103 20S6 15σ | icosahedral nebo dodekahedrál |  Buckminsterfullerene |  dodecaborate anion | 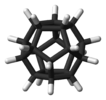 dodekahedran |
Zastoupení
Operace symetrie mohou být zastoupena mnoha způsoby. Pohodlné znázornění je matice. Pro libovolný vektor představující bod v kartézských souřadnicích vynásobením doleva získá nové umístění bodu transformovaného operací symetrie. Složení operací odpovídá násobení matic. V rámci skupiny bodů vede násobení matic dvou operací symetrie k matici jiné operace symetrie ve stejné skupině bodů.[9] Například v C2v příklad toto je:
Ačkoli existuje nekonečné množství takových reprezentací, neredukovatelné reprezentace (nebo "irreps") skupiny se běžně používají, protože všechny ostatní reprezentace skupiny lze popsat jako lineární kombinaci neredukovatelných reprezentací.
Tabulky znaků
Pro každou skupinu bodů a tabulka znaků shrnuje informace o operacích symetrie a o svých neredukovatelných reprezentacích. Protože vždy existuje stejný počet neredukovatelných reprezentací a tříd operací symetrie, jsou tabulky čtvercové.
Samotná tabulka se skládá z postavy které představují, jak se konkrétní neredukovatelná reprezentace transformuje, když se použije konkrétní operace symetrie. Jakákoli operace symetrie ve skupině bodů molekuly působící na samotnou molekulu ji ponechá beze změny. Ale za jednání na obecném subjektu, jako je a vektor nebo orbitální, nemusí tomu tak být. Vektor mohl změnit znaménko nebo směr a orbitál mohl změnit typ. Pro jednoduché skupiny bodů jsou hodnoty buď 1 nebo −1: 1 znamená, že znaménko nebo fáze (vektoru nebo orbity) se operací symetrie nezmění (symetrický) a −1 označuje změnu znaménka (asymetrický).
Reprezentace jsou označeny podle sady konvencí:
- A, když je rotace kolem hlavní osy symetrická
- B, když rotace kolem hlavní osy je asymetrická
- E a T jsou dvojnásobně a trojnásobně zdegenerované reprezentace
- když má skupina bodů střed inverze, dolní index g (Němec: gerade nebo dokonce) signalizuje žádnou změnu znaménka a dolní index u (ungerade nebo nerovnoměrné) změna znaménka s ohledem na inverzi.
- se skupinami bodů C.V a D..H symboly jsou vypůjčené moment hybnosti popis: Σ, Π, Δ.
Tabulky také zachycují informace o tom, jak se kartézské bazické vektory, rotace kolem nich a jejich kvadratické funkce transformují operacemi symetrie skupiny, a upozorňují na to, která neredukovatelná reprezentace se transformuje stejným způsobem. Tyto údaje jsou obvykle na pravé straně tabulek. Tato informace je užitečná, protože chemicky důležité orbitaly (zejména str a d orbitaly) mají stejnou symetrii jako tyto entity.
Tabulka znaků pro C.2v skupina bodů symetrie je uvedena níže:
| C2v | E | C2 | σproti(xz) | σproti„(yz) | ||
|---|---|---|---|---|---|---|
| A1 | 1 | 1 | 1 | 1 | z | X2, y2, z2 |
| A2 | 1 | 1 | −1 | −1 | Rz | xy |
| B1 | 1 | −1 | 1 | −1 | X, R.y | xz |
| B2 | 1 | −1 | −1 | 1 | y, R.X | yz |
Zvažte příklad vody (H2O), který má C.2v symetrie popsaná výše. 2strX orbitální kyslíku má B1 symetrie jako ve čtvrtém řádku tabulky znaků výše, s x v šestém sloupci). Je orientován kolmo na rovinu molekuly a přepíná znaménko s C2 a σproti'(yz) operace, ale zůstane nezměněna s dalšími dvěma operacemi (znak operace operace identity je samozřejmě vždy +1). Znaková sada tohoto orbitálu je tedy {1, −1, 1, −1}, což odpovídá B1 neredukovatelné zastoupení. Stejně tak 2strz orbital je viděn mít symetrii A1 neredukovatelné zastoupení (tj.: žádná ze operací symetrie to nezmění), 2stry B2a 3dxy orbitální A2. Tyto úkoly a další jsou uvedeny ve dvou sloupcích tabulky úplně vpravo.
Historické pozadí
Hans Bethe použil znaky operací bodových skupin ve své studii o teorie pole ligandů v roce 1929 a Eugene Wigner používal teorii skupin k vysvětlení pravidel výběru atomová spektroskopie.[16] První tabulky znaků byly sestaveny uživatelem László Tisza (1933), v souvislosti s vibračními spektry. Robert Mulliken jako první publikoval tabulky znaků v angličtině (1933) a E. Bright Wilson použil je v roce 1934 k předpovědi symetrie vibrací normální režimy.[17] Kompletní soubor 32 krystalografických skupin bodů publikovali v roce 1936 Rosenthal a Murphy.[18]
Molekulární nerigidita
Jak je uvedeno výše v části Skupiny bodů a skupiny permutace-inverze, bodové skupiny jsou užitečné pro klasifikaci vibronických stavů tuhý molekuly (někdy nazývané polotuhý molekuly), které procházejí jen malými oscilacemi kolem jedné rovnovážné geometrie. Longuet-Higgins zavedla obecnější typ skupiny symetrie vhodný nejen pro klasifikaci rovibronických stavů tuhých molekul, ale také pro klasifikaci stavů netuhý (nebo fluxional) molekuly, které tunelují mezi ekvivalentními geometrií (tzv verze[19]) a který může také umožnit rušivé účinky molekulární rotace.[11] Tyto skupiny jsou známé jako permutace-inverze skupiny, protože operace symetrie v nich jsou energeticky proveditelné permutace identických jader nebo inverze vzhledem k těžišti ( parita operace) nebo jejich kombinace.
Například, etan (C2H6) má tři ekvivalenty střídavé konformace. K tunelování mezi konformacemi dochází při běžné teplotě do vnitřní rotace jedné methylové skupiny ve vztahu k druhému. To není rotace celé molekuly kolem C.3 osa. Ačkoli každá konformace má D3d symetrie, jak je uvedeno v tabulce výše, popis vnitřní rotace a souvisejících kvantových stavů a energetických úrovní vyžaduje úplnější skupinu permutace-inverze G36.
Podobně, amoniak (NH3) má dva ekvivalentní pyramidové (C3v) konformace, které jsou interkonvertovány procesem známým jako inverze dusíku. Toto není operace inverze skupiny bodů i používá se pro centrosymmetrické tuhé molekuly (tj. inverze vibračních posunů a elektronických souřadnic v jaderném těžišti hmoty) od NH3 nemá žádné centrum inverze a není centrosymmetrické. Spíše jde o inverzi jaderných a elektronických souřadnic v molekulárním těžišti (někdy nazývanou paritní operace), která je pro tuto molekulu energeticky proveditelná. Vhodná skupina permutace-inverze, která se má v této situaci použít, je D.3h(M), který je izomorfní s bodovou skupinou D3h.
Jako příklady dále slouží metan (CH4) a H3+ molekuly mají vysoce symetrické rovnovážné struktury s Td a D.3h symetrie bodových skupin; postrádají trvalé elektrické dipólové momenty, ale mají velmi slabá čistá rotační spektra kvůli rotačně odstředivému zkreslení.[20][21] Skupiny permutace-inverze potřebné pro kompletní studium CH4 a H3+ jsou Td(M) a D.3h(M).
Druhý a méně obecný přístup k symetrii nerigidních molekul je způsoben Altmannem.[22][23] V tomto přístupu jsou skupiny symetrie známé jako Schrödingerovy superskupiny a skládají se ze dvou typů operací (a jejich kombinací): (1) operace geometrické symetrie (rotace, odrazy, inverze) tuhých molekul a (2) isodynamické operace, které vezmou nerigidní molekulu do energeticky ekvivalentní formy fyzikálně přijatelným procesem, jako je rotace kolem jednoduché vazby (jako v etanu) nebo molekulární inverze (jako v amoniaku).[23]
Viz také
- Parita (fyzika) § Molekuly
- Neredukovatelné zastoupení § Aplikace v teoretické fyzice a chemii
- Woodward-Hoffmann pravidla § Korelační diagramy
- Hapticita § Hapticita a fluxionality
- Tabulka znaků
- Krystalografická skupina bodů
- Skupiny bodů ve třech dimenzích
- Symetrie rozsivkových molekul
- Symetrie v kvantové mechanice
Reference
- ^ Kvantová chemie, 3. vyd. John P. Lowe, Kirk Peterson ISBN 0-12-457551-X
- ^ Fyzikální chemie: Molekulární přístup Donald A. McQuarrie, John D. Simon ISBN 0-935702-99-7
- ^ Chemická vazba, 2. vyd. J.N. Murrell, S.F.A. Konvice, J.M.Tedder ISBN 0-471-90760-X
- ^ Fyzikální chemie, 8. vyd. P.W. Atkins a J. de Paula, W.H. Freeman, 2006 ISBN 0-7167-8759-8, kap.12
- ^ G. L. Miessler a D. A. Tarr Anorganická chemie, 2. vyd. Pearson, Prentice Hall, 1998 ISBN 0-13-841891-8, kap.4.
- ^ Molekulární symetrie a spektroskopie, 2. vyd. Philip R. Bunker a Per Jensen, NRC Research Press, Ottawa (1998) [1] ISBN 9780660196282
- ^ „Operace symetrie a tabulky znaků“. University of Exeter. 2001. Citováno 29. května 2018.
- ^ LEO Ergebnisse für "einheit"
- ^ A b C d E Pfenning, Brian (2015). Principy anorganické chemie. John Wiley & Sons. ISBN 9781118859025.
- ^ P. R. Bunker a P. Jensen (2005),Základy Molekulární symetrie (CRC Press)ISBN 0-7503-0941-5[2]
- ^ A b Longuet-Higgins, H.C. (1963). „Skupiny symetrie netuhých molekul“. Molekulární fyzika. 6 (5): 445–460. Bibcode:1963MolPh ... 6..445L. doi:10.1080/00268976300100501.
- ^ Pfennig, Brian. Principy anorganické chemie. Wiley. str. 191. ISBN 978-1-118-85910-0.
- ^ fenik, Briane. Principy anorganické chemie. Wiley. ISBN 978-1-118-85910-0.
- ^ Miessler, Gary (2004). Anorganická chemie. Pearson. ISBN 9780321811059.
- ^ Miessler, Gary L. (1999). Anorganická chemie (2. vyd.). Prentice-Hall. str. 621–630. ISBN 0-13-841891-8.
Tabulky znaků (všechny kromě D7h)
- ^ Skupinová teorie a její aplikace na kvantovou mechaniku atomových spekter, E. P. Wigner, Academic Press Inc. (1959)
- ^ Oprava dvou dlouhotrvajících chyb v tabulkách symetrie skupin bodů Randall B. Košile J. Chem. Educ. 2007, 84, 1882. Abstraktní
- ^ Rosenthal, Jenny E .; Murphy, G. M. (1936). "Skupinová teorie a vibrace polyatomových molekul". Rev. Mod. Phys. 8: 317–346. Bibcode:1936RvMP .... 8..317R. doi:10.1103 / RevModPhys.8.317.
- ^ Bone, R.G.A .; et al. (1991). "Přechodové stavy ze skupin molekulární symetrie: Analýza netuhého trimeru acetylenu". Molekulární fyzika. 72 (1): 33–73. doi:10.1080/00268979100100021.
- ^ Watson, J.K.G (1971). "Zakázaná rotační spektra polyatomových molekul". Journal of Molecular Spectroscopy. 40 (3): 546–544. Bibcode:1971JMoSp..40..536W. doi:10.1016/0022-2852(71)90255-4.
- ^ Oldani, M .; et al. (1985). „Čistá rotační spektra metanu a methanu-d4 ve vibračním základním stavu pozorovaná mikrovlnnou Fourierovou transformační spektroskopií“. Journal of Molecular Spectroscopy. 110 (1): 93–105. Bibcode:1985JMoSp.110 ... 93O. doi:10.1016/0022-2852(85)90215-2.
- ^ Altmann S.L. (1977) Indukované reprezentace v krystalech a molekulách, Academic Press
- ^ A b Flurry, R.L. (1980) Skupiny symetrie, Prentice-Hall, ISBN 0-13-880013-8, str. 115-127
externí odkazy
- Symetrie skupiny bodů @ Newcastle University
- Molekulární symetrie @ Imperial College London
- Molekulární symetrie online @ Otevřená izraelská univerzita
- Tabulky skupin symetrie skupin molekulárních bodů
- Symetrie @ Otterbein
- Internetový přednáškový kurz o molekulární symetrii @ Bergische Universitaet
- Tabulky znaků pro skupiny bodů pro chemii Odkaz


