Kubánský - Cubane
| |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC Kubánský[1] | |||
| Systematický název IUPAC Pentacyclo [4.2.0.02,5.03,8.04,7]oktan | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C8H8 | |||
| Molární hmotnost | 104,15 g / mol | ||
| Hustota | 1,29 g / cm3 | ||
| Bod tání | 133,5 ° C (272,3 ° F; 406,6 K)[2] | ||
| Bod varu | 161,6 ° C (322,9 ° F; 434,8 K)[2] | ||
| Související sloučeniny | |||
Příbuzný uhlovodíky | Cuneane Dodecahedrane Čtyřstěn Prismane Prismane C8 | ||
Související sloučeniny | Heptanitrocuban Octanitrocubane Oktaazacuban | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Kubánský (C8H8) je syntetický uhlovodík molekula který se skládá z osmi uhlík atomy uspořádány v rozích a krychle, s jedním vodík atom vázaný na každý atom uhlíku. Pevná látka krystalický látka, kuban je jedním z Platonické uhlovodíky a člen vězení. Poprvé byl syntetizován v roce 1964 Philip Eaton a Thomas Cole.[3] Před touto prací vědci věřili, že kubické molekuly na bázi uhlíku by byly příliš nestabilní, než aby existovaly. Kubický tvar vyžaduje, aby atomy uhlíku zaujaly neobvykle ostrý 90 ° úhel vazby, což by bylo velmi vysoké napjatý ve srovnání s úhlem 109,45 ° a čtyřboká uhlík. Jakmile je vytvořen, je kubán docela kineticky stabilní, kvůli nedostatku snadno dostupných cest rozkladu. Je to nejjednodušší uhlovodík s oktaedrická symetrie.
Díky vysoké potenciální energii, ale kinetické stabilitě je kuban a jeho deriváty užitečné pro řízené ukládání energie. Například, oktanitrocuban a heptanitrocubane byly studovány jako vysoce výkonné výbušniny.
Tyto sloučeniny mají také obvykle velmi vysokou hodnotu hustota pro molekuly uhlovodíků. Výsledná vysoká hustota energie znamená, že velké množství energie může být uloženo ve srovnatelně malém množství prostoru, což je důležitý faktor pro aplikace při skladování paliva a transportu energie.
Syntéza
Klasická syntéza z roku 1964 začíná převodem 2-cyklopentenon na 2-bromcyklopentadienon:[3][4]
Allylic bromace s N-bromsukcinimid v chlorid uhličitý následuje přidání molekulárního bromu k alken dává 2,3,4-tribromocyklopentanon. Ošetření této sloučeniny pomocí diethylamin v diethylether příčiny odstranění dvou ekvivalentů bromovodík za vzniku dienového produktu.
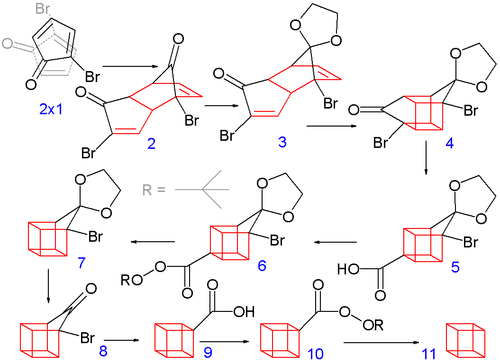 Eatonova syntéza kubanu z roku 1964
Eatonova syntéza kubanu z roku 1964
Konstrukce rámce s osmi uhlíky v kubanu začíná, když 2-bromcyklopentadienon spontánně prochází Diels-Alderova dimerizace, analogicky k dimerizaci cyklopentadien na dicyklopentadien —Dvě molekuly 1 reagovat na formu 2. Aby byly následující kroky úspěšné, pouze endo izomer je užitečný a jedná se o převládající izomer vytvořený při této reakci. Toto je nejpravděpodobnější produkt v důsledku minimalizace sterický interakce mezi bromem každé molekuly s bromem a karbonyl druhého, když se reaktanty k sobě přiblíží a minimalizují interakce podobného dipólu v přechodový stav samotné reakce. Obě karbonylové skupiny jsou chráněný tak jako acetály s ethylenglykol a str-toluensulfonová kyselina v benzen; jeden acetal se potom selektivně zbaví ochrany vodným kyselina chlorovodíková na 3.
V dalším kroku se endo izomer 3 (s oběma alken skupiny v těsné blízkosti) tvoří izomer podobný kleci 4 v fotochemické [2+2] cykloadice. The bromoketon skupina se převede na smluvně uzavřenou karboxylová kyselina 5 v Favorskii přesmyk s hydroxid draselný. Dále termální dekarboxylace probíhá prostřednictvím chlorid kyseliny (s thionylchlorid ) a tert-butyl perester 6 (s tert-butylhydroperoxid a pyridin ) až 7; poté se acetal znovu odstraní dovnitř 8. Druhé přeskupení Favorskii dává 9a nakonec další dekarboxylace dává, via 10, kubánský (11).
Deriváty
Syntéza oktafenylu derivát z tetrafenylcyklobutadien niklbromidu od Freedmana v roce 1962 předchází datu mateřské sloučeniny. Je to těžko rozpustná bezbarvá sloučenina, která taje při 425–427 ° C.[2][5][6][7] A hyperkuban, s hyperkrychle struktura, se předpokládalo, že bude existovat v publikaci z roku 2014.[8][9] Dva různé izomery kubene byly syntetizovány a třetí analyzována výpočetně. Alken v ortho-kuben je díky svému výjimečně reaktivní pyramidalizovaná geometrie. V době syntézy se jednalo o nejvíce pyramidovaný alken, který byl úspěšně vyroben.[10] The meta-kubenový izomer je ještě méně stabilní a odst-kubenový izomer pravděpodobně existuje pouze jako a diradical spíše než skutečná diagonální vazba.[11]
Cubylcubanes a Oligocubanes
Kuban (1,2-dehydrocuban) a 1,4-kubandiyl (1,4-dehydrocuban) jsou enormně napjaté sloučeniny, které podléhají nukleofilní adici velmi rychle, což chemikům umožnilo syntetizovat cubylcuban. Řešení rentgenové difrakční struktury ukázalo, že centrální cubylcubanová vazba je mimořádně krátká (1,458 Angstrom), mnohem kratší než typická jednoduchá vazba C-C (1,578 Angstrom). To je přičítáno skutečnosti, že exocyklické orbitaly kubanu jsou bohaté na s a blízko jádra.[12] Chemici na University of Chicago prodloužili a upravili sekvenci způsobem, který umožňuje přípravu hostitele [n] cubylcubane oligomerů.[13] [N] cubylcubanes jsou tuhé molekulární tyče se zvláštním příslibem v době výroby tekutých krystalů s výjimečnou UV průhledností. Jak se zvyšuje počet propojených kubanových jednotek, rozpustnost [n] cubylcubane se vrhá; ve výsledku byla v řešeních úspěšně syntetizována pouze omezená délka řetězce (až 40 jednotek). Kostra [n] cubylcubanes je stále složena z enormně napjatých uhlíkových kostek, které proto omezují její stabilitu. Naproti tomu vědci z Penn State University ukázali, že polykuban syntetizovaný reakcí v pevné fázi je 100% sp3 uhlík vázaný s čtyřbokým úhlem (109,5 stupně) a vykazuje výjimečné optické vlastnosti (vysoký index lomu). [14]
Reakce
Cuneane mohou být vyrobeny z kubanu a přeuspořádání σ-vazby katalyzované kovovými ionty.[15][16]
Viz také
Reference
- ^ Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 169. doi:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
Zachované názvy adamantan a kuban se používají v obecné nomenklatuře a jako preferované názvy IUPAC.
- ^ A b C Biegasiewicz, Kyle; Griffiths, Justin; Savage, G. Paul; Tsanakstidis, John; Priefer, Ronny (2015). „Cubane: 50 years later“. Chemické recenze. 115 (14): 6719–6745. doi:10.1021 / cr500523x. PMID 26102302.
- ^ A b Eaton, Philip E .; Cole, Thomas W. (1964). „Kubánský“. J. Am. Chem. Soc. 86 (15): 3157–3158. doi:10.1021 / ja01069a041.
- ^ Eaton, Philip E .; Cole, Thomas W. (1964). "Kubánský systém". J. Am. Chem. Soc. 86 (5): 962–964. doi:10.1021 / ja01059a072.
- ^ Freedman, H. H. (1961). „Tetrapenylcyklobutadienové deriváty. II.1 Chemické důkazy pro stav tripletů“. J. Am. Chem. Soc. 83 (9): 2195–2196. doi:10.1021 / ja01470a037.
- ^ Freedman, H. H .; Petersen, D. R. (1962). „Deriváty tetrafenylcyklobutadienu. IV.1„ Octaphenylcubane “; Dimer tetrafenylcyklobutadienu.“ J. Am. Chem. Soc. 84 (14): 2837–2838. doi:10.1021 / ja00873a046.
- ^ Pawley, G. S .; Lipscomb, W. N .; Freedman, H. H. (1964). "Struktura dimeru tetrafenylcyklobutadienu". J. Am. Chem. Soc. 86 (21): 4725–4726. doi:10.1021 / ja01075a042.
- ^ Pichierri, F. (2014). „Hypercubane: předpověď DFT založená na DFT Óh-symetrický dvouplášťový uhlovodík ". Chem. Phys. Lett. 612: 198–202. Bibcode:2014CPL ... 612..198P. doi:10.1016 / j.cplett.2014.08.032.
- ^ „Hypercubane: predikce DFT oh-symetrického dvouplášťového uhlovodíku“.
- ^ Eaton, Philip E .; Maggini, Michele (1988). "Cubene (1,2-dehydrocubane)". J. Am. Chem. Soc. 110 (21): 7230–7232. doi:10.1021 / ja00229a057.
- ^ Minyaev, Ruslan M .; Minkin, Vladimir I .; Gribanova, Tatyana N. (2009). „2.3 Teoretický přístup ke studiu a návrhu prizmatických systémů“. V Dodziuk, Helena (ed.). Napjaté uhlovodíky. Wiley. p.55. ISBN 9783527627141.
- ^ Gilardi, Richard .; Maggini, Michele .; Eaton, Philip E. (1. října 1988). "Rentgenové struktury cubylcubanu a 2-terc-butylcubylcubanu: krátké vazby klec-klec". Journal of the American Chemical Society. 110 (21): 7232–7234. doi:10.1021 / ja00229a058. ISSN 0002-7863.
- ^ Eaton, Philip E. (1992). „Kubánci: Výchozí materiály pro chemii 90. let a nového století“. Angewandte Chemie International Edition v angličtině. 31 (11): 1421–1436. doi:10.1002 / anie.199214211. ISSN 1521-3773.
- ^ Huang, Haw-Tyng; Zhu, Li; Ward, Matthew D .; Wang, Tao; Chen, Bo; Chaloux, Brian L .; Wang, Qianqian; Biswas, Arani; Gray, Jennifer L .; Kuei, Brooke; Cody, George D .; Epshteyn, Albert; Crespi, Vincent H .; Badding, John V .; Strobel, Timothy A. (21. ledna 2020). „Nanoarchitektura prostřednictvím napjatých molekul: lešení odvozená z kubanů a nejmenší uhlíková nanozávity“. Journal of the American Chemical Society. doi:10.1021 / jacs.9b12352. ISSN 0002-7863. PMID 31961671.
- ^ Smith, Michael B .; March, Jerry (2001). March's Advanced Organic Chemistry (5. vydání). John Wiley & Sons. p.1459. ISBN 0-471-58589-0.
- ^ Kindler, K .; Lührs, K. (1966). „Studien über den Mechanismus chemischer Reaktionen, XXIII. Hydrierungen von Nitrilen unter Verwendung von Terpenen als Wasserstoffdonatoren“. Chem. Ber. 99: 227–232. doi:10,1002 / cber.19660990135.