Kombinovaná injekční antikoncepce - Combined injectable birth control - Wikipedia
| Kombinovaná injekční antikoncepce | |
|---|---|
| Pozadí | |
| Typ | Hormonální |
| První použití | V roce 1969 |
| Míra selhání (první rok) | |
| Perfektní použití | 0–0.2%[1] |
| Typické použití | ? |
| Používání | |
| Efekt trvání | 1 měsíc |
| Připomenutí uživatelů | ? |
| Výhody a nevýhody | |
| STI ochrana | Ne |
| Výhody | Obzvláště dobré, pokud špatně dodržujete pilulky |
Kombinovaná injekční antikoncepce (CIC) jsou formou hormonální antikoncepce pro ženy. Skládají se z měsíčních injekce kombinovaných formulací obsahujících estrogen a a progestin aby se zabránilo těhotenství.
CIC se liší od injekční antikoncepce obsahující pouze gestagen (POIC), například sklad medroxyprogesteron-acetát (DMPA; obchodní značky Depo-Provera, Depo-SubQ Provera 104) a norethisteron enantát (NETE; značka Noristerat), které nejsou kombinovány s estrogenem a jsou podávány jednou za dva až tři měsíce místo jednou za měsíc.[2]
Hormonální antikoncepce funguje primárně tím, že brání ovulaci, ale může také zesílit cervikální hlen a bránit pronikání spermií.[3][4][5] Hormonální antikoncepce má také účinky na endometrium,[6][7] to by teoreticky mohlo ovlivnit implantaci,[8][9][10][11]
Lékařské použití
CIC se podávají intramuskulární injekcí do deltoidní, gluteus maximus nebo přední stehno.[1] V ideálním případě se podávají každých 28 až 30 dní, i když se prokázalo, že jsou účinné až 33 dní.[1]
O některých CIC se říká, že je používá transgender ženy jako prostředek feminizující hormonální terapie také.[12]
Dostupné formuláře
| Složení | Dávka | Vozidlo | Názvy značek | Dostupnost |
|---|---|---|---|---|
| Estradiol valerát / norethisteron enantát | 5 mg EV 50 mg NETE | Olejový roztok | Násobek[A] | Schváleno v nejméně 36 zemích |
| Estradiol cypionát / medroxyprogesteron-acetát | 5 mg ES 25 mg MPA | Mikrokrystalická vodná suspenze | Násobek[b] | Schváleno v nejméně 18 zemích |
| Estradiol enantát / algeston acetofenidA | 10 mg E2-EN 150 mg DHPA | Olejový roztok | Násobek[C] | Schváleno v nejméně 19 zemích |
| 5 mg E2-EN 75 mg DHPA | Olejový roztok | Anafertin†, Patector NF, Yectames | Schváleno nejméně 9 zemí | |
| 10 mg E2-EN 120 mg DHPA | Olejový roztok | Unalmes, Yectuna | Schváleno v nejméně 3 zemích | |
| 10 mg E2-EN 75 mg DHPA | Olejový roztok | Ova Repos† | Prodej ukončen (firma byla ve Španělsku) | |
| Estradiol benzoát butyrát / algeston acetofenid | 10 mg ODLIV 150 mg DHPA | Olejové řešení? | Redimen, Soluna, Unijab, Unimens§ | Schváleno v Peru a Singapuru |
| Estradiol-valerát / hydroxyprogesteron-kaproát | 5 mg EV 250 mg OHPC | Olejový roztok | Čínský injekční č. 1 | Schváleno v Číně |
| Estradiol / Megestrol-acetát | 3,5 mg E2 25 mg MGA | Mikrokrystalická vodná suspenze | Čínský injekční přípravek č. 2, Mego-E | Schváleno v Číně |
| Estradiol cypionát / hydroxyprogesteron kaproát | 5 mg ES 250 mg OHPC | Olejové řešení? | Sinbios† | Prodej ukončen (firma byla v Mexiku) |
| Estradiol valerát / Estradiol benzoát / Hydroxyprogesteron kaproát | 10 mg EV 1 mg EB 250 mg OHPC | Olejové řešení? | Sin-Ol† | Prodej ukončen (firma byla v Mexiku) |
Poznámky: Všechny jsou dány intramuskulární injekce jednou měsíčně. Poznámky pod čarou: † = Ukončeno. § = Nikdy na trhu. A = Netříděné obchodní značky (dávky neznámé; pro E2-EN / DHPA ): Evitas† a Femineo†. Zdroje: [13][2][14][15][16][17][18][19][20][21][22][23]
| ||||
Řada různých CIC, obvykle obsahující krátkodobě působící přírodní látky estradiolester a dlouhodobě působící ester progestinu, jsou k dispozici pro klinické použití.[24][15][2][16][13] Používané estrogeny zahrnují estradiol valerát, estradiol cypionát, estradiol enantát, estradiol benzoát butyrát, a estradiol, zatímco použité progestiny zahrnují norethisteron enantát, medroxyprogesteron-acetát, algeston acetofenid (dihydroxyprogesteron-acetofenid), hydroxyprogesteron kaproát, a megestrol-acetát.[15][2][16][13] Estradiol benzoát má doba trvání to je příliš krátké pro CIC jednou za měsíc a nepoužívá se v nich.[25] Naopak se říká, že estradiol enantát má trvání, které je příliš dlouhé pro CIC jednou za měsíc, ale přesto se v nich používá.[25]
Vedlejší efekty
Vedlejší účinky CIC, kromě změn menstruačního krvácení, jsou minimální.[26] Nejvýznamnější vedlejší účinky CIC jsou menstruační nepravidelnosti během prvních 3 až 6 měsíců používání.[1] Dysmenorea bylo hlášeno u 30 až 65% žen.[26] Mezi další nežádoucí účinky patří citlivost / bolest prsou, bolest hlavy, a libido Změny.[26] Nějaký zadržování tekutin může nastat, ale přibývání na váze je minimální.[26] Místní reakce v místě vpichu byly také hlášeny u 15 až 35% žen.[26]
Účinky CIC na koagulace a fibrinolýza jsou minimální a nejsou považovány za klinicky relevantní.[27] Naopak, kombinované perorální antikoncepční pilulky obsahující ethinylestradiol mají značné účinky na koagulaci a fibrinolýzu.[27] Rozdíly lze připsat nedostatku efekt prvního průchodu s parenterální podání stejně jako strukturální a farmakologické rozdíly mezi estradiolem a ethinylestradiolem.[28][29]
Farmakologie

CIC obsahují estrogen a a progestin. Estrogen je obecně krátkodobě působící estradiolester, který funguje jako proléčivo z estradiol.[24] Estery estradiolu jsou přírodní a bioidentický estrogeny a předpokládá se, že mají příznivější účinky na metabolismus lipidů, kardiovaskulární zdraví a hemostáza než syntetický estrogeny, jako je ethinylestradiol.[30][31][32] Progestin je dlouhodobě působící ester progestogenu, které mohou nebo nemusí působit jako proléčiva.[24] Progesteron deriváty počítaje v to medroxyprogesteron-acetát, algeston acetofenid (dihydroxyprogesteron-acetofenid), hydroxyprogesteron kaproát, a megestrol-acetát jsou aktivní samy o sobě a nejsou prodrogy, zatímco testosteron derivát norethisteron enantát je proléčivem norethisteron. Bez ohledu na to, zda se jedná o proléčiva nebo ne, estery steroidů tvoří a sklad a mají prodlouženou trvání akce kvůli depotní efekt při podávání intramuskulární nebo subkutánní injekce.
Protože jsou spravovány CIC parenterálně, obcházejí efekt prvního průchodu v játra a střeva který se vyskytuje u ústní podání estrogenů.[24] Odhaduje se však, že asi 20% podané dávky stále nakonec prochází játry.[24] Proto tyto přípravky nejsou zcela jaterně neutrální.[24] Nicméně mají dramaticky snížené jaterní účinky ve srovnání s perorálním ethinylestradiolem.[28] Kromě toho parenterální estradiol obecně má přibližně 4 až 5krát sníženou účinnost v játrech než perorální estradiol.[28]
| Sloučenina | Formulář | Dávka pro zvláštní použití (mg)[C] | DOA[d] | |||
|---|---|---|---|---|---|---|
| TFD[E] | POICD[F] | CICD[G] | ||||
| Algeston acetofenid | Solný olej | - | – | 75–150 | 14–32 d | |
| Gestonoron kaproát | Solný olej | 25–50 | – | – | 8–13 d | |
| Hydroxyprogest. acetát[h] | Vod. susp. | 350 | – | – | 9–16 d | |
| Hydroxyprogest. kaproát | Solný olej | 250–500[i] | – | 250–500 | 5–21 d | |
| Medroxyprog. acetát | Vod. susp. | 50–100 | 150 | 25 | 14–50 + d | |
| Megestrol-acetát | Vod. susp. | - | – | 25 | > 14 d | |
| Norethisteron enanthate | Solný olej | 100–200 | 200 | 50 | 11–52 d | |
| Progesteron | Solný olej | 200[i] | – | – | 2–6 d | |
| Vod. soln. | ? | – | – | 1–2 d | ||
| Vod. susp. | 50–200 | – | – | 7-14 d | ||
Poznámky a zdroje:
| ||||||
Dějiny
První studovaný CIC byl estradiol-valerát / hydroxyprogesteron-kaproát (EV / OHPC) v roce 1963 a druhým studovaným CIC byl estradiol enantát / algeston acetofenid (E2-EN / DHPA) v roce 1964.[26][25] V roce 1967 byl E2-EN / DHPA v pozdních fázích klinického vývoje.[50][26] V roce 1969 byl lék k dispozici pro lékařské použití pod značkou Perlutal.[51] Během několika let byl uveden na trh pod jinými značkami, jako jsou Topasel a Ova-Repos.[52][53][54][55] Kromě toho bylo do roku 1972 zavedeno pro lékařské použití několik dalších CIC.[55] Do roku 1976 se používaly dvě hlavní CIC: E2-EN / DHPA (obchodní značky Perlutan, Topasel) v Španělsko a Latinská Amerika a EV / OHPC (značka Injectable No. 1) v Čína.[56] Tyto CIC byly popsány jako CIC první generace.[56] Dvě CIC druhé generace, estradiol cypionát / medroxyprogesteron-acetát (EC / MPA; obchodní názvy Cyclofem a později Lunelle) a estradiol-valerát / norethisteron-enantát (EV / NETE; značka Mesigyna), byly zavedeny pro klinické použití v roce 1993.[57][14][15] Dne 5. října 2000 Pharmacia obdržela schválení FDA pro Lunelle měsíční antikoncepční injekci.[1] V dubnu 2003 společnost Pharmacia získala společnost Pfizer (tvůrci depotní medroxyprogesteron-acetát ).[Citace je zapotřebí ] V říjnu 2003 byla Lunelle ukončena Spojené státy.[Citace je zapotřebí ]
Společnost a kultura
Dostupnost
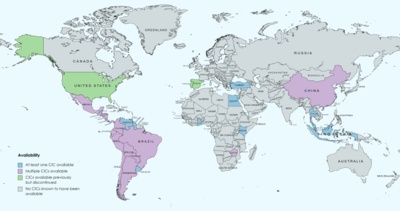
CIC jsou k dispozici v mnoha zemích po celém světě, včetně široce po celém světě Centrální a Jižní Amerika, v Mexiko a karibský, v Čína, v několika Jihovýchodní Asiat a Afričan zemích a v krocan.[21][22][23][13][2][14][15][16][17] Byly také dříve dostupné v Spojené státy, Portugalsko, a Španělsko, ale v těchto zemích byly ukončeny.[22][23]
Výzkum
Mnoho dalších CIC bylo studováno, ale nebylo schváleno nebo uvedeno na trh pro klinické použití.[15][16][58][25][59][2]
Níže jsou uvedeny na trh CIC v různých dávkách, než které jsou schváleny:
- Estradiol valerát 2,5 až 5 mg + norethisteron enantát 50 až 80 mg v an olejový roztok[15][16]
- Estradiol valerát 10 mg + hydroxyprogesteron kaproát 500 mg v olejovém roztoku[15]
- Estradiol cypionát 2,5 až 10 mg + medroxyprogesteron-acetát 12,5 až 50 mg v a mikrokrystalický vodná suspenze[15][16]
- Estradiol enantát 5 až 50 mg + algeston acetofenid 75 až 200 mg v olejovém roztoku[58][15]
Formulace poloviční dávky progestinu estradiolvalerát / norethisteron enantát (5 mg / 25 mg) je také známá jako HRP-103 a formulace poloviční dávky progestinu estradiol cypionát / medroxyprogesteron acetát (5 mg / 12,5 mg) je také známý jako HRP-113.[60]
Toto jsou CIC, která nikdy nebyla uvedena na trh:
- Estradiol valerát 20 mg + medroxyprogesteron-acetát 100 mg v mikrokrystalické vodné suspenzi[15][16]
- Estradiol undecylát 5 až 10 mg + norethisteron enantát 50 až 70 mg v olejovém roztoku[25][15][59][61]
- Estradiol cypionát + norethisteron enantát[59][15]
- Estradiol valerát 10 mg + methenmadinon kaproát 60 mg (Lutofollin)[25][59][61]
- Estradiol hexahydrobenzoát 5 mg (olejový roztok) + norgestrel 25 mg (vodná suspenze)[25][15][59][61][62]
- Estradiol cypionát 3,5 až 5 mg + megestrol-acetát 25 mg v mikrokrystalické vodné suspenzi (na trh v Číně?)[25][15][59]
- Estradiol valerát 3 až 5 mg + chlormadinon kaproát 80 mg v olejovém roztoku[25][15][59]
- Estradiol valerát 5 mg + megestrol-acetát 15 mg v an vodná suspenze z želatina mikrosféry (50–80 μm)[25][16][59][32]
- Estradiol 5 mg + levonorgestrel 7 mg v an vodná suspenze z monolitický mikrosféry (80 μm) nebo v a makrokrystalický suspenze (15 μm)[16][32]
- Estradiol cypionát 5 mg + levonorgestrel butanoát 7 mg v an vodná suspenze[16]
- Estradiol benzoát 5 až 10 mg + norethisteron enanthát 50 až 100 mg[59]
- Mestranol 1,0–1,2 mg + norethisteron 10–12 mg v a mikrokrystalický vodná suspenze definovaných velikosti částic (125–177 μm)[25][16][59][32]
- Ethinylestradiol + norethisteron[15]
- Estradiol 5 mg a progesteron 100 až 300 mg v an vodná suspenze z monolitický mikrosféry nebo v makrokrystalický suspenze[25][16][2][15][63][64][32]
- Polyestradiol fosfát 40 mg + medroxyprogesteron-acetát 150 mg[65][66][67]
Viz také
- Tabulka potencí a trvání přírodních estrogenů intramuskulární injekcí
- Zvláštní program pro lidskou reprodukci
- Koncept Foundation
- Kombinovaná hormonální antikoncepce s prodlouženým cyklem
- Koalice pro potřeby reprodukčního zdraví
- Perorální antikoncepce obsahující estradiol
Reference
- ^ A b C d E „FDA schvaluje kombinovanou měsíční injekční antikoncepci“. Zpráva o antikoncepci. 12 (3). 2001. Archivovány od originál 26. září 2006.
- ^ A b C d E F G h Bagade O, Pawar V, Patel R, Patel B, Awasarkar V, Diwate S (2014). „Zvyšující se používání dlouhodobě působící reverzibilní antikoncepce: bezpečná, spolehlivá a nákladově efektivní antikoncepce“ (PDF). Svět J Pharm Pharm Sci. 3 (10): 364–392. ISSN 2278-4357. Archivovány od originál (PDF) dne 10. 8. 2017. Citováno 2016-08-24.
- ^ MUDr. Tamara Callahan, MD, Aaron Caughey, Blueprints Obstetrics and Gynecology, 2013
- ^ KD Tripathi, Essentials of Medical Pharmacology, 2013
- ^ Učebnice porodnictví Dc Dutty, 2014
- ^ K. A. Petrie, A. H. Torgal, C. L. Westhoff, Analýza spárovaných párů ovariální suprese během užívání perorální vs. vaginální hormonální antikoncepce, „Antikoncepce“ 2011, t. 84, s. e2-3
- ^ R. L. Birtch, O. A. Olatunbosum, R. A. Pierson, Ovariální folikulární dynamika při konvenčním a kontinuálním užívání antikoncepce, „Antikoncepce“ 2006, t. 73, s. 235. str. 239.
- ^ K. Bugge, K. S. Richter, J. Bromer a kol., Míra těhotenství po oplodnění in vitro je snížena tenkým endometriem, ale nesouvisí s tloušťkou endometria nad 10 milimetrů, „Fertility and Sterility“ 2004, t. 82, s. S199.
- ^ T. Fiumino, A. Kuwata, A. Teranischi a kol., Význam tloušťky endometria pro hodnocení receptivity endometria pro embrya v přirozeném cyklu, „Plodnost a sterilita“ 2008, t. 90, s. S159.
- ^ K. S. Richter, K. R. Bugge, J. G. Bromer, Vztah mezi tloušťkou endometria a implantací embrya, založený na 1,294 cyklech oplodnění in vitro s přenosem dvou embryí ve stádiu blastocysty, „Fertility and Sterility“ 2007, t. 87, s. 53.
- ^ Rivera R, Yacobson I, Grimes D (1999). „Mechanismus působení hormonální antikoncepce a nitroděložních antikoncepčních prostředků“. Jsem J. Obstet Gynecol. 181 (5 Pt 1): 1263–9. doi:10.1016 / S0002-9378 (99) 70120-1. PMID 10561657.
- ^ Don Kulick (12. ledna 2009). Travesti: Sex, pohlaví a kultura mezi brazilskými transgenderovými prostitutkami. University of Chicago Press. str. 64–66. ISBN 978-0-226-46101-4.
- ^ A b C d Pracovní skupina IARC pro hodnocení karcinogenních rizik pro člověka; Mezinárodní agentura pro výzkum rakoviny (1. ledna 1999). Hormonální antikoncepce a postmenopauzální hormonální terapie (PDF). IARC. str. 65. ISBN 978-92-832-1272-0.
- ^ A b C Pramilla Senanayake; Malcolm Potts (14. dubna 2008). Atlas antikoncepce, druhé vydání. CRC Press. str. 50–. ISBN 978-0-203-34732-4.
- ^ A b C d E F G h i j k l m n Ó p q r Newton JR, D'arcangues C, Hall PE (1994). „Přehled„ kombinovaných injekčních antikoncepčních prostředků “„ jednou za měsíc “. J Obstet Gynaecol (Lahore). 4 Suppl 1: S1–34. doi:10.3109/01443619409027641. PMID 12290848.
- ^ A b C d E F G h i j k l m n Garza-Flores J (duben 1994). „Farmakokinetika injekčních kontraceptiv podávaných jednou za měsíc“. Antikoncepce. 49 (4): 347–59. doi:10.1016/0010-7824(94)90032-9. PMID 8013219.
- ^ A b Pracovní skupina IARC pro hodnocení karcinogenních rizik pro člověka; Světová zdravotnická organizace; Mezinárodní agentura pro výzkum rakoviny (2007). Kombinovaná antikoncepce s estrogenem a gestagenem a kombinovaná menopauzální léčba estrogenem a gestagenem. Světová zdravotnická organizace. 431–. ISBN 978-92-832-1291-1.
- ^ Klitsch M (1995). „Stále čekám na antikoncepční revoluci“. Fam Plann Perspect. 27 (6): 246–53. doi:10.2307/2136177. PMID 8666089.
- ^ Gallo MF, Grimes DA, Lopez LM, Schulz KF, d'Arcangues C (2013). "Kombinovaná injekční antikoncepce pro antikoncepci". Cochrane Database Syst Rev. 3: CD004568. doi:10.1002 / 14651858.CD004568.pub3. PMID 23641480.
- ^ Harry W. Rudel; Fred A. Kinel (září 1972). "Perorální antikoncepce. Studie lidské plodnosti a vedlejší účinky". V M. Tausk (ed.). Farmakologie endokrinního systému a příbuzných léčiv: Progesteron, progestagena a látky proti neplodnosti. II. Pergamon Press. 385–469. ISBN 978-0080168128. OCLC 278011135.
- ^ A b https://www.drugs.com/international/
- ^ A b C Sweetman, Sean C., vyd. (2009). "Sexuální hormony a jejich modulátory". Martindale: The Complete Drug Reference (36. vydání). London: Pharmaceutical Press. str. 2082. ISBN 978-0-85369-840-1.
- ^ A b C http://www.micromedexsolutions.com/micromedex2/librarian/
- ^ A b C d E F V. Unzeitig; Rick H.W. van Lunsen (15. února 2000). Antikoncepční volby a realita: Sborník z 5. kongresu Evropské společnosti pro antikoncepci. CRC Press. 133, 136. ISBN 978-1-85070-067-8.
- ^ A b C d E F G h i j k l m Toppozada MK (duben 1994). "Existující kombinovaná injekční antikoncepce jednou za měsíc". Antikoncepce. 49 (4): 293–301. doi:10.1016/0010-7824(94)90029-9. PMID 8013216.
- ^ A b C d E F G Benagiano, G .; Primiero, F.M. (1983). "Současný stav dlouhodobě působících antikoncepcí". Drogy. 25 (6): 570–609. doi:10.2165/00003495-198325060-00003. ISSN 0012-6667.
- ^ A b „Fakta o injekčních antikoncepcích podávaných jednou měsíčně: memorandum ze setkání WHO“. Býk. Světový zdravotnický orgán. 71 (6): 677–89. 1993. PMC 2393537. PMID 8313486.
- ^ A b C Kuhl H (2005). „Farmakologie estrogenů a progestogenů: vliv různých cest podání“ (PDF). Klimakterický. 8 Suppl 1: 3–63. doi:10.1080/13697130500148875. PMID 16112947.
- ^ von Schoultz, Bo; Carlström, Kjell; Collste, Lars; Eriksson, Ambjörn; Henriksson, Peter; Pousette, Åke; Stege, Reinhard (1989). "Estrogenová terapie a funkce jater - metabolické účinky orálního a parenterálního podání". Prostata. 14 (4): 389–395. doi:10.1002 / pros.2990140410. ISSN 0270-4137.
- ^ Michael Oettel; Ekkehard Schillinger (6. prosince 2012). Estrogeny a antiestrogeny II: Farmakologie a klinické použití estrogenů a antiestrogenů. Springer Science & Business Media. str. 235–237, 261, 271. ISBN 978-3-642-60107-1.
Zde uvažované přírodní estrogeny zahrnují: [...] Estery 17β-estradiolu, jako je estradiol valerát, estradiol benzoát a estradiol cypionát. Cílem esterifikace je buď lepší absorpce po orálním podání, nebo trvalé uvolnění z depa po intramuskulárním podání. Během absorpce jsou estery štěpeny endogenními esterázami a uvolňuje se farmakologicky aktivní 17p-estradiol; proto jsou estery považovány za přírodní estrogeny.
- ^ Nagrath Arun; Malhotra Narendra; Seth Shikha (15. prosince 2012). Pokrok v porodnictví a gynekologii - 3. Jaypee Brothers Medical Publishers Pvt. Ltd. str. 419–. ISBN 978-93-5090-575-3.
- ^ A b C d E F Sang GW (duben 1994). „Farmakodynamické účinky kombinovaných injekčních kontraceptiv jednou měsíčně“. Antikoncepce. 49 (4): 361–85. doi:10.1016/0010-7824(94)90033-7. PMID 8013220.
- ^ Knörr K, Beller FK, Lauritzen C (17. dubna 2013). Lehrbuch der Gynäkologie. Springer-Verlag. 214–. ISBN 978-3-662-00942-0.
- ^ Knörr K, Knörr-Gärtner H, Beller FK, Lauritzen C (8. března 2013). Geburtshilfe und Gynäkologie: Physiologie und Pathologie der Reproduktion. Springer-Verlag. str. 583–. ISBN 978-3-642-95583-9.
- ^ A. Labhart (6. prosince 2012). Klinická endokrinologie: teorie a praxe. Springer Science & Business Media. str. 554–. ISBN 978-3-642-96158-8.
- ^ Horský J, Presl J (1981). "Hormonální léčba poruch menstruačního cyklu". In Horsky J, Presl K (eds.). Funkce vaječníků a její poruchy: diagnostika a terapie. Springer Science & Business Media. 309–332. doi:10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Joachim Ufer (1969). Principy a praxe hormonální terapie v gynekologii a porodnictví. de Gruyter. str. 49.
17α-Hydroxyprogesteron kaproát je depotní progestogen, který je zcela bez vedlejších účinků. Dávka potřebná k vyvolání sekrečních změn v aktivovaném endometriu je přibližně 250 mg. na menstruační cyklus.
- ^ Willibald Pschyrembel (1968). Praktische Gynäkologie: für Studierende und Ärzte. Walter de Gruyter. 598, 601. ISBN 978-3-11-150424-7.
- ^ Ferin J (září 1972). "Účinky, doba působení a metabolismus u člověka". In Tausk M (ed.). Farmakologie endokrinního systému a příbuzných léčiv: Progesteron, progestagena a látky proti neplodnosti. II. Pergamon Press. s. 13–24. ISBN 978-0080168128. OCLC 278011135.
- ^ Henzl MR, Edwards JA (10. listopadu 1999). „Farmakologie progestinů: deriváty 17α-hydroxyprogesteronu a progestiny první a druhé generace“. In Sitruk-Ware R, Mishell DR (eds.). Progestiny a antiprogestiny v klinické praxi. Taylor & Francis. 101–132. ISBN 978-0-8247-8291-7.
- ^ Janet Brotherton (1976). Farmakologie pohlavních hormonů. Akademický tisk. str. 114. ISBN 978-0-12-137250-7.
- ^ Goebelsmann U (1986). "Farmakokinetika antikoncepčních steroidů u lidí". V Gregoire AT, Blye RP (eds.). Antikoncepční steroidy: farmakologie a bezpečnost. Springer Science & Business Media. str. 67–111. doi:10.1007/978-1-4613-2241-2_4. ISBN 978-1-4613-2241-2.
- ^ Becker H, Düsterberg B, Klosterhalfen H (1980). „[Biologická dostupnost cyproteron-acetátu po orální a intramuskulární aplikaci u mužů (autorský překlad)]“ [Biologická dostupnost cyproteron-acetátu po orální a intramuskulární aplikaci u mužů]. Urologia Internationalis. 35 (6): 381–5. doi:10.1159/000280353. PMID 6452729.
- ^ Moltz L, Haase F, Schwartz U, Hammerstein J (květen 1983). „[Léčba virilizovaných žen intramuskulárním podáním cyproteron-acetátu]“ [Účinnost intramuskulárně aplikovaného cyproteron-acetátu při hyperandrogenismu]. Geburtshilfe Und Frauenheilkunde. 43 (5): 281–7. doi:10.1055 / s-2008-1036893. PMID 6223851.
- ^ Wright JC, Burgess DJ (29. ledna 2012). Dlouhodobě působící injekce a implantáty. Springer Science & Business Media. str. 114–. ISBN 978-1-4614-0554-2.
- ^ Chu YH, Li Q, Zhao ZF (duben 1986). „Farmakokinetika megestrol-acetátu u žen, které dostávají IM injekci dlouhodobě působící injekční antikoncepce estradiol-megestrol“. Čínský žurnál klinické farmakologie.
Výsledky ukázaly, že po injekci rychle vzrostla koncentrace MA v plazmě. Mezitím byla maximální hladina MA v plazmě 3. den, u všech subjektů existoval lineární vztah mezi logaritmem koncentrace MA v plazmě a časem (den), eliminační poločas t1 / 2β = 14,35 ± 9,1 dne.
- ^ Runnebaum BC, Rabe T, Kiesel L (6. prosince 2012). Ženská antikoncepce: aktualizace a trendy. Springer Science & Business Media. str. 429–. ISBN 978-3-642-73790-9.
- ^ Artini PG, Genazzani AR, Petraglia F (11. prosince 2001). Pokroky v gynekologické endokrinologii. CRC Press. str. 105–. ISBN 978-1-84214-071-0.
- ^ King TL, Brucker MC, Kriebs JM, Fahey JO (21. října 2013). Varneyova porodní asistentka. Vydavatelé Jones & Bartlett. str. 495–. ISBN 978-1-284-02542-2.
- ^ Hecht-Lucari, G. (1967). Recientes Progresos de la Terapia Hormonal en Ginecología. Revista Colombiana de Obstetricia y Ginecología, 18 (5), 307-319. 10.18597 / rcog.2584 https://revista.fecolsog.org/index.php/rcog/article/view/2584}}
- ^ Hispano americano. Tiempo. Květen 1969. str. 46.
Entre los anovulatorios más usados están los siguientes: Prolestrín, Sequens, Anovlar, Sequentex, Orlex, Ginovlar, Enginón, Perlutal, Depo-proveda, Aconcén, Ovral, Retex, Lorophyn y otros menos solicitados.
- ^ Botella-Llusia, J. (1970). Les ovaires au cours de l'administration des sterpides anticonceptionnels. [Vaječníky během podávání antikoncepčních steroidů.] In: Netter, A. L'Inhibition de l'ovulation; Colloque de la Societe Nationale pour l'Etude de la Sterilite et de la Fecondite. (Inhibition of ovulation: Proceedings of the National Society for the Study of Sterility and Fertility.) Paris, Masson, 1970. s. 141-156
- ^ Universidad Complutense de Madrid (1971). Revista de la Universidad de Madrid. Prensa de la Universidad de Madrid. str. 11.
- ^ Liria, R. H. (1972). Anticoncepcionismo (Un problema de hoy, de ayer y de siempre). In Anales de medicina y cirugía (sv. 52, č. 230, s. 329-348). https://www.raco.cat/index.php/AnalesMedicina/article/download/99455/152590
- ^ A b Harry W. Rudel; Fred A. Kinel (září 1972). "Perorální antikoncepce. Studie lidské plodnosti a vedlejší účinky". V M. Tausk (ed.). Farmakologie endokrinního systému a příbuzných léčiv: Progesteron, progestagena a látky proti neplodnosti. II. Pergamon Press. 385–469. ISBN 978-0080168128. OCLC 278011135.
- ^ A b J. Bringer; B. Hedon (15. září 1995). Plodnost a sterilita: aktuální přehled. CRC Press. str. 47–. ISBN 978-1-85070-694-6.
- ^ d'Arcangues C (1993). „Injekční antikoncepce jednou za měsíc“. Světové fórum o zdraví. 14 (4): 439–40. PMID 8185807.
- ^ A b Koetsawang S (duben 1994). „Injekční antikoncepce jednou měsíčně: účinnost a důvody pro ukončení léčby“. Antikoncepce. 49 (4): 387–98. doi:10.1016/0010-7824(94)90034-5. PMID 8013221.
- ^ A b C d E F G h i j Mokhtar K. Toppozada (1983). "Měsíčně injekční antikoncepce". V Alfredo Goldsmith; Mokhtar Toppozada (eds.). Dlouhodobě působící antikoncepce. 93–103. OCLC 35018604.
- ^ Nevyplněný Drugs Pharm AID. Neuvedené léky. 1993. s. 247. ISBN 978-0-913210-14-7.
- ^ A b C Toppozada M (červen 1977). „Klinické použití antikoncepčních přípravků podávaných každý měsíc“. Obstet Gynecol Surv. 32 (6): 335–47. doi:10.1097/00006254-197706000-00001. PMID 865726.
- ^ de Souza, J. C .; Coutinho, Elsimar M. (1972). "Kontrola plodnosti pomocí měsíčních injekcí směsi norgestrelu a dlouhodobě působícího estrogenu". Antikoncepce. 5 (5): 395–399. doi:10.1016/0010-7824(72)90031-5. ISSN 0010-7824. PMID 4650657.
- ^ Garza-Flores J, Fatinikun T, Hernandez L, Ramos I, Cardenas M, Menjivar M (červenec 1991). „Pilotní studie o hodnocení dlouhodobého uvolňování progesteronu / estradiolu jako antikoncepčního přípravku s jednou injekcí za měsíc“. Antikoncepce. 44 (1): 45–59. doi:10.1016 / 0010-7824 (91) 90105-O. PMID 1893701.
- ^ Garza-Flores J, Hall PE, Perez-Palacios G (1991). „Dlouhodobě působící hormonální antikoncepce pro ženy“. J. Steroid Biochem. Mol. Biol. 40 (4–6): 697–704. doi:10.1016 / 0960-0760 (91) 90293-E. PMID 1958567.
- ^ Joseph William Goldzieher; Kenneth Fotherby (1994). Farmakologie antikoncepčních steroidů. Raven Press. str. 154. ISBN 978-0-7817-0097-9.
- ^ Zañartu J, Rice-Wray E, Goldzieher JW (říjen 1966). „Kontrola plodnosti pomocí dlouhodobě působících injekčních steroidů. Předběžná zpráva“. Obstet Gynecol. 28 (4): 513–5. doi:10.1097/00006250-196610000-00011. PMID 5925038.
- ^ Harry Beckman (1967). Roční kniha lékové terapie. Vydavatelé knižních ročníků.
Další čtení
- Garza-Flores J (duben 1994). „Farmakokinetika injekčních kontraceptiv podávaných jednou za měsíc“. Antikoncepce. 49 (4): 347–59. doi:10.1016/0010-7824(94)90032-9. PMID 8013219.
- Sang GW (duben 1994). „Farmakodynamické účinky kombinovaných injekčních kontraceptiv jednou měsíčně“. Antikoncepce. 49 (4): 361–85. doi:10.1016/0010-7824(94)90033-7. PMID 8013220.
