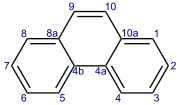
Fenantren - Phenanthrene
 | |
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Fenantren | |
| Ostatní jména Tricyklo [8.4.0.02,7] tetradeka-1,3,5,7,9,11,13-heptaen | |
| Identifikátory | |
3D model (JSmol ) | |
| 1905428 | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.001.437 |
| Číslo ES |
|
| 28699 | |
| KEGG | |
| Pletivo | C031181 |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C14H10 | |
| Molární hmotnost | 178.234 g · mol−1 |
| Vzhled | Bezbarvá pevná látka |
| Hustota | 1,18 g / cm3[1] |
| Bod tání | 101 ° C (214 ° F; 374 K)[1] |
| Bod varu | 332 ° C (630 ° F; 605 K)[1] |
| 1,6 mg / l[1] | |
| -127.9·10−6 cm3/ mol | |
| Nebezpečí | |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | 171 ° C (340 ° F; 444 K)[1] |
| Struktura | |
| C2v[2] | |
| 0 D | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Fenantren je pravděpodobná karcinogenní sloučenina, která představuje velké riziko toxicity pro exponované živé organismy. Je to polycyklický aromatický uhlovodík (PAH) - což je velká skupina organických sloučenin vyskytujících se ve skupinách po dvou nebo více. [3] Fenanthren se vyskytuje přirozeně a je také chemickou látkou. Lidé jsou běžně vystaveni působení fenanthrenu vdechováním cigaretového kouře, ale existuje mnoho způsobů expozice. Důkazy prokázané studiemi na zvířatech ukazují, že fenanthren je potenciální karcinogen [3]. Vypadá jako bezbarvá krystalická pevná látka, ale může také vypadat žlutě.[4]
Fenanthren se používá k výrobě barviv, plastů a pesticidů, výbušnin a drog. Používá se také k užívání žlučových kyselin, cholesterolu a steroidů.[4]
Sloučenina s fenanthrenovým skeletem a dusíky v polohách 4 a 5 je známá jako fenanthrolin.
Chemie
Fenanthren je téměř nerozpustný ve vodě, ale je rozpustný ve většině organických rozpouštědel s nízkou polaritou, jako je toluen, chlorid uhličitý, éter, chloroform, octová kyselina a benzen.
The Syntéza fenantrenu Bardhan – Sengupta je klasický způsob výroby fenanthrenů.[5]
Tento proces zahrnuje elektrofilní aromatická substituce pomocí uvázaného cyklohexanol skupina pomocí oxid fosforečný, který uzavírá centrální kruh na existující aromatický kruh. Dehydrogenace použitím selen převádí také ostatní kruhy na aromatické. Aromatizace šestičlenných kruhů selenem není jasně známa, ale produkuje H2Se.
Fenanthren lze také z určitých získat fotochemicky diaryletheny.
Reakce fenanthrenu se obvykle vyskytují v pozicích 9 a 10, včetně:
- Organická oxidace na fenanthrenochinon s kyselina chromová[6]
- Organická redukce až 9,10-dihydrofenanthren s vodík plyn a Raneyův nikl[7]
- Elektrofilní halogenace až 9-bromfenanthren s bróm[8]
- Aromatická sulfonace na 2 a 3-fenanthrenesulfonové kyseliny s kyselina sírová[9]
- Ozonolýza na difenylaldehyd[10]
Kanonické formy
Fenanthren je stabilnější než jeho lineární izomer anthracen. Klasické a dobře zavedené vysvětlení je založeno na Clarovo pravidlo. Nová teorie se dovolává takzvané stabilizační vodíkové vodíkové vazby mezi atomy vodíku C4 a C5.
Přirozené výskyty
Ravatit je přírodní minerál sestávající z fenanthrenu.[11] Nachází se v malém množství mezi několika místy spalujícími uhlí. Ravatit představuje malou skupinu organických minerálů.
V rostlinách
Viz také
Reference
- ^ A b C d E Záznam CAS RN 85-01-8 v databázi látek GESTIS Institut pro bezpečnost a ochranu zdraví při práci
- ^ Peter Atkins, J. D. P., Atkinsova fyzikální chemie. Oxford: 2010. str. 443
- ^ A b "Fenanthren" (PDF). EPA.gov. Citováno 3. října 2020.
- ^ A b "Informační list o fenantrenech" (PDF). archive.epa.gov. Americká agentura na ochranu životního prostředí. Citováno 19. července 2019.
- ^ „Bardhan Sengupta Synthesis“. Komplexní reakce organických jmen a reagenty. 49. 2010. str. 215–219. doi:10.1002 / 9780470638859.conrr049.
- ^ Organické syntézy, Sb. Sv. 4, str. 757 (1963); Sv. 34, s. 76 (1954) Odkaz
- ^ Organické syntézy, Sb. Sv. 4, str. 313 (1963); Sv. 34, s. 31 (1954) Odkaz.
- ^ Organické syntézy, Sb. Sv. 3, str. 134 (1955); Sv. 28, s. 19 (1948) Odkaz.
- ^ Organické syntézy, Sb. Sv. 2, str. 482 (1943); Sv. 16, s. 63 (1936) Odkaz.
- ^ Organické syntézy, Sb. Sv. 5, str. 489 (1973); Sv. 41, s. 41 (1961) Odkaz.
- ^ Ravatitová minerální data
externí odkazy
- Fenantren na scorecard.org


