Flavonol 3-O-glukosyltransferáza - Flavonol 3-O-glucosyltransferase

| Flavonol 3-O-glukosyltransferáza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifikátory | |||||||||
| EC číslo | 2.4.1.91 | ||||||||
| Číslo CAS | 50812-18-5 | ||||||||
| Databáze | |||||||||
| IntEnz | IntEnz pohled | ||||||||
| BRENDA | Vstup BRENDA | ||||||||
| EXPASY | Pohled NiceZyme | ||||||||
| KEGG | Vstup KEGG | ||||||||
| MetaCyc | metabolická cesta | ||||||||
| PRIAM | profil | ||||||||
| PDB struktur | RCSB PDB PDBe PDBsum | ||||||||
| Genová ontologie | AmiGO / QuickGO | ||||||||
| |||||||||
v enzymologie, a flavonol 3-O-glukosyltransferáza (ES 2.4.1.91 ) je enzym že katalyzuje the chemická reakce
- UDP-glukóza + flavonol UDP + flavonol 3-O-beta-D-glukosid
Tedy dva substráty tohoto enzymu jsou UDP-glukóza a flavonol, zatímco jeho dva produkty jsou UDP a flavonol 3-O-beta-D-glukosid. Flavonoidy, které mohou v této reakci působit jako substráty, zahrnují kvercetin, kaempferol, dihydrokaempferol, kaempferid, fisetin a isorhamnetin. Flavonol 3-O-glukosyltransferáza je enzym pro přenos hexosylové skupiny.[1]
Tento enzym je znám pod systematickým názvem UPD-glukóza: flavonol 3-O-D glukosyltransferáza a podílí se na biosyntéza flavonoidů a způsobí vznik antokyany. Antokyany produkují v rostlinných tkáních fialovou barvu, ve které jsou přítomny.[2]
Je to enzym, který se nejvíce vyskytuje v hroznech (Vitis vinifera ).[3] Tento enzym se nachází také v řadě dalších rostlin - jako jsou hledáčky (Antirrhinum majus ), kapusta (Brassica oleracea ) a grapefruit (Citrus x paradisi ).[4]
Cesty
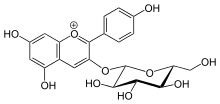
Tento enzym se podílí na biosyntéze sekundárních metabolitů. Primární funkcí tohoto enzymu v jeho dráze je vazba a glukosid na molekulu flavonolu za vzniku 3-O-glukosidu flavonolu.[5] Prostřednictvím tohoto mechanismu dochází k přeměně enzymu antokyanidiny na antokyany jako součást fenylpropanoid cesta. Jedním konkrétním příkladem může být působení těchto enzymů na pelargonidin. Flavonol 3-O-glukosyltransferáza váže glukosid na tento protein a vytváří pelargonidin 3-O-glukosid. Tento enzym se také účastní dráhy flavonových glykosidů a modifikace daphnetinu v některých organismech. Úlohou enzymu v těchto drahách je opět vázat glukosid k substrátu a konstruovat 3-O-glukosid flavonolu.[6]

Nomenklatura
Tento enzym patří do rodiny glykosyltransferázy, konkrétně hexosyltransferázy. The systematické jméno této třídy enzymů je UDP-glukóza: flavonol 3-O-D-glukosyltransferáza. Mezi další běžně používaná jména patří:
- GTI,
- uridin difosfoglukóza-flavonol 3-O-glukosyltransferáza,
- UDP-glukóza: flavonol 3-O-glukosyltransferáza a
- UDP-glukóza: flavonoid 3-O-glukosyltransferáza (UFGT).
Mezi nimi se UFGT dělí na UDP-glukózu: Flavonoid 3-O-glukosyltransferázu (UF3GT) a UDP-glukózu: Flavonoid 5-O-glukosyltransferázu (UF5GT), které jsou odpovědné za glukosylaci antokyany produkovat stabilní molekuly.[7]
Inhibitory a struktura enzymu
Některé z inhibitorů tohoto enzymu zahrnují CaCl2, CoCl2, Cu+2CuCl2, KCl, Mg+2a Mn+2.[8] Primárním zbytkem aktivního místa tohoto enzymu je Asp181, jak bylo stanoveno studiemi toho, jak mutace ovlivňují kapacitu enzymu.[9] Existuje několik dokumentací o krystalické struktuře 3-O-glukosyltransferázy flavonolu (2C1X, 2C1Z a 2C9Z),[10] a na základě těchto vykreslení enzymu existuje pouze jedna podjednotka ve kvartérní struktuře molekuly.
Reference
- ^ http://brenda-enzymes.info/enzyme.php?ecno=2.4.1.91&Suchword=&reference=&organism%5B%5D=Vitis+vinifera&show_tm=0#REACTION TYP
- ^ Dooner, H.K. & Nelson, O.E. Biochem Genet (1977) 15: 509. doi:10.1007 / BF00520194
- ^ Kobayashi S, Ishimaru M, Ding CK, Yakushiji H, Goto N (únor 2001). „Porovnání genových sekvencí UDP-glukózy: flavonoidové 3-O-glukosyltransferázy (UFGT) mezi bílými hrozny (Vitis vinifera) a jejich sportem s červenou kůží.“ Plant Sci. 160 (3): 543–550. doi:10.1016 / S0168-9452 (00) 00425-8. PMID 11166442.
- ^ „BRENDA - Informace o EC 2.4.1.91 - flavonol 3-O-glukosyltransferáza“.
- ^ http://brenda-enzymes.info/enzyme.php?ecno=2.4.1.91&Suchword=&reference=&organism%5B%5D=Vitis+vinifera&show_tm=0#SOURCE TKÁŇ
- ^ „KEGG ENZYME: 2.4.1.115“. www.genome.jp. Citováno 2016-12-06.
- ^ Zhao DQ, Han CX, Ge JT, Tao J (listopad 2012). „Izolace UDP-glukózy: Flavonoidový gen 5-0-glukosyltransferázy a analýza exprese biosyntetických genů antokyanů v bylinné pivoňce (Paeonia lactiflora Pall.)“. Electronic Journal of Biotechnology. 15 (6). doi:10.2225 / vol15-issue6-fulltext-7.
- ^ Schomburg, profesor Dietmar; Schomburg, Dr. Ida, eds. (1. ledna 2006). "Flavonol 3-O-glukosyltransferáza". Springer Handbook of Enzymes. 32. Springer Berlin Heidelberg. 21–29. doi:10.1007/978-3-540-49534-5_2. ISBN 978-3-540-32591-8.
- ^ Hiromoto, Takeshi; Honjo, Eijiro; Noda, Naonobu; Tamada, Taro; Kazuma, Kohei; Suzuki, Masahiko; Blaber, Michael; Kuroki, Ryota (06.12.2016). „Strukturální základ pro rozpoznávání UDP-glukózy mezi akceptorem a substrátem: antokyanidinová 3-O-glukosyltransferáza z Clitoria ternatea“. Věda o bílkovinách. 24 (3): 395–407. doi:10.1002 / pro.2630. ISSN 0961-8368. PMC 4353365. PMID 25556637.
- ^ W, Offen; C, Martinez-Fleites; M, Yang; E, Kiat-Lim; B.G, Davis; C.A, Tarling; C.M, Ford; D.J, Bowles; G.J., Davies (01.01.2006). „Struktura flavonoidové glukosyltransferázy odhaluje základ pro modifikaci přírodních rostlinných produktů“. EMBO J.. 25 (6): 1396–405. doi:10.1038 / sj.emboj.7600970. PMC 1422153. PMID 16482224.
Další čtení
- Wiermann R (1982). „Tvorba flavonol 3-O-diglykosidů a flavonol 3-O-triglykosidů enzymovými extrakty z prašníků Tulipa cv apeldoorn - charakterizace a aktivita 3 různých O-glykosyltransferáz během vývoje prašníku“. Z. Naturforsch. C. 37: 587–599. doi:10.1515 / znc-1982-7-808. S2CID 37241803.
- Sutter A, Grisebach H (1973). „UDP-glukóza: flavonol 3-0-glukosyltransferáza z buněčných suspenzních kultur petrželky“. Biochim. Biophys. Acta. 309 (2): 289–95. doi:10.1016/0005-2744(73)90027-2. PMID 4731963.

