Kyselina trifosforečná - Triphosphoric acid
tento článek potřebuje další citace pro ověření. (Prosince 2014) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC Difosfono hydrogenfosforečnan | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.030.752 |
| Číslo ES |
|
| KEGG | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| H5P3Ó10 | |
| Molární hmotnost | 257,95 g / mol |
| Kyselost (strK.A) | malý, malý, 2,30, 6,50, 9,24 |
| Konjugovaná základna | Trifosfát |
| Nebezpečí | |
| Hlavní nebezpečí | Žíravý (C) |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
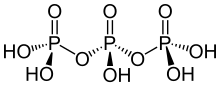
Kyselina trifosforečná (taky kyselina tripolyfosforečná), se vzorcem H5P3Ó10, je zhuštěný druh kyselina fosforečná. V rodině kyseliny fosforečné, je to další kyselina polyfosforečná po kyselina pyrofosforečná, H4P2Ó7, nazývaná také kyselina difosforečná.
Sloučeniny jako ATP (adenosintrifosfát ) jsou estery kyseliny trifosforečné.
Kyselina trifosforečná nebyla získána v krystalické formě. Rovnovážná směs s celkovým složením odpovídající H5P3Ó10 obsahuje asi 20% kyseliny trifosforečné. Roztok čistých druhů lze získat iontovou výměnou sodné soli, trifosforečnan sodný, při 0 ° C.[1]
Kyselina trifosforečná je a kyselina pentaprotová, což znamená, že může uvolnit pět protonů v dostatečně základních podmínkách. Různé strK.A hodnoty jsou uvedeny, 1,0; 2,2; 2,3; 5,7; 8,5,[1] 1.0 ; 2.2 ; 2.3 ; 3.7 ; 8.5 [2]
Reference
- ^ A b Corbridge, D. (1995). „Kapitola 3: Fosfáty“. Studies in anorganic Chemistry sv. 20. Elsevier Science B.V. str. 169–305. ISBN 0-444-89307-5.
- ^ Holleman, Arnold Frederik; Wiberg, Egon (2001), Wiberg, Nils (ed.), Anorganická chemie, přeloženo Eaglesonem, Mary; Brewer, William, San Diego / Berlin: Academic Press / De Gruyter, str. 729, ISBN 0-12-352651-5
| Tento anorganické sloučenina –Vztahující se článek je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
