Grepafloxacin - Grepafloxacin
 | |
| Klinické údaje | |
|---|---|
| AHFS /Drugs.com | Více informací pro spotřebitele |
| ATC kód | |
| Farmakokinetické data | |
| Vazba na bílkoviny | 50% |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.159.692 |
| Chemické a fyzikální údaje | |
| Vzorec | C19H22FN3Ó3 |
| Molární hmotnost | 359.401 g · mol−1 |
| 3D model (JSmol ) | |
| Chirality | Racemická směs |
| |
| |
| (ověřit) | |
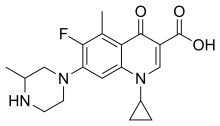
Grepafloxacin (jméno výrobku Raxar, Glaxo Wellcome ) byl orální širokospektrální fluorochinolon antibakteriální prostředek používaný k léčbě bakteriální infekce. Grepafloxacin byl celosvětově stažen z trhů v roce 1999,[1][2] kvůli jeho vedlejšímu účinku prodloužení QT interval na elektrokardiogram, vedoucí k srdečním příhodám a nenadálá smrt.[3]
Klinické použití
Grepafloxacin byl použit k léčbě exacerbací chronické bronchitidy způsobené citlivými bakteriemi (např. Haemophilus influenzae, Streptococcus pneumoniae, Moraxella catarrhalis ),[4][5][6] komunitní pneumonie (včetně těch, kromě výše uvedených choroboplodných zárodků, způsobených Mycoplasma pneumoniae )[7][8] kapavka a negonokoková uretritida a cervicitida (například způsobeno Chlamydia trachomatis nebo Ureaplasma urealyticum ).[9][10]
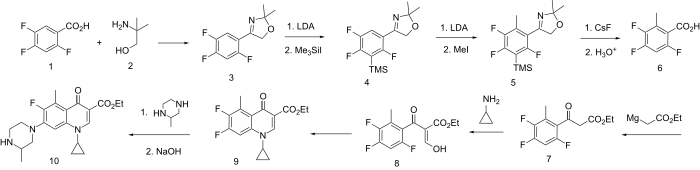
Syntéza
Příprava chinolonů nesoucích substituent v poloze 5 je komplikována větším elektrofilním charakterem polohy 8. Jedno schéma řešení problému spočívá v blokování přístupu na pozici 8 nejprve přidáním snadno odstranitelné skupiny do tohoto středu.
Schéma začíná přeměnou karboxylové kyseliny na (1) na jeho dimethyloxazolinový derivát (3) reakcí s aminomethyl propanol (2). Lithium diisopropylamid (LDA) poté odstraní proton z polohy 8; zacházení s tímto aniontem trimethylsilyljodid vede k silylovanému meziproduktu (4). Druhé kolo LDA pak vygeneruje a karbanion v jediné otevřené poloze; reakce s methyljodid vede k odpovídajícímu 5 methylderivátu (5). Zacházení s tímto výrobkem fluorid cesný rozbije vazbu uhlík-křemík odstraněním silylové skupiny; vodná kyselina pak hydrolyzuje oxazolin dovolit volnou kyselinu (6). Tento poslední meziprodukt se poté převezme na chinolon (9) [13] v podstatě stejným schématem, jaké se používalo při přípravě difloxacin, s tím rozdílem, že prodloužení řetězce je pomocí Grignardova činidla z ethylbromacetát. Léčba (9) s 2-methylpiperazinem probíhá reakcí na méně bráněné ze dvou aminoskupin; zmýdelnění pak poskytuje grepafloxacin (10).
Stereochemie
Grepafloxacin obsahuje stereocentrum a skládá se ze dvou enantiomerů. Tohle je racemát, tj. směs 1: 1 (R) - a (S)-formuláře:
| Enantiomery grepafloxacinu | |
|---|---|
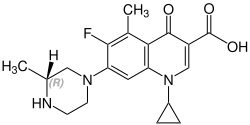 (R) -grepafloxacin Číslo CAS: 146761-68-4 | 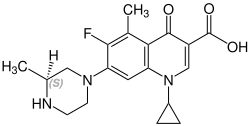 (S) -grepafloxacin CAS číslo: 146761-69-5 |
Viz také
Reference
- ^ „Glaxo Wellcome dobrovolně stažený Raxar (Grepafloxacin)“ (PDF). Citováno 2014-10-12.
- ^ „Odstoupení od smlouvy: RAXAR (grepafloxacin HCl) 600 mg tablety, 400 mg tablety a 200 mg tablety“. US Food and Drug Administration. Citováno 2014-10-12.
- ^ Sprandel, KA .; Rodvold, KA. (2003). "Bezpečnost a snášenlivost fluorochinolonů". Clin základní kámen. Suppl 3: S29–36. doi:10.1016 / s1098-3597 (03) 90027-5. PMID 14992418.
- ^ Chodosh S, Lakshminarayan S, Swarz H, Breisch S (leden 1998). „Účinnost a bezpečnost 10denní léčby 400 nebo 600 miligramů grepafloxacinu jednou denně pro léčbu akutních bakteriálních exacerbací chronické bronchitidy: srovnání s 10denní kúrou 500 miligramů ciprofloxacinu dvakrát denně“. Antimicrob. Agenti Chemother. 42 (1): 114–20. doi:10.1128 / AAC.42.1.114. PMC 105465. PMID 9449270.
- ^ Langan CE, Cranfield R, Breisch S, Pettit R (prosinec 1997). „Randomizovaná, dvojitě zaslepená studie grepafloxacinu versus amoxycilinu u pacientů s akutní bakteriální exacerbací chronické bronchitidy“. J. Antimicrob. Chemother. 40 Suppl A: 63–72. doi:10.1093 / jac / 40.suppl_1.63. PMID 9484875. Citováno 2014-10-12.
- ^ Langan CE, Zuck P, Vogel F, McIvor A, Peirzchala W, Smakal M, Staley H, Marr C (říjen 1999). „Randomizovaná, dvojitě zaslepená studie krátkodobého (5denního) grepafloxacinu versus 10denního klarithromycinu u pacientů s akutní bakteriální exacerbací chronické bronchitidy“. J. Antimicrob. Chemother. 44 (4): 515–23. doi:10.1093 / jac / 44.4.515. PMID 10588313. Citováno 2014-10-12.
- ^ O'Doherty B, Holanďan DA, Pettit R, Maroli A (prosinec 1997). „Randomizovaná, dvojitě zaslepená, srovnávací studie s grepafloxacinem a amoxycilinem v léčbě pacientů s komunitně získanou pneumonií“. J. Antimicrob. Chemother. 40 Suppl A: 73–81. doi:10.1093 / jac / 40.suppl_1.73. PMID 9484876. Citováno 2014-10-12.
- ^ Felmingham D (březen 2000). „Respirační patogeny: hodnocení vzorců rezistence v Evropě a potenciální role grepafloxacinu jako léčby pacientů s infekcemi způsobenými těmito organismy“. J. Antimicrob. Chemother. 45 (90002): 1–8. doi:10.1093 / jac / 45.suppl_2.1. PMID 10719006. Citováno 2014-10-12.
- ^ Ridgway GL, Salman H, Robbins MJ, Dencer C, Felmingham D (prosinec 1997). „In vitro aktivita grepafloxacinu proti Chlamydia spp., Mycoplasma spp., Ureaplasma urealyticum a Legionella spp.“. J. Antimicrob. Chemother. 40 Suppl A: 31–4. doi:10.1093 / jac / 40.suppl_1.31. PMID 9484871. Citováno 2014-10-12.
- ^ McCormack WM, Martin DH, Hook EW, Jones RB (1998). „Denní perorální podání grepafloxacinu vs. perorální doxycyklin dvakrát denně při léčbě endocervikální infekce Chlamydia trachomatis“. Infect Dis Obstet Gynecol. 6 (3): 109–15. doi:10.1155 / S1064744998000210. PMC 1784789. PMID 9785106.
- ^ Hagen, S.E .; Domagala, J. M .; Heifetz, C. L .; Johnson, J. (1991). "Syntéza a biologická aktivita 5-alkyl-1,7,8-trisubstituovaných-6-fluorchinolin-3-karboxylových kyselin". Journal of Medicinal Chemistry. 34 (3): 1155–61. doi:10.1021 / jm00107a040. PMID 2002456.
- ^ WO 8906649; eidem, US patent 4 920 120 (1989, 1990, Warner-Lambert).
- ^ Hagen, S.E .; Domagala, J. M. (1990). "Syntéza 5-methyl-4-oxochinolinkarboxylových kyselin". Journal of Heterocyclic Chemistry. 27 (6): 1609. doi:10,1002 / jhet. 5570270616.