Kyselina skořicová - Cinnamic acid - Wikipedia
 | |
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC (2E) -3-fenylprop-2-enová kyselina | |
| Ostatní jména Kyselina skořicová trans-Kyselina skořicová Kyselina fenylakrylová[1] Kyselina skořicová Kyselina 3-fenylakrylová (E) - Kyselina skořicová Kyselina benzenpropenová Kyselina isoskořicová | |
| Identifikátory | |
3D model (JSmol ) | |
| 3DMet | |
| 1905952 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.004.908 |
| Číslo ES |
|
| 3731 | |
| KEGG | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C9H8Ó2 | |
| Molární hmotnost | 148.161 g · mol−1 |
| Vzhled | Bílé monoklinické krystaly |
| Zápach | Zlato[2] |
| Hustota | 1,2475 g / cm3[3] |
| Bod tání | 133 ° C (271 ° F; 406 K)[3] |
| Bod varu | 300 ° C (572 ° F; 573 K)[3] |
| 500 mg / l[3] | |
| Kyselost (strK.A) | 4.44 |
| −7.836×10−5 cm3/ mol | |
| Nebezpečí | |
| Piktogramy GHS |  |
| Signální slovo GHS | Varování |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 | |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | > 100 ° C (212 ° F; 373 K)[3] |
| Související sloučeniny | |
Související sloučeniny | Kyselina benzoová, Kyselina fenyloctová, Kyselina fenylpropanová |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Kyselina skořicová je organická sloučenina se vzorcem C6H5 CH = CHCOOH. Je to bílá krystalická sloučenina, která je mírně rozpustný ve vodě a snadno rozpustný v mnoha organických rozpouštědlech.[4] Klasifikováno jako nenasycené karboxylová kyselina, vyskytuje se přirozeně v řadě rostlin. Existuje jako a cis a a trans izomer, ačkoli druhý je častější.[5]
Výskyt a výroba
Biosyntéza
Kyselina skořicová je ústředním meziproduktem v biosyntéze mnoha přírodních produktů včetně lignolů (prekurzorů lignin a lignocelulóza ), flavonoidy, isoflavonoidy, kumariny, aurony, stilbeny, katechin, a fenylpropanoidy. Své biosyntéza zahrnuje akci enzym fenylalanin amoniak-lyáza (PAL) zapnuto fenylalanin.[6]
Přirozený výskyt
Získává se z oleje z skořice nebo z balzámy jako Storax.[4] To je také nalezené v bambucké máslo. Kyselina skořicová má a Miláček - jako zápach;[2] a jeho těkavější ethylester (ethylcinamát ) jsou aromatické složky v éterickém oleji z skořice, ve kterém souvisí cinnamaldehyd je hlavní složkou.
Syntéza
Kyselina skořicová byla nejprve syntetizována bazicky katalyzovanou kondenzací acetylchlorid a benzaldehyd, následován hydrolýza z chlorid kyseliny produkt.[5] V roce 1890 Rainer Ludwig Claisen popsal syntézu ethylcinamát prostřednictvím reakce ethylacetát s benzaldehydem v přítomnosti sodík jako základna.[7] Další způsob přípravy kyseliny skořicové je Knoevenagelova kondenzace reakce.[8] Reaktanty pro to jsou benzaldehyd a kyselina mallonová v přítomnosti slabé báze, následované kyselinou katalyzovanou dekarboxylace. Může být také připraven oxidací cinnamaldehyd, kondenzace benzalchlorid a octan sodný (následuje kyselá hydrolýza) a Perkinova reakce. Nejstarší komerčně používaná cesta ke kyselině skořicové zahrnuje Perkinova reakce, který je uveden v následujícím schématu[5]
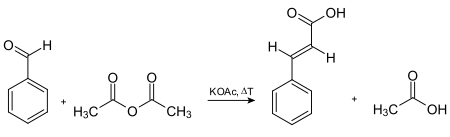 Syntéza kyseliny skořicové prostřednictvím Perkinova reakce.[9]
Syntéza kyseliny skořicové prostřednictvím Perkinova reakce.[9]
Použití
Kyselina skořicová se používá v aromatech, syntetické indigo a jisté léčiva. Hlavní použití je jako předzvěst výroby methylcinamát, ethylcinamát, a benzylcinamát pro parfémový průmysl.[4] Kyselina skořicová je předchůdcem sladidla aspartam pomocí aminace katalyzované enzymem fenylalanin.[5] Kyselina skořicová může dimerizovat v nepolárních rozpouštědlech, což vede k různým lineární volné energetické vztahy.[10]
Reference
- ^ . Encyklopedie Britannica. 6 (11. vydání). 1911. str. 376.
- ^ A b "Kyselina skořicová". flavornet.org.
- ^ A b C d E Záznam v databázi látek GESTIS Institut pro bezpečnost a ochranu zdraví při práci
- ^ A b C Budavari, Susan, ed. (1996), Merck Index: Encyclopedia of Chemicals, Drugs, and Biologicals (12. vydání), Merck, ISBN 0911910123
- ^ A b C d Garbe, Dorothea (2012). "Kyselina skořicová". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a07_099.
- ^ Vogt, T. (2010). „Biosyntéza fenylpropanoidů“. Molekulární rostlina. 3 (1): 2–20. doi:10,1093 / mp / ssp106. PMID 20035037.
- ^ Claisen, L. (1890). „Zur Darstellung der Zimmtsäure und ihrer Homologen“ [O přípravě kyseliny skořicové a jejích homologů]. Berichte der Deutschen Chemischen Gesellschaft. 23: 976–978. doi:10.1002 / cber.189002301156.
- ^ Tieze, L. (1988). Reakce a syntéza v laboratoři organické chemie. Mill Vall, CA. p. 1988.
- ^ F. K. Thayer (1925). „Kyselina m-nitrocinamová“. Organické syntézy. 5: 83. doi:10.15227 / orgsyn.005.0083.
- ^ Bradley, J.-C .; Abraham, M. H .; Acree, W. E .; Lang, A .; Beck, S. N .; Bulger, D. A .; Clark, E. A .; Condron, L. N .; Costa, S. T .; Curtin, E. M .; Kurtu, S. B .; Mangir, M. I .; McBride, M. J. (2015). "Stanovení deskriptorů rozpuštěných látek podle Abrahama pro monomerní a dimerní formy trans-skořicová kyselina pomocí změřených rozpustností z Open Notebook Science Challenge ". Centrální žurnál chemie. 9: 11. doi:10.1186 / s13065-015-0080-9. PMC 4369286. PMID 25798191.


