COPII - COPII
| Sec23 homolog A | |||||||
|---|---|---|---|---|---|---|---|
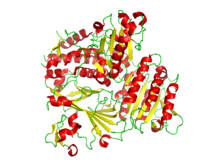 Ribbonový diagram krystalografické struktury COPII heterodimeru Sec23 a Sec24. Alfa šroubovice jsou v červené barvě a beta listy jsou žluté.[1] | |||||||
| Identifikátory | |||||||
| Symbol | SEC23A | ||||||
| Gen NCBI | 856311 | ||||||
| HGNC | 10701 | ||||||
| OMIM | 610511 | ||||||
| PDB | 1M2V | ||||||
| RefSeq | NM_006364 | ||||||
| UniProt | Q15436 | ||||||
| Další údaje | |||||||
| Místo | Chr. 14 q21.1 | ||||||
| |||||||
| Rodina SEC24, člen A | |||||||
|---|---|---|---|---|---|---|---|
| Identifikátory | |||||||
| Symbol | SEC24A | ||||||
| Gen NCBI | 10802 | ||||||
| HGNC | 10703 | ||||||
| OMIM | 607183 | ||||||
| PDB | 1M2V | ||||||
| RefSeq | XM_001132082 | ||||||
| UniProt | O95486 | ||||||
| Další údaje | |||||||
| Místo | Chr. 5 q31.1 | ||||||
| |||||||
COPII je coatomer, typ váček obalový protein, který transportuje bílkoviny z hrubé endoplazmatické retikulum do Golgiho aparát.[2][3] Tento proces se nazývá anterográdní doprava, na rozdíl od retrográdní doprava spojené s COPI protein. Název "COPII" odkazuje na konkrétní cona pkomplex proteinů, který iniciuje nadějný proces. Plášť se skládá z velkých proteinových subkomplexů, které jsou vyrobeny ze čtyř různých proteinových podjednotek.
Obalové proteiny
Plášť COPII se skládá z pěti proteinů: Sar1, Sec23, Sec24, Sec13, a Sec31.[4]Tyto proteiny dimerizují za vzniku větších proteinových komplexů:
Je důležité si uvědomit, že existuje pět různých typů proteinů, které tvoří plášť COPII, ale více proteinů stejné odrůdy tvoří proteinové komplexy kritické pro tvorbu pláště COPII.
Tyto obalové proteiny jsou nezbytné, ale nedostatečné k nasměrování nebo ukotvení vezikuly ke správné cílové membráně. SNARE pro tyto procesy je také zapotřebí náklad a další bílkoviny.
Nadějný proces
Sestavu vezikul COPII lze shrnout jako:
- Sar1-GDP interaguje s transmembránovým proteinem ER Sec12.
- Sar1-GTP rekrutuje krycí protein Sec23 / Sec24 a vytváří tak komplex před vznikem.
- Pre-pučící komplex (složený ze Sar1-GTP vázaného na Sec23 / 24) rekrutuje Sec13 / Sec31, který tvoří druhou vrstvu nátěru.
- Komplex Sec13 / Sec31 tvoří vnější plášť podobný kleci (podobný tvorbě Clathrin vezikuly).
Sar1p je GTPáza který funguje jako „přepínač“, který se otáčí mezi aktivovanou membránou zalitou formou vázanou na GTP a neaktivní rozpustnou formou vázanou na GDP.[5] Neaktivní Sar1p vázaný na GDP je přitahován k cytosolické straně endoplazmatického retikula.
Sec12, transmembránový protein nacházející se v ER, působí jako a Guaninový nukleotidový výměnný faktor stimulací uvolňování HDP, aby se umožnilo navázání GTP v Sar1.
Sar1p vázaný na GTP prochází konformační změnou, která vystavuje N-koncovou amfipatickou a-šroubovici (jiné zdroje uvádějí hydrofobní ocas), která má být vložena do membrány ER. Membránou vázaný Sar1p rekrutuje komplex Sec23p / 24p, aby vytvořil něco, co je souhrnně známé jako pre-pučící komplex. Sec23 / Sec24 se specificky váže na specifické třídicí signály v cytosolických doménách membránového nákladního proteinu, tyto třídicí signály nesdílejí jednoduchý signální motiv jako KDEL nebo KKXX. Nedávný výzkum naznačuje, že více signálů exportu ER spolupracuje na oddělení a vyloučení nesestaveného nákladu.[4]
Pre-pučící komplex (složený ze Sar1-GTP a Sec23 / 24) rekrutuje flexibilní komplex Sec13p / 31p, který se vyznačuje polymerací komplexu Sec13 / 31 s dalšími komplexy Sec13 / 31 za vzniku cuboctahedron se širší mřížkou než je jeho Clathrin analog vezikul. Tvorba cuboctahedronu deformuje membránu ER a odděluje vezikuly COPII (vedle proteinů nákladu a v-SNARE) a završuje tak nadějný proces vezikuly COPII.[6]
Bylo zjištěno, že některé proteiny jsou odpovědné za selektivní balení nákladu do vezikul COPII. Novější výzkumy naznačují, že komplex Sec23 / Sec24-Sar1 se podílí na výběru nákladu.[6] Například Erv29p v Saccharomyces cerevisiae bylo shledáno nezbytným pro balení glykosylovaného pro-a-faktoru.[7]
Po vytvoření vezikuly COPII zůstávají obalové proteiny COPII shromážděny, aby umožnily interakci komplexu Sec23 / Sec24 s vazebným faktorem na membráně Cis-Golgi. Když je vezikul COPII v těsné blízkosti membrány Cis-Golgi, zbavuje se pláště a komponenty se recyklují, aby fungovaly pro další vezikul.
Konformační změny
CopII má tři specifická vazebná místa, z nichž každé může být komplexováno. Sousední obrázek (Sed5) používá k propojení komplex Sec22 t-SNARE. Tento web je silněji vázán, a proto je více upřednostňován. (Embo)
- Krystalové struktury CopII
Viz také
Reference
- ^ PDB: 3EH1; Mancias JD, Goldberg J (listopad 2008). „Strukturní základ diskriminace proteinů z membrány nákladu lidským plášťovým strojem COPII“. EMBO J.. 27 (21): 2918–28. doi:10.1038 / emboj.2008.208. PMC 2580787. PMID 18843296.
- ^ Lee MC, Miller EA (srpen 2007). "Molekulární mechanismy tvorby vezikul COPII". Semin. Cell Dev. Biol. 18 (4): 424–34. doi:10.1016 / j.semcdb.2007.06.007. PMID 17686639.
- ^ Hughes H, Stephens DJ (únor 2008). „Sestavení, organizace a funkce kabátu COPII“. Histochem. Cell Biol. 129 (2): 129–51. doi:10.1007 / s00418-007-0363-x. PMC 2228377. PMID 18060556.
- ^ A b D'Arcangelo, Jennifer G .; Stahmer, Kyle R .; Miller, Elizabeth A. (listopad 2013). „Export zprostředkovaný vezikulemi z ER: funkce a regulace srsti COPII“. Biochimica et Biophysica Acta (BBA) - výzkum molekulárních buněk. 1833 (11): 2464–2472. doi:10.1016 / j.bbamcr.2013.02.003. PMC 3676692. PMID 23419775.
- ^ Bonifacino JS, Glick BS (leden 2004). "Mechanismy pučení a fúze váčků". Buňka. 116 (2): 153–66. doi:10.1016 / s0092-8674 (03) 01079-1. PMID 14744428. S2CID 1777139.
- ^ A b Fath S, Mancias JD, Bi X, Goldberg J (červen 2007). "Struktura a organizace obalových proteinů v kleci COPII". Buňka. 129 (7): 1325–36. doi:10.1016 / j.cell.2007.05.036. PMID 17604721. S2CID 10692166.
- ^ Belden WJ, Barlowe C (listopad 2001). "Role Erv29p při sběru rozpustných sekrečních proteinů do transportních vezikul odvozených od ER". Věda. 294 (5546): 1528–31. doi:10.1126 / science.1065224. PMID 11711675. S2CID 29870942.
- ^ A b 1 PCX; 1PD0; Mossessova E, Bickford LC, Goldberg J (srpen 2003). "SNARE selektivita kabátu COPII". Buňka. 114 (4): 483–95. doi:10.1016 / S0092-8674 (03) 00608-1. PMID 12941276. S2CID 11379372.


