Anidulafungin - Anidulafungin
 | |
| Klinické údaje | |
|---|---|
| Výslovnost | /eɪˌnɪdjʊləˈFʌndʒɪn/ ay-NID-yuu-lə-ZÁBAVA-jin |
| Obchodní názvy | Eraxis, Ecalta |
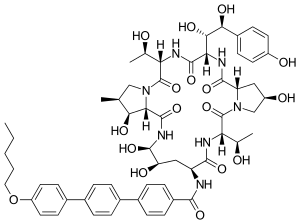
| Ostatní jména | (4R,5S) -4,5-dihydroxy-N2- [[4 '' - (pentyloxy) -p-terfenyl-4-yl] karbonyl] -L-ornithyl-L-threonyl-trans-4-hydroxy-L-prolyl- (S) -4-hydroxy-4- (p-hydroxyfenyl) -L-threonyl-L-threonyl- (3S,4S) -3-hydroxy-4-methyl-L-prolin cyklický (6 → 1) -peptid[1] 1-[(4R,5R) -4,5-dihydroxy-N2- [[4 '' - (pentyloxy) [1 ', 1': 4 ', 1' '- terfenyl] -4-yl] karbonyl] -L-ornithin] echinokandin B[2] |
| AHFS /Drugs.com | Monografie |
| Licenční údaje |
|
| Těhotenství kategorie |
|
| Trasy z správa | Intravenózní |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Biologická dostupnost | 100% (pouze intravenózní podání) |
| Vazba na bílkoviny | Rozsáhlé (> 99%) |
| Metabolismus | Jaterní metabolismus nebyl pozorován, CYP systém není zapojen |
| Odstranění poločas rozpadu | 27 hodin; 40–50 hodin (terminál) |
| Vylučování | Výkaly (~30%), moč (<1%) |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.184.856 |
| Chemické a fyzikální údaje | |
| Vzorec | C58H73N7Ó17 |
| Molární hmotnost | 1140.254 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| | |
Anidulafungin (HOSPODA )[1]:42 (obchodní názvy Eraxis, Ecalta) je polosyntetický echinokandin používá se jako antifungální lék. Dříve to bylo známé jako LY303366.[3][4][5] Může mít také použití při léčbě invazivních Aspergillus infekce při použití v kombinaci s Vorikonazolem.[6] Je členem třídy antifungálních léků známých jako echinokandiny; jeho mechanismus účinku je inhibicí (1 → 3) -β-D-lukan syntáza, enzym důležitý pro syntézu buněčné stěny hub.[7]
Indikace
- Kandidémie a další formy invazivní Candida infekce (nitrobřišní absces a zánět pobřišnice )
- Kandidóza jícnu
Anidulafungin nebyl studován u endokarditida, osteomyelitida, a meningitida kvůli Candida, a nebyl dostatečně studován neutropenický pacientů k určení účinnosti v této skupině.[2]
Farmakodynamika a farmakokinetika
Anidulafungin se významně liší od ostatních antimykotik tím, že v těle prochází chemickou degradací na neaktivní formy pH a teplota. Protože se nespoléhá na enzymatickou degradaci nebo jaterní nebo ledvinovou exkreci, je bezpečné použití tohoto léčiva u pacientů s jakýmkoli stupněm poškození jater nebo ledvin.[8]
Objem distribuce: 30–50 l.
Anidulafungin není evidentně metabolizován játra. Tento specifický lék podléhá pomalé chemii hydrolýza na peptid s otevřeným kruhem, který postrádá antifungální aktivitu. Poločas rozpadu léku je 27 hodin. Asi 30% se vylučuje stolicí (10% jako nezměněné léčivo). Méně než 1% se vylučuje močí.[9][10][11]
Mechanismus účinku
Anidulafungin inhibuje glukan syntáza, enzym důležitý při tvorbě (1 → 3) -β-D-glukan, hlavní složka buněčné stěny hub. Glukansyntáza není přítomna v savčích buňkách, takže je atraktivním cílem antifungální aktivity.[12]
Polosyntéza
Anidulafungin se vyrábí polosyntézou. Výchozí materiál je echinokandin B. (A lipopeptid fermentační produkt z Aspergillus nidulans nebo blízce příbuzný druh, A. rugulosus), který prochází deacylací (štěpením linoleoyl postranní řetězec) působením deacylázového enzymu z bakterie Actinoplanes utahensis;[13] ve třech následujících syntetických krocích, zahrnujících chemickou reacylaci, antifungální lék anidulafungin[12][14] je syntetizován.
Dějiny
Anidulafungin byl původně objeven v laboratořích Lilly Turnerem a Debonem a licencován společnosti Vicuron Pharmaceuticals, která jej předložila FDA.[15] Pfizer získala droga při akvizici společnosti Vicuron na podzim roku 2005.[16] Pfizer získal souhlas Úřad pro kontrolu potravin a léčiv (FDA) 21. února 2006.[17]
Reference
- ^ A b „Mezinárodní nechráněné názvy farmaceutických látek (INN). Doporučené mezinárodní nechráněné názvy: Seznam 43“ (PDF). Světová zdravotnická organizace. 2000. Citováno 11. listopadu 2016.
- ^ A b "Eraxis (anidulafungin) pro injekce, pro intravenózní podání. Úplné informace o předepisování". Roerig (divize společnosti Pfizer, Inc.), New York, NY 10017. Citováno 11. listopadu 2016.
- ^ Krause DS, Reinhardt J, Vazquez JA, Reboli A, Goldstein BP, Wible M, Henkel T (2004). „Fáze 2, randomizovaná studie rozsahu dávek hodnotící bezpečnost a účinnost anidulafunginu při invazivní kandidóze a kandidémii“. Antimikrobní látky Chemother. 48 (6): 2021–4. doi:10.1128 / AAC.48.6.2021-2024.2004. PMC 415613. PMID 15155194.
- ^ Pfaller MA, Boyken L, Hollis RJ, Messer SA, Tendolkar S, Diekema DJ (2005). „In vitro aktivity anidulafunginu proti více než 2 500 klinickým izolátům Candida spp., Včetně 315 izolátů rezistentních na flukonazol“. J Clin Microbiol. 43 (11): 5425–7. doi:10.1128 / JCM.43.11.5425-5427.2005. PMC 1287823. PMID 16272464.
- ^ Pfaller MA, Diekema DJ, Boyken L, Messer SA, Tendolkar S, Hollis RJ, Goldstein BP (2005). „Účinnost anidulafunginu při eradikaci druhů Candida při invazivní kandidóze“. Antimikrobní látky Chemother. 49 (11): 4795–7. doi:10.1128 / AAC.49.11.4795-4797.2005. PMC 1280139. PMID 16251335.
- ^ Grau, Santiago; Azanza, Jose Ramon; Ruiz, Isabel; Vallejo, Carlos; Mensa, Josep; Maertens, Johan; Heinz, Werner J .; Barrueta, Jon Andoni; Peral, Carmen (01.01.2017). „Analýza efektivity nákladů kombinované antifungální léčby vorikonazolem a anidulafunginem versus monoterapie vorikonazolem pro primární léčbu invazivní aspergilózy ve Španělsku“. ClinicoEconomics and Outcomes Research. 9: 39–47. doi:10.2147 / CEOR.S122177. PMC 5221484. PMID 28115858.
- ^ Zida, A .; Bamba, S .; Yacouba, A .; Ouedraogo-Traore, R .; Guiguemdé, R. T. (01.03.2017). „Přírodní produkty Anti-Candida albicans, zdroje nových antifungálních léků: přehled“. Journal de Mycologie Médicale. 27 (1): 1–19. doi:10.1016 / j.mycmed.2016.10.002. ISSN 1773-0449. PMID 27842800.
- ^ „Eraxis at RxList“. 2009-06-24. Citováno 2009-08-01.
- ^ Trissel LA a Ogundele AB, „Kompatibilita anidulafunginu s jinými léky během simulovaného podávání Y-místa“, Am J Health-Sys Pharm, 2005, 62: 834-7.
- ^ Vazquez JA, „Anidulafungin: Nový echinokandin s novým profilem“, Clin Ther, 2005, 27 (6): 657-73.
- ^ Walsh TJ, Anaissie EJ, Denning DW a kol., „Léčba aspergilózy: Pokyny pro klinickou praxi Americké společnosti pro infekční nemoci“, Clin Infect Dis, 2008, 46(3):327-60
- ^ A b Denning DW (1997). „Echinokandiny a pneumokandiny - nová antifungální třída s novým způsobem působení“. J Antimicrob Chemother. 40 (5): 611–614. doi:10.1093 / jac / dkf045. PMID 9421307.
- ^ Lei Shao; Jian Li; Aijuan Liu; Qing Chang; Huimin Lin; Daijie Chen (2013). „Efektivní biokonverze echinokandinu B na jeho jádro nadměrnou expresí deacylázových genů v různých hostitelských kmenech“. Aplikovaná a environmentální mikrobiologie. 79 (4): 1126–1133. doi:10.1128 / AEM.02792-12. PMC 3568618. PMID 23220968.
- ^ „Anidulafungin EMA Europa“ (PDF).
- ^ PRNewswire. Společnost Vicuron Pharmaceuticals podala novou žádost o léčbu (NDA) pro anidulafungin pro léčbu invazivní kandidózy / kandidémie Archivováno 16. května 2012, v Wayback Machine 08-18-2005.
- ^ PRNewswire. Akcionáři společnosti Vicuron Pharmaceuticals schválili fúzi se společností Pfizer Archivováno 16. května 2012, v Wayback Machine 08-15-2005
- ^ „FDA schvaluje novou léčbu plísňových infekcí“. Tisková zpráva FDA. Úřad pro kontrolu potravin a léčiv. 2006-02-21. Archivováno z původního dne 10. července 2009. Citováno 2009-08-01.
