Triazane - Triazane
 | |
| Jména | |
|---|---|
| Systematický název IUPAC Triazane[1] | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| N 3H 5 | |
| Molární hmotnost | 47,0598 g · mol−1 |
| Související sloučeniny | |
jiný anionty | Trifosfan |
Související binární azany | amoniak diazan |
Související sloučeniny | Diazen Triazene Tetrazen |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
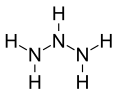
Triazane je anorganická sloučenina s chemický vzorec NH
2NHNH
2 nebo N
3H
5.[2] Triazan je třetí nejjednodušší acyklická látka azan po amoniak a hydrazin. Může být syntetizován z hydrazinu, ale je nestabilní a nelze jej izolovat ve formě volné báze, pouze ve formě solí, jako je triazan-sulfát. Pokusy převést pouze soli triazanu na uvolňování volné báze diazen a amoniak.[3] Triazan byl nejprve syntetizován jako a ligand iontu komplexu stříbra: tris (μ2-triazan-κ2N1,N3) disilver (2+). Triazan byl také syntetizován v amoniakových ledech ozářených elektrony a detekován jako stabilní produkt v plynné fázi po sublimace.[4]
Sloučeniny obsahující triazanovou kostru
Je známo několik sloučenin obsahujících triazanový skelet, včetně 1-methyl-1-nitrosohydrazinu, vyráběného reakcí bez rozpouštědel methylhydrazin a alkylnitrit:
- CN
2H
6 + RNO
2 → CN
3H
5Ó + RHO
1-Methyl-1-nitrosohydrazin je bezbarvá pevná látka, citlivá na nárazy, ale nikoli na tření. Taje při 45 ° C a rozkládá se při 121 ° C.
Reference
- ^ "triazan - PubChem Public Chemical Database". Projekt PubChem. USA: Národní centrum pro biotechnologické informace.
- ^ Zlatá kniha IUPAC
- ^ Wiberg, Holleman a Wiberg. Anorganická chemie. p 627. ISBN 9780123526519
- ^ Forstel, Maksyutenko, Jones, Sun, Chen, Chang a Kaiser. „Detekce nepolapitelné molekuly triazanu ([N
3H
5]) v plynové fázi “, ChemPhysChem, 2015, 16, 3139.
externí odkazy
- L-methyl-l-nitrosohydrazin, ukazuje strukturu 1-methyl-1-nitrosohydrazinu
| Tento anorganické sloučenina –Příbuzný článek je a pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |







