Indolový alkaloid - Indole alkaloid
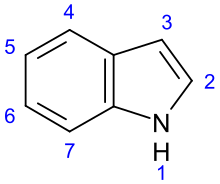
Indolové alkaloidy jsou třídou alkaloidy obsahující a strukturní skupina z indol; mnoho indolových alkaloidů také zahrnuje isopren skupiny a nazývají se tedy terpen indol nebo sekologanin tryptaminové alkaloidy. Obsahuje více než 4 400 známých různých sloučenin a je jednou z největších tříd alkaloidů.[1] Mnoho z nich má významnou fyziologickou aktivitu a některé z nich se používají v medicíně. The aminokyselina tryptofan je biochemické prekurzor indolových alkaloidů.[2]
Dějiny

Působení některých indolových alkaloidů je známé již věky. Aztékové použil psilocybinové houby které obsahují alkaloidy psilocybin a psilocin. Kvetoucí rostlina Rauvolfia serpentina který obsahuje reserpine byl běžný lék v Indie kolem roku 1000 před naším letopočtem. Afričané používali kořeny trvalka deštný prales keř Iboga, které obsahují ibogain jako stimulant. Infuze Calabar fazole Semena byla dána lidem obviněným z trestného činu v roce 2006 Nigérie: jeho odmítnutí žaludkem bylo považováno za známku neviny, jinak byla osoba zabita akcí fyzostigmin, který je v rostlině přítomen a který způsobuje ochrnutí srdce a plic.[3]
Spotřeba žito a související cereálie kontaminován houba Claviceps purpurea příčiny námel otravy a ergotismus u lidí a jiných savců. Vztah mezi námelem a ergotismem byl založen až v roce 1717 a alkaloidem ergotamin, jedna z hlavních účinných látek námele, byla izolována v roce 1918.[4]
První indolový alkaloid, strychnin, byl izolován Pierre Joseph Pelletier a Joseph Bienaimé Caventou v roce 1818 z rostlin rodu Strychnos. Správný strukturní vzorec strychninu byla stanovena až v roce 1947, ačkoli přítomnost indolového jádra ve struktuře strychninu byla stanovena o něco dříve.[5][6] Samotný indol poprvé získal Adolf von Baeyer v roce 1866 při rozkladu Indigo.[7]
Klasifikace
V závislosti na jejich biosyntéze se rozlišují dva typy indolových alkaloidů; isoprenoidy a neizoprenoidy. Mezi tyto patří terpenoidní strukturní prvky, syntetizované živými organismy z dimethylallylpyrofosfát (DMAPP) a / nebo isopentenylpyrofosfát (IPP):[8]
- Neizoprenoid:
- Jednoduché deriváty indol
- Jednoduché deriváty β-karbolin
- Pyrroloindolové alkaloidy
- Indol-3-karbinol
- Kyselina indol-3-octová
- Tryptaminy
- Karbazoly
- Isoprenoid:
- hemiterpenoidy: námelové alkaloidy
- monoterpenoidy.
- Strictosidin
- Catharanthine
- Yohimbin
- Vinca
- Strychnin
- Elipticin
Existují také čistě strukturální klasifikace založené na přítomnosti karbazol, β-karbolin nebo jiné jednotky v uhlíkovém skeletu molekuly alkaloidu.[9] Je známo asi 200 dimerních indolových alkaloidů se dvěma indolovými skupinami.[10]
Neizoprenoidové indolové alkaloidy
Počet známých neizoprenoidových indolových alkaloidů je malý ve srovnání s počtem indolových alkaloidů.[2]
Jednoduché indolové deriváty
Jedním z nejjednodušších a přesto rozšířených indolových derivátů jsou biogenní aminy tryptamin a 5-hydroxytryptamin (serotonin ).[11] Ačkoli jejich přiřazení k alkaloidu není všeobecně přijímáno,[12] oba se nacházejí v rostlinách a zvířatech.[13] Kostra tryptaminu je součástí velké většiny indolových alkaloidů.[14] Například, N,N-dimethyltryptamin (DMT), psilocin a jeho fosforylovaný psilocybin jsou nejjednodušší deriváty tryptaminu.[13] Některé jednoduché indolové alkaloidy neobsahují tryptamin, jako např gram a glykozolin (druhý z nich je derivátem karbazol ).[15] Kamalexin je jednoduchý indolový alkaloid produkovaný rostlinou Arabidopsis thaliana, často používaný jako model pro biologii rostlin.[16]
Jednoduché deriváty β-karbolinu
Prevalence β-karbolin alkaloidy je spojeno se snadnou tvorbou jádra β-karbolinu z tryptaminu v intramolekulární Mannichova reakce. Mezi jednoduché (neizoprenoidové) β-karbolinové deriváty patří harmine, harmalin, harman[17] a trochu složitější struktura kanthinonu.[18] Harmalin byl poprvé izolován v roce 1838 Göbelem[19] a harmine v roce 1848 Fritzche.[20][21][22]
Pyroloindolové alkaloidy
Pyroloindolové alkaloidy tvoří relativně malou skupinu derivátů tryptaminu. Jsou vyráběny společností methylace indolového jádra v poloze 3 a následující nukleofilní adice na atomu uhlíku v polohách 2 s uzavřením ethylaminoskupiny do kruhu. Typickým představitelem této skupiny je fyzostigmin,[23] který byl izolován Jobstem a Hessem v roce 1864.[24][25]
Isoprenoidové indolové alkaloidy

Isoprenoidové indolové alkaloidy zahrnují zbytky tryptofanu nebo tryptaminu a izoprenoidové stavební bloky odvozené od dimethylallylpyrofosfát a isopentenylpyrofosfát.[2]
Ergotové alkaloidy
Ergot alkaloidy jsou třídou hemiterpenoidních indolových alkaloidů souvisejících s kyselina lysergová, který se zase tvoří ve vícestupňových reakcích zahrnujících tryptofan a DMAPP. Mnoho námelových alkaloidů je amidy kyseliny lysergové. Nejjednodušší takový amid je ergin, a složitější lze rozdělit do následujících skupin:[26][27]
- Rozpustné ve vodě aminoalkohol deriváty, jako např ergometrin a jeho izomer ergometrinin
- Ve vodě nerozpustný polypeptid deriváty:
- Ergotamin skupina zahrnující ergotamin, ergosin a jejich izomery
- Ergoxin skupiny, včetně ergostinu, ergoptinu, ergoninu a jejich izomerů
- Ergotoxin skupina, včetně ergokristin, α-ergokryptin, β-ergokryptin, ergokornin a jejich izomery.
Ergotinin, objevený v roce 1875, a ergotoxin (1906) byly následně prokázány jako směs několika alkaloidů. V čisté formě první námelové alkaloidy, ergotamin a jeho izomer ergotaminin byly izolovány Arthurem Stollem v roce 1918.[27]
Monoterpenoidové indoly alkaloidy nebo secologanin tryptaminové alkaloidy
Většina monoterpenoidních alkaloidů obsahuje 9 nebo 10 uhlíkový fragment (na obrázku tučně) (pocházející z secologanin ) a konfigurace umožňuje seskupení do Corynanthe, Iboga a Aspidosperma třídy. Monoterpenoidní část jejich uhlíkových koster je ilustrována níže na příkladu alkaloidů ajmalicinu a kataranthinu. Atomy uhlíku v kroužku chybí v alkaloidech, které obsahují C9 fragment místo C10.[14]
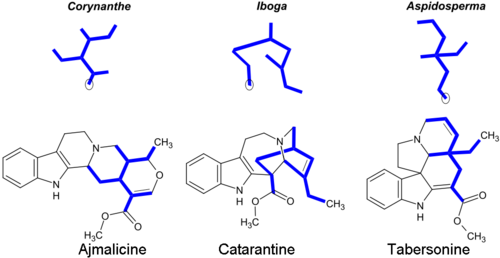
Corynanthe alkaloidy zahrnují nezměněnou kostru secologaninu, který je modifikován v Iboga a Aspidosperma alkaloidy.[28] Některé reprezentativní monoterpenoidní indolové alkaloidy:[5][29][30]
| Typ | Počet atomů uhlíku v monoterpenoidním fragmentu | |
|---|---|---|
| C9 | C10 | |
| Corynanthe | Ajmaline, aquamycin, strychnin, brucine | Ajmalicin, yohimbin, reserpine, sarpagin, mitragynin |
| Iboga | Ibogain, ibogamin | Voacangine, katarantin |
| Aspidosperma | Eburnamin | Tabersonin, vindolin, vinkamin |
V rostlině je také malá skupina alkaloidů Aristotelia - asi 30 sloučenin, z nichž nejdůležitější je peduncularine - které obsahují monoterpenoid C10 část nepocházející ze secologaninu.[31]
Bisindole alkaloidy
Dimery derivátů strictosidinu, volně nazývané bisindoly, ale komplikovanější než to. Je známo více než 200 dimerních indolových alkaloidů. Produkují se v živých organismech dimerizací monomerních indolových bází v následujících reakcích:[32]
- Mannichova reakce (voacamine)
- Michaelova reakce (villalstonine)
- Kondenzace z aldehydy s aminy (toxiferin, calebassine)
- Oxidační kopulace tryptaminů (kalikantin);
- Rozdělení funkční skupiny jednoho z monomerů (vinblastin, vinkristin ).
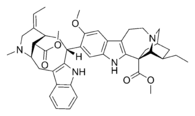 |  |  |  |
| Voacamine | Villalstonine | Toxiferin | Vinblastin |
Kromě bisindolových alkaloidů existují dimerní alkaloidy, které se tvoří dimerizací indolového monomeru s jiným typem alkaloidu. Příkladem je tubulosin sestávající z indolu a isochinolin fragmenty.[33]
Distribuce v přírodě
Rostliny, které jsou bohaté na neizoprenoidové indolové alkaloidy, zahrnují harmonický (Peganum harmala), který obsahuje harman, harmin a harmalin, a Calabar fazole (Physostigma venenosum) obsahující fyzostigmin.[34] Někteří členové rodiny Svlačec obecný, zejména Ipomoea violacea a Turbina corymbosa obsahují ergoliny a lysergamidy.[35] Navzdory značné strukturální rozmanitosti je většina monoterpenoidních indolových alkaloidů lokalizována ve třech rodinách dvouděložný rostliny: Apocynaceae (rody Alstonia, Aspidosperma, Rauvolfia a Catharanthus ), Rubiaceae (Corynanthe ) a Loganiaceae (Strychnos ).[36][37]
Indolové alkaloidy jsou také přítomny v houbách. Například, psilocybinové houby obsahuje deriváty tryptaminu a Claviceps obsahuje deriváty kyseliny lysergové.[34] Kůže mnoha druhů ropuchy rodu Bufo obsahuje derivát tryptaminu, bufotenin a kůže a jed tohoto druhu Bufo alvarius (Ropucha Colorado ) obsahuje 5-MeO-DMT.[38] Serotonin, což je důležité neurotransmiter u savců lze také přičíst jednoduchým indolovým alkaloidům.[39]

Harmal obsahuje β-karbolinové alkaloidy

Ipomoea violacea obsahuje ergoliny

Alstonia macrophylla obsahuje Corynanthe alkaloidy

Rauvolfia serpentina obsahuje Corynanthe alkaloidy

Catharanthus roseus obsahuje monoterpenoidové indolové alkaloidy

Psilocybe cubensis obsahuje psilocybin a psilocin
Ergot obsahuje ergoliny

Ropucha Colorado (Bufo alvarius) obsahuje bufotenin a 5-MeO-DMT

Tabernaemontana divaricata obsahuje indolové alkaloidy včetně katarantin, conophylline, ibogamin, tabersonine a voacristin[40]
Biosyntéza
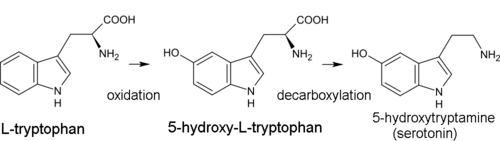
Biogenetickým prekurzorem všech indolových alkaloidů je aminokyselina tryptofan. U většiny z nich je první krok syntézy dekarboxylace tryptofanu tryptamin. Dimethyltryptamin (DMT) je tvořen z tryptaminu methylace za účasti koenzym z S-adenosyl methionin (SAM). Psilocin je produkován spontánní defosforylací psilocybin.[41]
Při biosyntéze serotoninu není meziproduktem tryptamin, ale 5-hydroxytryptofan, který je zase dekarboxylován za vzniku 5-hydroxytryptaminu (serotoninu).[13]
Biosyntéza β-karbolin alkaloidy nastávají tvorbou Schiffova základna z tryptaminu a aldehyd (nebo keto kyselina ) a následné intramolekulární Mannichova reakce, kde atom uhlíku C (2) indolu slouží jako a nukleofil. Poté aromatičnost se obnovuje ztrátou protonu na atomu C (2). Výsledná kostra tetrahydro-p-karbolinu pak postupně oxiduje na dihydro-p-karbolin a p-karbolin. Při tvorbě jednoduchých β-karbolinových alkaloidů, jako je harmin a harmalin, kyselina pyrohroznová působí jako kyselina keto. Při syntéze monoterpenoidových indolových alkaloidů secologanin hraje roli aldehydu. Pirroloindolové alkaloidy jsou syntetizovány v živých organismech podobným způsobem.[42]

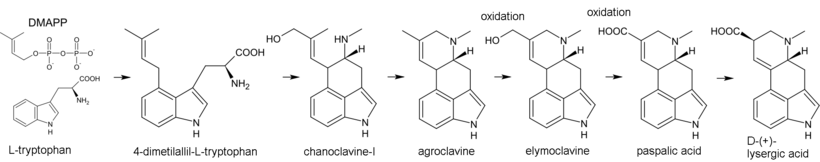
Biosyntéza námelových alkaloidů začíná alkylací tryptofanu pomocí dimethylallylpyrofosfát (DMAPP), kde atom uhlíku C (4) v indolovém jádru hraje roli nukleofilu. Výsledný 4-dimethylallyl-L-tryptofan podléhá N-methylaci. Dalšími produkty biosyntézy jsou chanoklavin-I a agroclavin - ten je hydroxylován na elymoklavin, který zase oxiduje na kyselina paspalová. V procesu alylového přesmyku se kyselina paspalová přeměňuje na kyselinu lysergovou.[43]
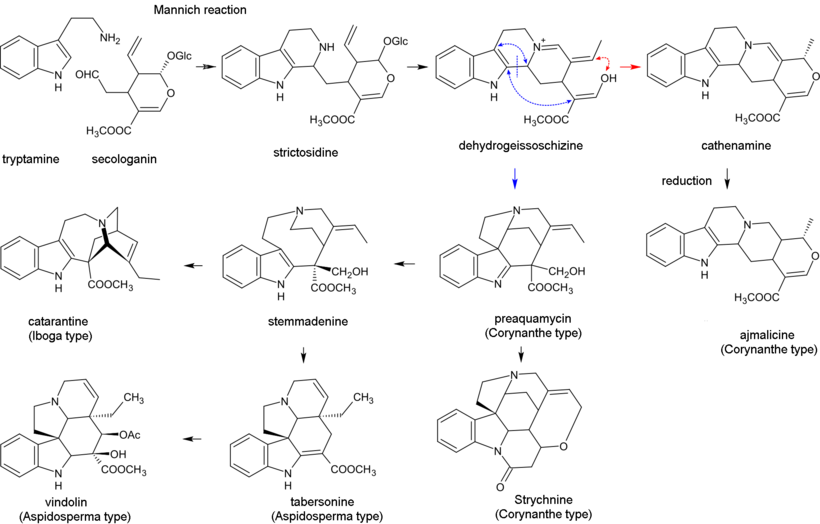
Biosyntéza monoterpenoidních indolových alkaloidů začíná Mannichovou reakcí tryptaminu a secologaninu; dává se strictosidin který se převede na 4,21-dehydrogeissoschizin. Poté biosyntéza většiny alkaloidů obsahujících nerušenou monoterpenoidní část (Corynanthe typu) probíhá cyklizací s tvorbou katenaminu a následnou redukcí na ajmalicin za přítomnosti nikotinamid adenin dinukleotid fosfát (NADPH). V biosyntéze jiných alkaloidů, 4,21-dehydrogeissoschizin nejprve převede na preakuammicin (alkaloid podtypu strychnos, typ Corynanthe), z něhož vznikají další alkaloidy podtypu strychnos a typů Iboga a Aspidosperma. Bisindolové alkaloidy vinblastin a vinkristin jsou produkovány při reakci zahrnující kataranthin (alkaloid typu Iboga) a vindolin (typ Aspidosperma).[29][44]
Fyziologická aktivita

Indolové alkaloidy působí na centrální a obvodový nervové systémy. Kromě toho ukazují bisindolové alkaloidy vinblastin a vinkristin antineoplastický účinek.[45]
Kvůli strukturálním podobnostem se serotoninem může mnoho tryptaminů interagovat se serotoninem 5-HT receptory.[46] Hlavní účinek serotonergní psychedelika jako LSD, DMT, a psilocybin souvisí s jejich bytím agonisté z 5-HT2A receptory.[47][48] Naproti tomu gramin je antagonista 5-HT2A receptor.[49]
Ergoliny, jako kyselina lysergová, zahrnují strukturní prvky tryptaminu i fenyletylamin a tím působit na celou skupinu 5-HT receptorů, adrenoreceptory (většinou typu α) a dopaminové receptory (většinou typu D2).[50][51] Tak ergotamin je částečný agonista α-adrenergních a 5-HT2 receptory, a tedy zužuje se cév a stimuluje zúžení děloha. Dihydroergotamin je selektivnější vůči α-adrenergním receptorům a má slabší účinek na serotoninové receptory. Ergometrin je agonista a-adrenergního 5-HT2 a částečně D2 receptory.[51][52] Ve srovnání s jinými námelovými alkaloidy má ergometrin větší selektivitu při stimulaci dělohy.[52] LSD, polosyntetický psychedelický ergolin, je agonista 5-HT2A, 5-HT1A a v menší míře D2 receptory a má silný psychedelický účinek.[53][54]
Některé monoterpenoidní indolové alkaloidy také interagují s adrenoreceptory. Například ajmalicin je selektivní antagonista α1-adrenergní receptory, a proto má antihypertenzní akce.[55][56] Yohimbin je selektivnější k α2 adrenoreceptor;[56] blokováním presynaptického α2-adrenoceptory, zvyšuje uvolňování norepinefrin čímž se zvyšuje krevní tlak. Yohimbin byl použit k léčbě erektilní dysfunkce u mužů až do vzniku účinnějších léků.[57]
Některé alkaloidy ovlivňují obrat monoaminů nepřímo. Harmin a harmalin jsou tedy reverzibilní selektivní inhibitory monoaminooxidázy-A.[58] Reserpine snižuje koncentraci monoaminů v presynaptických a synaptický neurony, čímž vyvolává antihypertenzní a antipsychotické účinky.[55]
Některé indolové alkaloidy interagují s jinými typy receptorů. Mitragynin je agonista μ-opioidní receptor.[30] Harmal alkaloidy jsou antagonisty vůči GABAA-receptor,[59] a ibogain - do NMDA receptory.[60] Fyzostigmin je reverzibilní inhibitor acetylcholinesterázy.[61]

Aplikace
Rostliny a houby, které obsahují indolové alkaloidy, mají dlouhou historii použití v tradiční medicína. Rauvolfia serpentina, který obsahuje jako účinnou látku reserpin, se v roce 2006 používal více než 3000 let Indie léčit hadí kousnutí a šílenství.[62] Ve středověké Evropě jsou výtažky z námel byly použity v lékařský potrat.[63]
Později byly rostliny spojeny čistými přípravky indolových alkaloidů. Reserpine byl druhý (po chlorpromazin ) antipsychotikum lék; Vykazoval však relativně slabé působení a silné vedlejší účinky a pro tento účel se již nepoužívá.[64] Místo toho je předepsán jako antihypertenzivum, často v kombinaci s jinými látkami.[65]
Jiné léky, které ovlivňují kardiovaskulární systém zahrnout ajmaline, což je antiarytmikum třídy I,[66] a ajmalicin, který se v Evropě používá jako antihypertenzivum.[55] Fyzostigmin - inhibitor acetylcholinesterázy - a jeho syntetické analogy se používají při léčbě glaukom, Alzheimerova choroba (rivastigmin ) a myastenie (neostigmin, pyridostigmin, distigmin ).[67] Ergotové alkaloidy ergometrin (ergobazin, ergonovin), ergotamin a jejich syntetické deriváty (methylergometrin ) se aplikují proti děložnímu krvácení,[68] a bisindolové alkaloidy vinblastin a vinkristin jsou protinádorová činidla.[69]
Studie na zvířatech to ukázaly ibogain má potenciál v léčbě heroin, kokain, a alkohol závislosti, která je spojena s antagonismem ibogainu vůči NMDA receptory. Léčebnému použití ibogainu brání jeho právní status, protože je v mnoha zemích zakázán jako silná psychedelická droga s nebezpečnými důsledky předávkování. Nicméně nelegální síť v Evropa a Spojené státy poskytují ibogain pro léčbu drogové závislosti.[70][71]

Od starověku se jako rostliny používaly rostliny obsahující indolové alkaloidy psychedelické léky. The Aztékové použitý a Lidé Mazatec nadále používat psilocybinové houby a psychoaktivní semena ranní sláva druhy jako Ipomoea tricolor.[72] Amazonské kmeny používají psychedelickou infuzi, ayahuasca, vyrobeno z Psychotria viridis a Banisteriopsis caapi.[73] Psychotria viridis obsahuje psychedelickou drogu DMT, zatímco Banisteriopsis caapi obsahuje harmala alkaloidy, které fungují jako inhibitory monoaminooxidázy. Předpokládá se, že hlavní funkcí harmala alkaloidů v ayahuasce je prevence metabolizace DMT v zažívací trakt a játra, takže může překročit hematoencefalická bariéra zatímco přímý účinek harmala alkaloidů na centrální nervový systém je minimální.[74] Jed z Ropucha Colorado, Bufo alvarius, může užívat jako psychedelická droga, její aktivní složky jsou 5-MeO-DMT a bufotenin.[75] Jeden z nejběžnějších rekreační psychedelické léky, LSD, je polosyntetický ergoline (který obsahuje indolovou část).[76]
Reference
- ^ David S. Seigler (2001). Sekundární metabolismus rostlin. Springer. p. 628. ISBN 0-412-01981-7.
- ^ A b C I. L. Knunyants (1988). Chemická encyklopedie. Sovětská encyklopedie. p. 623.
- ^ Dewick, str. 348–367.
- ^ Hesse, str. 333–335.
- ^ A b Hesse, str. 316.
- ^ Orekhov, str. 616
- ^ L. Elderfild (1954). Heterocyklické sloučeniny. 3. Moskva. p. 5..
- ^ Dewick, str. 346–376.
- ^ Hesse, s. 14–30.
- ^ Hesse, str. 91–92.
- ^ Hesse, str. 15
- ^ Leland J. Cseke; et al. (2006). Přírodní produkty z rostlin. Druhé vydání. CRC. p. 30. ISBN 0-8493-2976-0.
- ^ A b C Dewick, str. 347
- ^ A b Dewick, str. 350.
- ^ Hesse, str. 16.
- ^ Glawischnig (2007). „Camalexin“. Fytochemie. 68 (4): 401–406. doi:10.1016 / j.phytochem.2006.12.005.
- ^ Dewick, str. 349
- ^ Hesse, str. 22
- ^ Goebel, o. (1838). „Ueber das Harmalin“. Annalen der Chemie (v němčině). 38 (3): 363–366. doi:10,1002 / jlac.18410380318.
- ^ Orekhov, str. 565.
- ^ Fritzche, J. (1848). „Untersuchungen über die Samen von Peganum Harmala“. Journal für Praktische Chemie (v němčině). 43: 144–155. doi:10.1002 / prac.18480430114.
- ^ „Bestandtheile der Samen von Peganum harmala“. Annalen der Chemie (v němčině). 64 (3): 360–369. 1848. doi:10,1002 / jlac.18480640353.
- ^ Dewick, str. 365–366
- ^ Jobst, J .; Hesse, O. (1864). „Ueber die Bohne von Calabar“ (PDF). Annalen der Chemie (v němčině). 129 (1): 115–121. doi:10,1002 / jlac.18641290114.
- ^ Goldfrank, Lewis R. a Flomenbaum, Neal Goldfrankovy toxikologické mimořádné události, McGraw-Hill Professional, 2006 ISBN 0-07-147914-7 p. 794.
- ^ Dewick, str. 370–372.
- ^ A b Orekhov, str. 627.
- ^ Dewick, str. 351
- ^ A b Dewick, str. 350–359
- ^ A b Hiromitsu Takayama (2004). „Chemie a farmakologie analgetických indolových alkaloidů z rostliny Rubiaceous, Mitragyna speciosa". Chemický a farmaceutický bulletin. 52 (8): 916–928. doi:10,1248 / cpb.52,916. PMID 15304982. Archivovány od originál 4. března 2009.
- ^ Hesse, str. 30
- ^ Hesse, str. 91–105
- ^ Hesse, str. 99
- ^ A b Waksmundzka, str. 625–626
- ^ Tadeusz Aniszewski (2007). Alkaloidy - tajemství života. Amsterdam: Elsevier. p. 39. ISBN 978-0-444-52736-3.
- ^ Waksmundzka, s. 626
- ^ Tadeusz Aniszewski (2007). Alkaloidy - tajemství života. Amsterdam: Elsevier. 37–39. ISBN 978-0-444-52736-3.
- ^ Michael E. Peterson; Patricia A. Talcott (2005). Toxikologie malých zvířat. Saunders. p. 1086. ISBN 0-7216-0639-3.
- ^ Waksmundzka, s. 625
- ^ Kulshreshtha, Ankita; Saxena, Jyoti (2019). "Alkaloidy a nealkaloidy z Tabernaemontana divaricata" (PDF). International Journal of Research and Review. 6 (8): 517–524.
- ^ Fricke, Janis; Blei, Felix; Hoffmeister, Dirk (25. 09. 2017). "Enzymatická syntéza psilocybinu". Angewandte Chemie International Edition. 56 (40): 12352–12355. doi:10.1002 / anie.201705489. PMID 28763571.
- ^ Dewick, str. 349, 365
- ^ Dewick, str. 369–370
- ^ Tadhg P. Begley (2009). Encyclopedia of Chemical Biology. Wiley. str. 5–7. ISBN 978-0-471-75477-0.
- ^ Dewick, str. 356
- ^ Richard A. Glennon (2006). „Strategie pro rozvoj selektivních serotonergních látek“. Serotoninové receptory. Od molekulární farmakologie k humánním terapeutikům. Humana Press. p. 96. ISBN 1-58829-568-0.
- ^ Richard A. Glennon (2008). „Neurobiologie halucinogenů“. American Psychiatric Publishing učebnice léčby zneužíváním návykových látek. Americké psychiatrické nakladatelství. p. 183. ISBN 978-1-58562-276-4.
- ^ Alper, str. 8
- ^ Froldi Guglielmina; Silvestrin Barbara; Dorigo Paola; Caparrotta Laura (2004). „Gramine: a vasorelaxing alkaloid působící na 5-HT2A receptory“. Planta Medica. 70 (4): 373–375. doi:10.1055 / s-2004-818953. PMID 15095157.
- ^ Dewick, str. 374–375
- ^ A b B. T. Larson; et al. (1995). „Ergovalinová vazba a aktivace D2 dopaminových receptorů v GH4ZR7 Buňky ". Journal of Animal Science. 73 (5): 1396–1400. doi:10,2527 / 1995,7351396x. PMID 7665369.
- ^ A b Bertram G. Katzung (2009). Základní a klinická farmakologie. McGraw-Hill Medical. p. 272. ISBN 978-0-07-160405-5.
- ^ Torsten Passie; et al. (2008). „Farmakologie diethylamidu kyseliny lysergové: recenze“ (PDF). CNS Neuroscience & Therapeutics. 14 (4): 295–314. doi:10.1111 / j.1755-5949.2008.00059.x. PMC 6494066. PMID 19040555.
- ^ Seeman, P. (2004). „Komentář k“ Různá psychotomimetika působí prostřednictvím společné signální cesty"". Věda. 305 (5681): 180c. doi:10.1126 / science.1096072. PMID 15247457.
- ^ A b C Dewick, str. 353
- ^ A b Demichel, P; Gomond, P; Roquebert, J (1982). "alfa-adrenoreceptor blokující vlastnosti raubasinu u dýkovaných krys". J. Pharmacol. 77 (3): 449–454. doi:10.1111 / j.1476-5381.1982.tb09317.x. PMC 2044614. PMID 6128043.
- ^ Bertram G. Katzung (2009). Základní a klinická farmakologie. McGraw-Hill Medical. p. 145. ISBN 978-0-07-160405-5.
- ^ Andreas Moser (1998). Farmakologie endogenních neurotoxinů: příručka. Braun-Brumfield. p. 138. ISBN 3-7643-3993-4.
- ^ Andreas Moser (1998). Farmakologie endogenních neurotoxinů: příručka. Braun-Brumfield. p. 131. ISBN 3-7643-3993-4.
- ^ Alper, str. 7
- ^ Dewick, str. 367
- ^ Dewick, str. 352
- ^ Hesse, str. 332–333
- ^ Alan F. Schatzberg; Charles B. Nemeroff (2009). Americká psychiatrická publikační učebnice psychofarmakologie. Americké psychiatrické nakladatelství. p. 533. ISBN 978-1-58562-309-9.
- ^ Симпатолитики (v Rusku).
- ^ Антиаритмические средства (v Rusku).
- ^ Dewick, str. 367–368
- ^ Утеротоники [(Uterotonika)] (v ruštině).
- ^ "Противоопухолевые средства растительного происхождения (protinádorové látky v rostlinách)" (v Rusku).
- ^ Alper, s. 2–19
- ^ Dewick, str. 357
- ^ Dewick, str. 348
- ^ Christina Pratt (2007) Encyclopedia of Shamanism Volume 1, The Rosen Publishing Group, ISBN 1-4042-1140-3 p. 310
- ^ Jordi Riba; et al. (2003). „Human Pharmacology of Ayahuasca: Subjective and Cardiovascular Effects, Monoamine Metabolite Excression, and Pharmacokinetics“. Journal of Pharmacology and Experimental Therapeutics. 306 (1): 73–83. doi:10.1124 / jpet.103.049882. PMID 12660312.
- ^ NA. Weil; W. Davis (1994). "Bufo alvarius: silný halucinogen živočišného původu “. Journal of Ethnopharmacology. 41 (1–2): 1–8. doi:10.1016/0378-8741(94)90051-5. PMID 8170151.
- ^ Dewick, str. 376
Bibliografie
- Alper, Kenneth R (2001). „Ibogaine: recenze“. Alkaloidy. Akademický tisk. ISBN 0-12-053206-9.
- Dewick, Paul M (2002). Léčivé přírodní produkty. Biosyntetický přístup. Druhé vydání. Wiley. ISBN 0-471-49640-5.
- Hesse, Manfred (2002). Alkaloidy. Přírodní kletba nebo požehnání. Wiley-VCH. ISBN 978-3-906390-24-6.
- Orekhov AP (1955). Chemické alkaloidy (2. vyd.). M .: SSSR.
- Waksmundzka-Hajnos, Monika; Sherma, Joseph; Kowalska, Teresa (2008). Tenkovrstvá chromatografie ve fytochemii. CRC Press. ISBN 978-1-4200-4677-9.















