Disulfid rhenia - Rhenium disulfide
 | |
| Jména | |
|---|---|
| Název IUPAC Bis (sulfanyliden) rhenium | |
| Ostatní jména Sulfid rhenia (IV) | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.031.695 |
| Číslo ES |
|
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| ReS2 | |
| Molární hmotnost | 250,337 g / mol[1] |
| Zápach | bez zápachu |
| Hustota | 7,6 g / cm3[1] |
| nerozpustný | |
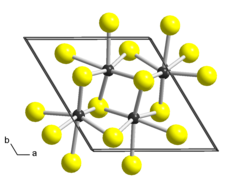
| Struktura | |
| Triclinic, aP12, vesmírná skupina P1, Č. 2[2] | |
A = 0,6455 nm, b = 0,6362 nm, C = 0,6401 nm a = 91,60 °, p = 105,04 °, y = 118,97 ° | |
Jednotky vzorce (Z) | 4 |
| Související sloučeniny | |
jiný anionty | Oxid rhenia (IV) Rhenium diselenid Ditellurid rhenia |
jiný kationty | Mangan diselenid |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Disulfid rhenia je anorganická sloučenina z rhenium a síra se vzorcem ReS2. Má vrstvenou strukturu, kde jsou atomy silně vázány v každé vrstvě. Vrstvy drží pohromadě slabé Van der Waalsovy dluhopisy a lze jej snadno odloupnout od sypkého materiálu.
Výroba
ReS2 se v přírodě vyskytuje jako minearl rheniite.[3] Může být syntetizován z reakce mezi rheniem a sírou při 1000 ° C nebo z rozkladu sulfid rhenium (VII) při 1100 ° C:[4]
- Re + 2 S → ReS2
- Re2S7 → 2 ReS2 + 3 S.
Nanostrukturovaný ReS2 lze obvykle dosáhnout mechanickým odlupováním, chemická depozice par (CVD) a chemické a kapalné exfoliace. Větší krystaly lze pěstovat pomocí toku tekutého uhličitanu za vysokého tlaku. Je široce používán v elektronických a optoelektronických zařízeních, skladování energie, fotokatalytických a elektrokatalytických reakcích.[5]
Vlastnosti
Jedná se o dvourozměrnou (2D) skupinu VII dichalkogenid přechodného kovu (TMD). ReS2 byla v roce 2014 poprvé izolována na monovrstvy, což je tloušťka pouze jedné jednotkové buňky.[6] Tyto monovrstvy vykazovaly elektrické, optické a vibrační vlastnosti nezávislé na vrstvě, které se výrazně lišily od ostatních TMD.
Reference
- ^ A b Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92. vydání). Boca Raton, FL: CRC Press. str. 4,84. ISBN 1439855110.
- ^ Wildervanck, J.C .; Jellinek, F (1971). "Dichalkogenidy technecia a rhenia". Journal of the Less Common Metals. 24: 73–81. doi:10.1016/0022-5088(71)90168-8.
- ^ Rheniite, MinDat.org, vyvoláno 2020-07-17
- ^ Brauer, Georg (1981). Handbuch der Präparativen Anorganischen Chemie. Pásmo III (v němčině) (3. vyd.). Stuttgart: Ferdinand Enke. str. 1619. ISBN 3-432-87823-0.
- ^ Rahman, Mohammad; Davey, Kenneth; Qiao, Shi-Zhang (2017). „Příchod 2D disulfidu rhenia (ReS2): základy aplikací“ (PDF). Pokročilé funkční materiály. 27 (10): 1606129. doi:10.1002 / adfm.201606129. hdl:2440/103880.
- ^ Tongay, Sefaattin; Sahin, Hasan; Ko, Changhyun; Luce, Alex; Ventilátor, Wen; Liu, Kai; Zhou, Jian; Huang, Ying-Sheng; Ho, Ching-Hwa; Yan, Jinyuan; Ogletree, D. Frank; Aloni, Shaul; Ji, Jie; Li, Shushen; Li, Jingbo; Peeters, F. M .; Wu, Junqiao (2014). "Chování monovrstvy hromadně ReS2 díky elektronickému a vibračnímu oddělení “. Příroda komunikace. 5. doi:10.1038 / ncomms4252. PMID 24500082.
