Základní octan berylnatý - Basic beryllium acetate
 | |
| Jména | |
|---|---|
| Systematický název IUPAC Hexakis (μ-acetato) -μ (sup 4) -oxotetraberyllium | |
| Ostatní jména Oxyacetát berylnatý Acetát oxidu berylnatého | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.038.881 |
| Číslo ES |
|
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| Vlastnosti | |
| C 12H 18Být 4Ó 13 | |
| Molární hmotnost | 406,3122 g / mol |
| Vzhled | bezbarvý |
| Bod tání | 285 ° C (545 ° F; 558 K) |
| Bod varu | 330 ° C (626 ° F; 603 K) |
| Rozpustnost v chloroformu | rozpustný |
| Nebezpečí | |
| Hlavní nebezpečí | vysoce toxický |
| NIOSH (Limity expozice USA pro zdraví): | |
PEL (Dovolený) | PEL 0,002 mg / m3 C 0,005 mg / m3 (30 minut), s maximem maxima 0,025 mg / m3 (jako Be)[1] |
REL (Doporučeno) | Ca C 0,0005 mg / m3 (jako Be)[1] |
IDLH (Okamžité nebezpečí) | Ca [4 mg / m3 (jako Be)][1] |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Základní octan berylnatý je chemická sloučenina se vzorcem Be4O (O.2CCH3)6. Tento sloučenina zaujímá charakteristickou strukturu, ale nemá žádné aplikace a byl jen mírně prozkoumán. Je to bezbarvá pevná látka, která je rozpustná v organických rozpouštědlech.
Příprava
Může být připraven zpracováním základní uhličitan berylnatý s horkým octová kyselina.
- 2 Být
2CO
3(ACH)
2 + 6 AcOH → Být
4O (AcO)
6 + 5 H
2Ó + 2 CO
2
Základní octan berylnatý je nerozpustný ve vodě, ale rozpustný v chloroform, v souladu s tím, že je nepolární. Taje a sublimuje ve vakuu bez rozkladu.[2]
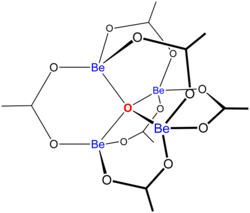
Struktura
"Základní acetáty „sestávají ze souboru kovových center vázaných na iont centrálního oxidu a sbírky acetátu ligandy. Základní octan berylnatý má čtyřboký Be4Ó6+ jádro s octany (CH3CO2−) překlenující každou z dvojic Be2+ centra.[3][4] Skládá se ze vzájemně propojeného šestičlenného Be2Ó3C kroužky. Struktura je relevantní pro svou značnou stabilitu (sloučenina je destilovatelná při 330 ° C).
Použití
Rozpustnost soli v organických rozpouštědlech (chloroform) je užitečná pro extrakci a čištění frakcí bohatých na berylium pro mnoho účelů. Jednoduché monokrystaly octanu berylnatého lze snadno pěstovat a jsou užitečné pro srovnání rentgenových difraktometrů a také jako reference v krystalografii proteinů .
Viz také
- Základní octan zinečnatý - izostrukturální
Reference
- ^ A b C NIOSH Kapesní průvodce chemickými nebezpečími. "#0054". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ Moeller, T. (1950). "Základní deriváty berylia z organických kyselin". In Audrieth, L. F. (ed.). Anorganic Syntheses, svazek 3. John Wiley & Sons. str. 4. doi:10.1002 / 9780470132340.ch2. ISBN 978-0-470-13234-0.
- ^ Bragg W. H. (1923). "Krystalová struktura základního octanu berylnatého". Příroda. 111 (2790): 532. Bibcode:1923Natur.111..532B. doi:10.1038 / 111532a0.
- ^ Pauling, L .; Sherman, J. (1934). „Struktura karboxylové skupiny. II. Krystalová struktura základního octanu berylnatého“ (PDF). Sborník Národní akademie věd. 20 (6): 340. Bibcode:1934PNAS ... 20..340P. doi:10.1073 / pnas.20.6.340.
Acetylhalogenidy a jejich soli acetát ion | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | On | ||||||||||||||||||
| LiOAc | Být (OAc)2 BeAcOH | B (OAc)3 | AcOAc ROAc | NH4OAc | Ahoj | FAc | Ne | ||||||||||||
| NaOAc | Mg (OAc)2 | Al (OAc)3 ALSOL Al (OAc)2ACH Al2TAK4(OAc)4 | Si | P | S | ClAc | Ar | ||||||||||||
| KOAc | Ca (OAc)2 | Sc (OAc)3 | Ti (OAc)4 | VO (OAc)3 | Cr (OAc)2 Cr (OAc)3 | Mn (OAc)2 Mn (OAc)3 | Fe (OAc)2 Fe (OAc)3 | Co (OAc)2, Co (OAc)3 | Ni (OAc)2 | Cu (OAc)2 | Zn (OAc)2 | Ga (OAc)3 | Ge | Jako (OAc)3 | Se | BrAc | Kr | ||
| RbOAc | Sr (OAc)2 | Y (OAc)3 | Zr (OAc)4 | Pozn | Mo (OAc)2 | Tc | Ru (OAc)2 Ru (OAc)3 Ru (OAc)4 | Rh2(OAc)4 | Pd (OAc)2 | AgOAc | Cd (OAc)2 | v | Sn (OAc)2 Sn (OAc)4 | Sb (OAc)3 | Te | IAc | Xe | ||
| CsOAc | Ba (OAc)2 | Hf | Ta | Ž | Re | Os | Ir | Pt (OAc)2 | Au | Hg2(OAc)2, Hg (OAc)2 | TlOAc Tl (OAc)3 | Pb (OAc)2 Pb (OAc)4 | Bi (OAc)3 | Po | Na | Rn | |||
| Fr. | Ra | Rf | Db | Sg | Bh | Hs | Mt. | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| La (OAc)3 | Ce (OAc)X | Pr | Nd | Odpoledne | Sm (OAc)3 | EU (OAc)3 | Gd (OAc)3 | Tb | Dy (OAc)3 | Ho (OAc)3 | Er | Tm | Yb (OAc)3 | Lu (OAc)3 | |||||
| Ac | Čt | Pa | UO2(OAc)2 | Np | Pu | Dopoledne | Cm | Bk | Srov | Es | Fm | Md | Ne | Lr | |||||
