Antroponotické onemocnění - Anthroponotic disease
Zvrátit zoonóza, také známý jako zooantroponóza, a někdy antroponóza (Řecký zoon "zvíře", antropos "muž", nosos "nemoc "), odkazuje na patogeny rezervováno v lidé které lze přenést na jiné nečlověka zvířata.[1]
Terminologie
Antroponóza se týká patogenů pocházejících z člověka a může zahrnovat přenos z člověka na člověka a na člověka, ale také na člověka a člověka. Termín zoonóza technicky označuje nemoc přenášenou mezi jakýmkoli zvířetem a jiným zvířetem, člověkem nebo člověkem, bez uvážení, a byla také definována jako nemoc přenášená ze zvířat na člověka a naopak.[1] Přesto kvůli lékařským předsudkům zaměřeným na člověka má zoonóza tendenci se používat stejným způsobem jako antropozoonóza, která konkrétně odkazuje na patogeny rezervované u zvířat jiných než lidských, které jsou přenosné na člověka.[1]
Další zmatek kvůli četnosti vědců, kteří používají „antropozoonózu“ a „zooantroponózu“ zaměnitelně, byl vyřešen během kloubu z roku 1967 Potraviny a zemědělství a Světová zdravotnická organizace schůze výboru, která doporučila použití „zoonózy“ k popisu obousměrné výměny infekčních patogenů mezi zvířaty a lidmi.[2][1]
Navíc, protože lidé jsou zřídka v přímém kontaktu s divokými zvířaty a zavádějí patogeny prostřednictvím „měkkého kontaktu“, je třeba zavést pojem „sapronotické látky“. Sapronózy (řecky sapros „rozpadající se“) odkazuje na lidské nemoci, které skrývají schopnost růst a replikovat se (nejen přežít nebo kontaminovat) abiotický prostředí, jako je půda, voda, rozpadající se rostliny, zvířecí mrtvoly, výkaly a další substráty.[1] Kromě toho lze sapro-zoonózy charakterizovat tak, že mají jak živého hostitele, tak místo vývoje organických látek, půdy nebo rostlin bez vývoje zvířat.[1] Je třeba poznamenat, že obligátní intracelulární paraziti, kteří se nemohou replikovat mimo buňky a jsou zcela reprodukčně závislí na vstupu do buňky, aby mohli využívat intracelulární zdroje, jako jsou viry, rickettsie, chlamydie a Cryptosporidium parvum, nemohou být sapronotickými látkami.[1]
Etymologické nástrahy
Kategorizace nemoci do epidemiologických tříd podle předpokládaného zdroje infekce nebo směru přenosu vyvolává řadu rozporů, které by bylo možné vyřešit použitím cyklických modelů, jak ukazují následující scénáře:
Zoonóza vs. zvrátit zoonózu vs. antroponóza
V případě nemocí přenesených z členovec vektory například městské žlutá zimnice, dengue, epidemický tyfus, relapsující horečka přenášená klíšťaty, horečka zika, a malárie,[1] rozlišení mezi pojmy se stává stále nejasnějším. Například člověka nakaženého malárií kousne komár, který je následně také nakažen. Toto je případ reverzní zoonózy (člověk na zvíře). Nově infikovaný komár však poté infikuje dalšího člověka. Může se jednat o případ zoonózy (zvíře na člověka), pokud je komár považován za původní zdroj, nebo antroponózy (člověk na člověka), pokud je člověk považován za původní zdroj. Pokud by tento infikovaný komár infikoval primáta jiného než lidského původu, mohlo by to být považováno za případ reverzní zoonózy / zooantroponózy (člověk na zvíře), pokud je člověk považován za primární zdroj, nebo jednoduše zoonózy (zvíře na zvíře), pokud je komár považován primární zdroj.
Zoonóza vs. antroponóza
Podobně, HIV pocházející z opic (crossover kvůli lidem konzumujícím divočinu šimpanz bushmeat ) a chřipka A viry pocházející z ptáci (crossover kvůli antigennímu posunu) mohl být zpočátku považován za zoonotický přenos, protože infekce nejprve pocházely od obratlovců, ale v současné době by mohl být považován za antroponózu kvůli jeho potenciálu přenosu mezi lidmi na člověka.
Sapronóza vs. sapro-zoonóza
Typickými příklady sapronotických činidel jsou houbové látky, jako jsou kokcidioidomykóza, histoplazmóza, aspergilóza, kryptokokóza, Microsporum gypseum. Některé mohou být bakteriální z sporulující klostridium a bacil Rhodococcus equi, Burkholderia pseudomallei, Listeria, Erysipelothrix, Yersinia pseudotuberculosis, legionelóza, horečka Pontiac, a netuberkulózní mykobakteriózy. Ostatní sapronotické látky jsou amebické jako v primárních amebická meningoencefalitida. V případě sporulujících bakterií, jejichž infekční spory se produkují až po významném období neaktivity, se opět vyskytují potíže s klasifikací. vegetativní růst v abiotickém prostředí, přesto se to stále považuje za případ sapronóz.[1] Případy týkající se zoo-sapronóz Listeria, Erysipelothrix, Yersinia pseudotuberculosis, Burkholderia pseudomallei, a Rhodococcus equi mohou být přenášeny zvířetem nebo abiotickým substrátem, ale obvykle k nim dochází prostřednictvím a fekálně-orální cesta mezi lidmi a jinými zvířaty.[3]
Případy s režimy přenosu
Vektory členovců
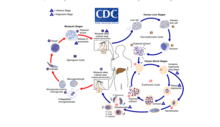
Malárie
Malárie zahrnuje cyklickou infekci zvířat (lidských i jiných) a komáři z rodu Anopheles s řadou Plasmodium druh. Parazit Plasmodium se přenáší na komára, který se živí krví infikovaného zvířete, načež začíná sporogenní cyklus ve střevě komára, který infikuje další zvíře při další krevní moučce. Nezdá se, že by na komáry byly v důsledku parazitární infekce nějaké škodlivé účinky.[4] The Plasmodium brasilianum Parazit, který se běžně vyskytuje u primátů, je morfologicky podobný malárii vyvolávající Plasmodium malariae, která se běžněji vyskytuje u lidí, a sporné je, zda jsou oba tyto druhy skutečně odlišné.[5] Přesto 12 zpráv o malárii na vzdáleném místě původních obyvatel Yanomami společenství venezuelských Amazonka vznikl tam, kde bylo překvapivě zjištěno, že je způsoben kmenem P. brasilianum se 100% identickými sekvencemi nalezenými v Alouatta seniculus mniši.[6] To naznačuje jednoznačnou zoonózu a vysokou možnost zpětného úniku zpět do pásem primátů jiných než lidských jako reverzní zoonózy.

Africká spavá nemoc
Trypanosoma brucei gambiense (T. b. Gambiense) je druh Afričan trypanosomy což jsou prvoky hemoflageláty zodpovědný za trypanosomiáza (více obyčejně známý jako Africká spavá nemoc ) u lidí a jiných zvířat. Protozoa jsou přenášena prostřednictvím Tsetse letí kde se množí a mohou být přeneseny na jiného zvířecího hostitele během krmení mouchy krví.[7] Ohniska spavé nemoci v určitých lidských komunitách byla odstraněna, ale pouze dočasně, protože neustálé opětovné zavádění z neznámých zdrojů statisticky naznačuje přítomnost nehumánního rezervoáru, kde se v patogenezi udržuje únik sylvatic cyklus a znovu zavedeny do městského cyklu.[8] Přítomnost T. b. gambiense byl nalezen samostatně u lidí a hospodářských zvířat. To podnítilo molekulární studii porovnávající sérovou reaktivitu prasata, kozy, a krávy člověku sérum kde jsou patrné podobnosti ve všech vzorcích, zejména však ve vzorcích prasat.[9] Dohromady tyto nálezy implikují reverzní přenos zoonotického člověka na zvíře.
Arboviry

Mezi viry žluté zimnice, viry horečky dengue a viry Zika patří Flavivirus rody a Chikungunya virus je Alfavirus rody. Všechny z nich jsou brány v úvahu arboviry označující jejich schopnost přenášet se prostřednictvím vektorů členovců.[10][11] Sylvatické přenosové cykly pro arboviry v komunitách primátů jiných než člověk mají potenciál přenést se do městského cyklu uvnitř lidí, kde by lidé mohli být slepí hostitelé ve scénářích, kde je eliminováno další prolínání, ale mnohem pravděpodobnější je opětovný výskyt těchto virů do kteréhokoli cyklu kvůli přelévání.[12] Zachování arbovirového městského cyklu mezi lidmi očividně vyžaduje, aby se vyskytla vzácná nebo podceněná konjunkce faktorů. Nastane jedna z následujících situací:
- Infikovaný člověk v městském prostředí živí sylvatické (obvykle vzdáleně umístěné) komáry, jako jsou Haemogogus (který má relativně dlouhou životnost ve srovnání s jinými komáry a může přenášet virus po delší dobu), který infikuje jiného člověka nebo jiného člověka, který bude sloužit jako rezervoár.
- Městský Aedes (běžněji se vyskytují v městských oblastech [13] krmí a přenáší virus na jiné lidské nebo nehumánní zvíře, které bude sloužit jako rezervoár.
- Dostatečný počet komárů vektorových a živočišná nádrž obývají stejnou ekologickou niku v těsném kontaktu, aby podporovaly a udržovaly zoonotický cyklus viru.
- Zvířecí rezervoár viru udržuje vhodnou hladinu viru v krvi, aby umožnil infekci vektorového komára.
- Most-vektor komár, jako je Aedes albopictus, které mohou přežít v městské oblasti a šířit se do venkovských, polo venkovských a lesních oblastí, by mohly virus přenést do sylvatického prostředí.[14]
- Zika horečka: Virus Zika je způsoben jednořetězcová RNA Flavivirus, který používá komár Aedes jako vektor k infikování dalších lidských a zvířecích hostitelů.[15] Kmen viru zika z roku 2015 izolovaný z člověka v Brazílie byl použit k infikování těhotné makaků rhesus intravenózně a uvnitřplodová voda spojenec. Přehrady i přehrady placenty byli infikováni vzorky pozitivní tkáně Zika, které byly zaznamenávány po dobu až 105 dnů. To potvrzuje potenciál reverzního zoonotického přenosu mezi lidmi a subhumánní primáti. [16]
- Žlutá zimnice: Virus žluté zimnice se přenáší také kousnutím infikovaného komára druhu Aedes nebo Haemagogus, který se živí infikovaným zvířetem. Historický průběh Americký obchod s otroky je ukázkovým příkladem zavedení patogenu k vytvoření zcela nového sylvatického cyklu. Předchozí hypotézy o „Nový svět YFV "byli položeni k odpočinku ve studii z roku 2007, která zkoumala míru substituce nukleotidů a divergence k určení, že žlutá zimnice byla do Ameriky zavlečena přibližně před 400 lety od roku západní Afrika. Bylo to také kolem 17. století, kdy byla dokumentována žlutá zimnice Evropany, kteří se podíleli na obchodování s otroky. Skutečný způsob zavedení mohl hrát v řadě scénářů, ať už byl viremický člověk ze Starého světa, nakažený komár ze Starého světa, vejce nakažená komáry infikovaným ze Starého světa, nebo všichni tři byli přepraveni do Ameriky, když viděli, že přenos žluté zimnice nebyl neobvyklé na plachetnicích.[17] Uprostřed novějších ohnisek žluté zimnice v jihovýchodní Brazílii byl vysoce naznačen potenciál přelévání.[18] Molekulární srovnání kmenů ohniska primátů (kromě člověka) se ukázala být více příbuzná lidským kmenům než kmeny odvozené od jiných subhumánních primátů, což naznačuje pokračující reverzní zoonózu.[19]
- Chikungunya: Virus Chikungunya je jednořetězcový RNA alfavirus typicky přenášený komáři Aedes na jiného zvířecího hostitele. Neexistují žádné důkazy, které by naznačovaly překážku pro přepínání hostitelů Chikungunya mezi lidmi a subhumánními primáty, protože u žádného daného druhu primátů nemá žádné preference. Má vysoký potenciál přelévání nebo přelévání zpět do sylmatických cyklů, jako tomu bylo u podobného arboviru, který byl do Ameriky importován během obchodu s otroky.[20] Studie prokázaly, že chikungunya má potenciál orálně infikovat sylvatické druhy komárů včetně Haemagogus leucocelaenus a Aedes terrens. Navíc v a sérologické průzkum prováděný na subhumánních primátech městských a příměstských oblastí města Stát Bahia, 11 zvířat ukázalo chikungunya neutralizující protilátky.[12]
- Horečka dengue: Virus dengue je flavivirus také přenosný virem Aedes vektory komárů jiným hostitelům zvířat. Dengue byl do Ameriky také představen obchodem s otroky spolu s Aedes aegypti.[21] Studie z roku 2009 v Francouzská Guyana zjistili, že infekce virů dengue typů 1 až 4 byly přítomny v různých různých typech virů dengue neotropické les savci jiné než primáti, jako je hlodavci, vačnatci, a netopýři. Po sekvenčních analýzách bylo zjištěno, že 4 kmeny savců jiných než člověk měly index podobnosti 89% až 99% s lidskými kmeny cirkulujícími současně. To potvrzuje, že ostatní savci v okolí mají potenciál být infikováni lidskými zdroji, a naznačuje přítomnost městského cyklu.[22][23] Případ, který dokazuje, že vektory členovců jsou schopné infekce, pochází z Brazílie, kde Aedes albopictus (který často navštěvuje dvorky lidských domů, ale snadno se šíří do venkovského, polo venkovského a divokého prostředí) byl nalezen infikovaný virem dengue 3 v Sao Paulo Stát. Mezitím, ve státě Bahia, sylvatic vektor Haemogogus leucocelaenus bylo zjištěno, že je infikováno virem dengue 1.[24] V jiné studii provedené v Atlantický les Bahia, primáti (Leontopithecus chrysomelas a Sapajus xanthosternos ) byly nalezeny s protilátkami dengue viry 1 a 2, zatímco lenostiBradypus torquatus ) měl protilátky proti viru dengue 3, což naznačuje možnou přítomnost zavedeného sylvatického cyklu.
Divoká zvířata
Velké množství divokých zvířat s přírodními stanovišti, která ještě musí být zasažena lidmi, je stále ovlivněna sapronotickými látkami prostřednictvím kontaminované vody.
Giardia
Podtyp viru chřipky A H1N1
- Těsnění: V roce 1999 byly divoké tuleně přijaty do nizozemského rehabilitačního centra pro tuleně s příznaky podobné chřipce a bylo zjištěno, že byli ve skutečnosti nakaženi člověkem chřipka B jako virus, který obíhal u lidí v roce 1995 a prodělal antigenní posun od adaptace na svého nového hostitele tuleňů.[26]
Tuberkulóza
- Jelen, divočák: V oblastech intenzivního řízení hry, které zahrnovaly oplocení velké zvěře, místa doplňkového krmení a pasoucí se dobytek, byly případy tuberkulóza objevily se léze u divokých jelenů a divočáků. Někteří kanci a jeleni sdíleli stejné kmeny tuberkulózy podobné těm, které se vyskytují u hospodářských zvířat a lidí, což naznačuje možnou sapronotickou nebo sapro-zoonotickou kontaminaci sdílených vodních zdrojů, doplňkového krmiva, přímého kontaktu s lidmi nebo hospodářskými zvířaty nebo jejich vylučování.[27]
Domestikovaná společenská zvířata
E-coli
- Psi, koně: Důkaz infekce člověkem E-coli Byly nalezeny kmeny u několika psů a koní v celé Evropě, což implikuje možnost zoonotického mezispeciálního přenosu multirezistentních kmenů z člověka na společenská zvířata a naopak.[28]
Tuberkulóza
- Pes: A Jorkšírský teriér byl přijat na veterinární kliniku s chronickým kašlem, špatnou retencí hmotnosti a zvracením hlášeným po celé měsíce, kdy vyšlo najevo, že se majitel zotavil z tuberkulózy, ale pes byl původně testován na tuberkulózu negativně ve 2 různých molekulárních testech a byl propuštěn. O 8 dní později byl pes euthanized kvůli obstrukce močové trubice. Kde byla provedena nekroskopie játra a tracheobronchiální lymfatické uzliny vzorky byly ve skutečnosti pozitivně testovány na přesně stejný kmen tuberkulózy, jaký vlastnil dříve. Toto je velmi jasný případ reverzní zoonózy.[29]
Podtyp viru chřipky A H1N1
- Fretky: Fretky se často používají u lidí klinické studie tak byla dříve potvrzena možnost lidské chřipky infikovat je. Potvrzení přirozeného přenosu lidského kmene H1N1 z ohniska fretek pro domácí mazlíčky v roce 2009 však dále zahrnuje přenos z člověka na zvíře.[30]
COVID-19
Uprostřed globálního roku 2020 pandemický z COVID-19 Citlivost koček, fretek, psů, kuřata, prasata a kachny do SARS-CoV-2 koronavirus byl zkoumán a bylo zjištěno, že to může být replikováno u koček a fretek se smrtelnými výsledky.
- Kočky: Virus může být přenášen ve vzduchu mezi kočkami. Virový RNA byl detekován ve stolici během 3–5 dnů po infekci a patologické studie detekovaly virovou RNA v měkké patro, mandle, a průdušnice. Koťata získala masivní léze v plicích, nosní a tracheální sliznice epitel. Dohled nad SARS-CoV-2 u koček by měl být považován za doplněk k eliminaci COVID-19 u lidí.[31]
- Fretky: Fretky byly naočkovány virovými kmeny z prostředí Huanan Seafood Market ve Wuhan v Číně a také lidskými izoláty z Wuhan. Bylo zjištěno, že u obou izolátů se virus může replikovat v horních dýchacích cestách fretek až 8 dní, aniž by způsobil onemocnění nebo smrt, a virová RNA byla detekována rektální tampony. Patologické studie provedené po 13 dnech infekce odhalily mírné peribronchitida v plicích, těžká lymfoplazmatická perivaskulitida a vaskulitida mimo jiné onemocnění s protilátka u všech fretek byla detekována produkce proti SARS-CoV-2. Skutečnost, že se SARS-CoV-2 efektivně replikuje v horních cest dýchacích z fretek z nich dělá kandidátský zvířecí model pro hodnocení antivirových léků nebo kandidátů na vakcíny proti COVID-19.[31]
- Psi: Z Beagle u testovaných psů byla virová RNA detekována ve stolici a 50% Beagles, kteří byli naočkováni sérokonverze po 14 dnech, zatímco zbývajících 50% zůstalo seronegativní vykazující nízkou citlivost na SARS-CoV-2 u psů.[31]
- Kuře, kachna, prase: U kuřat, kachen nebo prasat nebyly žádné důkazy citlivosti, přičemž všechny výtěry virové RNA vykazovaly negativní výsledky a séronegativní po 14 dnech po inokulaci.[31]
Domestikovaná hospodářská zvířata
Podtyp viru chřipky A H1N1
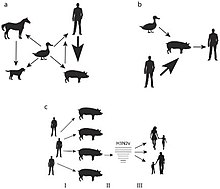
- Krůty: A Norština stádo chovatelů krůt vykazovalo pokles produkce vajec bez dalších klinické příznaky poté, co ruka farmy uvedla, že H1N1. Studie odhalila, že krůty měly také H1N1 a byly séropozitivní na jeho antigeny. Mateřské protilátky H1N1 byly detekovány ve vaječných žloutcích a další genetické analýzy odhalily identický kmen H1N1 u krůt jako zemědělský pracovník, který pravděpodobně infikoval krůty během umělé oplodnění.[32]
- Prasata: Přenos H1N1 z člověka na prase byl hlášen v Kanadě,[33] Korea,[34] a nakonec během vypuknutí roku 2009 zahrnoval každý kontinent kromě Antarktidy.[35] Bylo také známo, že se šíří během sezónních epidemií v roce Francie mezi lidmi a prasaty.[36]
Staphylococcus aureus rezistentní na meticilin
- Koně: 11 koňský Vystavovali pacienti přijatí do veterinární nemocnice z různých důvodů z různých farem po dobu přibližně jednoho roku MRSA infekce později. Vzhledem k tomu, že izoláty MRSA jsou u koní extrémně vzácné, bylo navrženo, že k propuknutí MRSA došlo nozokomiální infekce pocházející z člověka během pobytu koně v nemocnici.[37]
- Krávy, krůty, prasata: Byl navržen případ reverzní zoonózy, který vysvětluje, jak konkrétní člověk Meticilin Citlivý kmen Streptococcus Aureus byl nalezen u hospodářských zvířat (prasata, krůty, krávy) nejen se ztrátou člověka virulentní geny (což by mohlo snížit zoonotický potenciál pro lidskou kolonizaci), ale také přidání rezistence na methicilin a a tetracyklin (což zvýší výskyt infekcí MRSA). Obava je zde příliš velká používání antibiotik u hospodářských zvířat inscenace umocňují tvorbu románu odolný vůči antibiotikům zoonotický patogeny.[38]
Divoká zvířata v zajetí
Tuberkulóza
- Sloni: V roce 1996, The Hawthorne Cirkus Společnost uvedla, že ukrývají 4 jejich slony a 11 jejich chovatelů M. tuberculosis infekce. Bohužel tito sloni byli dále pronajati různým cirkusovým akcím a zoologickým zahradám po celé Americe. To pobídlo celostátní epidemický, ale protože tuberkulóza není nemoc, která se obvykle přenáší ze zvířat na člověka, bylo navrženo, že epidemie byla způsobena přenosem z lidského manipulátora na zajatého slona.[39]
COVID-19
- Alpaky: Vypuknutí alpaky v roce 2007 koronavirus kvůli vzájemnému prolínání na národní výstavě alpaky vedlo ke srovnání mezi lidskými a alpakovými koronaviry ve snaze odvodit zdroj ohniska. Bylo zjištěno, že koronavirus z alpaky je nejvíce evolučně podobný lidskému kmenu koronavirů, který byl izolován v 60. letech, což naznačuje, že koronavirus z alpaky mohl velmi dobře cirkulovat po celá desetiletí respirační onemocnění ve stádech nezjištěných pro nedostatek diagnostických schopností. Navrhuje také způsob přenosu z člověka na alpaku.[40]
Helmintové a prvoky
- Primáti: Na University of Ibadan Zoologická zahrada v Nigérie, fekální vzorky zookeepers pozitivní test na hlísty (Ancylostoma duodenale, Ascaris lumbricoides a Trichuris trichiura ) a cysty prvoků (Giardia lamblia a Entamoeba histolytica ). Přesně stejný kmen helmintů a cyst prvoků byl nalezen u primátů (kromě člověka) v zoo, což implikovalo zoonózu mezi nimi.[41]
Spalničky
- Nehumánní primáti: V roce 1996, a spalničky k propuknutí došlo ve svatyni u 94 subhumánních primátů. Ačkoli zdroj ohniska nebyl nikdy určen, sérum a moč testování prokázalo, že virus byl určitě spojen s nedávnými případy spalniček v USA[42]
Helicobacter pylori
- Vačnatci: Pruhovaný obličej je Australan vačnatec, který čelil několika vypuknutím Helicobacter pylori v zajetí. Žaludek vzorkování vačnatce odhalilo, že H. pylori kmen odpovědný za ohniska se 100% vyrovnal s kmenem pocházejícím z lidského střevního traktu. Lze tedy předpokládat, že ohnisko bylo způsobeno manipulátory.[43]
Divoká zvířata v chráněných oblastech
- Šimpanzi: Přenos lidského koronaviru (HCoV) OC43 divokým šimpanzům (Pan troglodytes verus ) žijící v Národní park Taï, Pobřeží slonoviny byl hlášen v letech 2016 až 2017. Tito šimpanzi byli zvyklí na lidskou přítomnost, která studovala tyto konkrétní komunity od 80. let [44] HCoV-OC43, patřící k druhu Betacoronavirus 1 (BetaCoV1), obvykle způsobuje epizody nachlazení i n lidí (toto vylučuje SARS a MERS ) lidské koronaviry [45] ale byl také zjištěn v kopytníci, masožravci, a zajícovití.[46] Proto je zcela pravděpodobné, že vědci nebo pytláci mohl nechtěně šířit virus na šimpanze, čímž odhalil další rozhraní v přepínání hostitelů koronaviru.[47]
Rhinovirus C.
- Šimpanzi: Ačkoli byl dříve považován za jedinečně lidský patogen, lidský Rhinovirus C. bylo určeno jako příčina propuknutí respiračních infekcí u šimpanzů v roce 2013 Uganda. Vyšetřování šimpanzů z celé Afriky zjistilo, že vykazují univerzálnost homozygotnost pro 3 CDHR3-Y529 alela (kadherin příbuzný člen rodiny), kterým je a receptor že drasticky zvyšuje náchylnost k infekci rhinovirem C a astma u lidí. Pokud jsou respirační viry lidského původu schopné udržovat cirkulaci u subhumánních primátů, ukázalo by se to škodlivé, pokud by se infekce rozšířila do lidských komunit.[48]
Tuberkulóza
- Sloni: Nekroskopie volně se pohybujícího slona afrického (Loxodonta africana ) v Krugerův národní park v Jižní Afrika nalezeno významné poškození plic v důsledku lidského kmene M. tuberculosis. Sloni zkoumají své okolí svými kmeny, proto to bylo velmi pravděpodobné aerosolizováno zdrojem infekce byly patogeny z domácího odpadu, kontaminovaná voda z lidské komunity proti proudu, lidské výkaly nebo kontaminované potraviny od turistů.[49]
Pneumoviry
- Šimpanzi: V Ugandě zprávy o respiračních virech lidského původu infikovaly dvě komunity šimpanzů (Pan troglodytes schweinfurthii) ve stejném lese. Později bylo zjištěno, že je způsoben člověkem metapneumovirus (také známý jako MPV, Pneumoviridae, Metapneumovirus ) a člověk respirovirus 3 (také známý jako HRV3, Paramyxoviridae, Respirovirus, nebo dříve známý jako virus parainfluenzy 3 ).[50]
Reverzní zoonóza u goril
- Gorily: Chráněné oblasti podléhající ekoturistice v Ugandě, Rwanda a Demokratická republika Kongo „Volně se pohybující gorily si stále častěji zvykají na přítomnost lidí, ať už ve formě průvodců, turistů, stopařů, veterinářů, pytláků nebo výzkumníků. Iodamoeba buetschlii, Giardia lamblia, Chilomastix sp., Endolimax nana, Entamoeba coli, a Entamoeba histolytica byly nalezeny ve výkalech goril a promiskuitních defekací, které po sobě zanechali lidé zasahující do stanoviště. Navíc, zvýšený počet Cryptosporidium sp. a capillaria infekce byly zjištěny u goril, které udržovaly častější kontakt s lidmi, než u těch, které ne. Tyto nálezy společně naznačují výskyt reverzních zoonóz.[51]
Viz také
Reference
- ^ A b C d E F G h i Hubálek Z (březen 2003). „Vznikající lidské infekční nemoci: antroponózy, zoonózy a sapronózy“. Vznikající infekční nemoci. 9 (3): 403–4. doi:10.3201 / eid0903.020208. PMC 2958532. PMID 12643844.
- ^ Zoonózy, Smíšený výbor odborníků FAO / WHO dne; Organizace, světové zdraví; Organizace spojených národů, výživy a zemědělství (1967). Smíšený výbor odborníků FAO / WHO pro zoonózy [zasedání konané v Ženevě od 6. do 12. prosince 1966]: třetí zpráva. Světová zdravotnická organizace. hdl:10665/40679. ISBN 978-92-4-120378-4.
- ^ Tuzio, H; Edwards, D; Elston, T; Jarboe, L; Kudrak, S; Richards, J; Rodan, I (srpen 2005). „Pokyny pro zoonózy koček od Americké asociace praktiků koček“. Journal of Feline Medicine & Surgery. 7 (4): 243–274. doi:10.1016 / j.jfms.2004.11.001. PMID 16130211.
- ^ Prevence, Centra pro kontrolu nemocí CDC a (2019-01-28). „CDC - Malárie - O malárii - Biologie“. www.cdc.gov. Citováno 2020-04-22.
- ^ Ramasamy, Ranjan (2014-08-18). „Zoonotická malárie - globální přehled a výzkum a politické potřeby“. Hranice ve veřejném zdraví. 2: 123. doi:10.3389 / fpubh.2014.00123. ISSN 2296-2565. PMC 4135302. PMID 25184118.
- ^ Lalremruata, Albert; Magris, Magda; Vivas-Martínez, Sarai; Koehler, Maike; Esen, Meral; Kempaiah, Prakasha; Jeyaraj, Sankarganesh; Perkins, Douglas Jay; Mordmüller, Benjamin; Metzger, Wolfram G. (září 2015). „Přirozená infekce Plasmodium brasilianum u lidí: Člověk a opice sdílejí parazity quartanu s malárií ve venezuelské Amazonii“. EBioMedicine. 2 (9): 1186–1192. doi:10.1016 / j.ebiom.2015.07.033. ISSN 2352-3964. PMC 4588399. PMID 26501116.
- ^ „CDC - africká trypanosomiáza - biologie“. www.cdc.gov. 2019-06-12. Citováno 2020-04-22.
- ^ Funk, Sebastian; Nishiura, Hiroshi; Heesterbeek, Hans; Edmunds, W. John; Checchi, Francesco (2013-01-17). „Identifikace přenosových cyklů na rozhraní člověk-zvíře: role zvířecích rezervoárů při udržování lidské africké trypanosomiázy Gambiense“. PLOS výpočetní biologie. 9 (1): e1002855. Bibcode:2013PLSCB ... 9E2855F. doi:10.1371 / journal.pcbi.1002855. ISSN 1553-734X. PMC 3547827. PMID 23341760.
- ^ Cordon-Obras, Carlos; Cano, Jorge; González-Pacanowska, Dolores; Benito, Agustin; Navarro, Miguel; Bart, Jean-Mathieu (2013-12-23). „Trypanosoma brucei gambiense Adaptace na různá savčí séra je spojována s VSG expresní stránkou plasticity“. PLOS ONE. 8 (12): e85072. Bibcode:2013PLoSO ... 885072C. doi:10.1371 / journal.pone.0085072. ISSN 1932-6203. PMC 3871602. PMID 24376866.
- ^ Kuno, G .; Chang, G. J .; Tsuchiya, K. R .; Karabatsos, N .; Cropp, C. B. (leden 1998). "Fylogeneze rodu Flavivirus". Journal of Virology. 72 (1): 73–83. doi:10.1128 / JVI.72.1.73-83.1998. ISSN 0022-538X. PMC 109351. PMID 9420202.
- ^ Forrester, N.L .; Palacios, G .; Tesh, R. B .; Savji, N .; Guzman, H .; Sherman, M .; Weaver, S. C .; Lipkin, W. I. (březen 2012). „Fylogeneze rodu alphavirus v měřítku genomu naznačuje mořský původ“. Journal of Virology. 86 (5): 2729–2738. doi:10.1128 / JVI.05591-11. ISSN 1098-5514. PMC 3302268. PMID 22190718.
- ^ A b Figueiredo, Luiz Tadeu Moraes (2019). „Lidské městské arboviry mohou infikovat divoká zvířata a přejít na cykly údržby Sylvatic v Jižní Americe“. Hranice v buněčné a infekční mikrobiologii. 9: 259. doi:10.3389 / fcimb.2019.00259. ISSN 2235-2988. PMC 6653809. PMID 31380302.
- ^ Ndenga, Bryson Alberto; Mutuku, Francis Maluki; Ngugi, Harun Njenga; Mbakaya, Joel Omari; Aswani, Peter; Musunzaji, Peter Siema; Vulule, John; Mukoko, Dunstan; Kitron, Uriel; LaBeaud, Angelle Desiree (19. 12. 2017). „Charakteristika dospělých komárů Aedes aegypti ve venkovských a městských oblastech západní a pobřežní Keni“. PLOS ONE. 12 (12): e0189971. Bibcode:2017PLoSO..1289971N. doi:10.1371 / journal.pone.0189971. ISSN 1932-6203. PMC 5736227. PMID 29261766.
- ^ Hanley, Kathryn A .; Monath, Thomas P .; Weaver, Scott C .; Rossi, Shannan L .; Richman, Rebecca L .; Vasilakis, Nikos (říjen 2013). „Horečka versus horečka: role vnímavosti hostitele a vektorů a mezidruhové konkurence při formování současného a budoucího distribuce syvatických cyklů viru dengue a viru žluté zimnice“. Infekce, genetika a evoluce: Journal of Molecular Epidemiology and Evolutionary Genetics in Infectious Diseases. 19: 292–311. doi:10.1016 / j.meegid.2013.03.008. ISSN 1567-7257. PMC 3749261. PMID 23523817.
- ^ „Epidemiologie virů Zika a země ohrožené přenosem Zika“. www.zikavirusnet.com. Citováno 2020-04-22.
- ^ Coffey LL, Van Rompay K, Keesler R, Pesavento P, Singapuri A, Linnen J, Gao K (22. května 2017). „Závěrečná zpráva HHSF223201610542P“ (PDF). Úřad pro kontrolu potravin a léčiv. Archivováno (PDF) z původního dne 26.01.2018. Citováno 22. dubna 2020.
- ^ Bryant, Juliet E; Holmes, Edward C; Barrett, Alan D. T (květen 2007). „Mimo Afriku: Molekulární pohled na zavedení viru žluté zimnice do Ameriky“. PLOS patogeny. 3 (5): e75. doi:10.1371 / journal.ppat.0030075. ISSN 1553-7366. PMC 1868956. PMID 17511518.
- ^ Couto-Lima, Dinair; Madec, Yoann; Bersot, Maria Ignez; Campos, Stephanie Silva; Motta, Monique de Albuquerque; Santos, Flávia Barreto Dos; Vazeille, Marie; Vasconcelos, Pedro Fernando da Costa; Lourenço-de-Oliveira, Ricardo; Failloux, Anna-Bella (7. července 2017). „Potenciální riziko opětovného městského přenosu viru žluté zimnice v Brazílii usnadněné příslušnými populacemi Aedes“. Vědecké zprávy. 7 (1): 4848. Bibcode:2017NatSR ... 7.4848C. doi:10.1038 / s41598-017-05186-3. ISSN 2045-2322. PMC 5501812. PMID 28687779.
- ^ Moreira-Soto, A .; Torres, M. C .; Lima de Mendonça, M. C .; Mares-Guia, M. A .; Dos Santos Rodrigues, C. D .; Fabri, A. A .; Dos Santos, C. C .; Machado Araújo, E. S .; Fischer, C .; Ribeiro Nogueira, R. M .; Drosten, C. (září 2018). „Důkazy o několika cyklech přenosu sylvatic během vypuknutí viru žluté zimnice 2016–2017, Brazílie“. Klinická mikrobiologie a infekce. 24 (9): 1019.e1–1019.e4. doi:10.1016 / j.cmi.2018.01.026. ISSN 1469-0691. PMID 29427798.
- ^ Tsetsarkin, Konstantin A; Chen, tření; Weaver, Scott C (únor 2016). „Mezidruhový přenos a výskyt viru chikungunya“. Aktuální názor na virologii. 16: 143–150. doi:10.1016 / j.coviro.2016.02.007. ISSN 1879-6257. PMC 4824623. PMID 26986235.
- ^ Hanley, Kathryn A .; Monath, Thomas P .; Weaver, Scott C .; Rossi, Shannan L .; Richman, Rebecca L .; Vasilakis, Nikos (říjen 2013). „Horečka proti horečce: role vnímavosti hostitele a vektorů a mezidruhové konkurence při formování současného a budoucího distribuce syvatických cyklů viru dengue a viru žluté zimnice“. Infekce, genetika a evoluce: Journal of Molecular Epidemiology and Evolutionary Genetics in Infectious Diseases. 0: 292–311. doi:10.1016 / j.meegid.2013.03.008. ISSN 1567-1348. PMC 3749261. PMID 23523817.
- ^ de Thoisy, Benoît; Lacoste, Vincent; Germain, Adeline; Muñoz-Jordán, Jorge; Colón, Candimar; Mauffrey, Jean-François; Delaval, Marguerite; Catzeflis, François; Kazanji, Mirdad; Matheus, Séverine; Dussart, Philippe (duben 2009). „Infekce dengue u neotropických lesních savců“. Vector Borne and Zoonotic Diseases (Larchmont, NY). 9 (2): 157–170. doi:10.1089 / vbz.2007.0280. ISSN 1557-7759. PMID 18945183.
- ^ Calderón, Alfonso; Guzmán, Camilo; Mattar, Salim; Rodriguez, Virginie; Martínez, Caty; Violet, Lina; Martínez, Jairo; Figueiredo, Luiz Tadeu Moraes (říjen 2019). „Virus dengue u netopýrů z Córdoby a Sucre v Kolumbii“. Vector Borne and Zoonotic Diseases (Larchmont, NY). 19 (10): 747–751. doi:10.1089 / vbz.2018.2324. ISSN 1557-7759. PMC 6765209. PMID 31211661.
- ^ de Figueiredo, Mario LG; de C Gomes, Almério; Amarilla, Alberto A .; de S Leandro, André; de S Orrico, Agnaldo; de Araujo, Renato F .; do SM Castro, Jesuína; Durigon, Edison L .; Aquino, Victor H .; Figueiredo, Luiz TM (12.7.2010). „Komáři infikovaní viry dengue v Brazílii“. Virology Journal. 7 (1): 152. doi:10.1186 / 1743-422X-7-152. ISSN 1743-422X. PMC 2913956. PMID 20624314.
- ^ Ash, A .; Lymbery, A .; Lemon, J .; Vitali, S .; Thompson, R. C. A. (2010-12-15). „Molekulární epidemiologie Giardia duodenalis u ohroženého masožravce - africký malovaný pes“. Veterinární parazitologie. 174 (3): 206–212. doi:10.1016 / j.vetpar.2010.08.034. ISSN 0304-4017. PMID 20851525.
- ^ Osterhaus, A.D .; Rimmelzwaan, G. F .; Martina, B. E .; Bestebroer, T. M .; Fouchier, R. A. (2000-05-12). "Virus chřipky B v tuleních". Věda. 288 (5468): 1051–1053. Bibcode:2000Sci ... 288.1051O. doi:10.1126 / science.288.5468.1051. ISSN 0036-8075. PMID 10807575.
- ^ Barasona, J. A .; Vicente, J .; Díez-Delgado, I .; Aznar, J .; Gortázar, C .; Torres, M. J. (srpen 2017). „Environmentální přítomnost komplexu Mycobacterium tuberculosis v agregačních bodech na rozhraní divoká zvěř / hospodářská zvířata“. Přeshraniční a vznikající nemoci. 64 (4): 1148–1158. doi:10,1111 / tbed.12480. ISSN 1865-1682. PMID 26865411.
- ^ Ewers, Christa; Grobbel, Mirjam; Stamm, Ivonne; Kopp, Peter A .; Diehl, Ines; Semmler, Torsten; Fruth, Angelika; Beutlich, Janine; Guerra, Beatriz; Wieler, Lothar H .; Guenther, Sebastian (duben 2010). „Vznik lidské pandemie O25: H4-ST131 CTX-M-15 Escherichia coli produkující rozšířené spektrum beta-laktamázy mezi společenskými zvířaty“. The Journal of Antimicrobial Chemotherapy. 65 (4): 651–660. doi:10.1093 / jac / dkq004. ISSN 1460-2091. PMID 20118165.
- ^ Erwin, Paul C .; Bemis, David A .; McCombs, Scott B .; Sheeler, Lorinda L .; Himelright, Inga M .; Halford, Sandy K .; Diem, Lois; Metchock, Beverly; Jones, Timothy F .; Schilling, Melisse G .; Thomsen, Bruce V. (prosinec 2004). „Přenos Mycobacterium tuberculosis z člověka na psa“. Vznikající infekční nemoci. 10 (12): 2258–2210. doi:10.3201 / eid1012.040094. ISSN 1080-6040. PMC 3323378. PMID 15672533.
- ^ Swenson, Sabrina L .; Koster, Leo G .; Jenkins-Moore, Melinda; Killian, Mary L .; DeBess, Emilio E .; Baker, Rocky J .; Mulrooney, Donna; Weiss, Robin; Galeota, Judith; Bredthauer, Annette (září 2010). „Přírodní případy pandemie viru chřipky A H1N1 A 2009 u fretek v zájmovém chovu“. Journal of Veterinary Diagnostic Investigation. 22 (5): 784–788. doi:10.1177/104063871002200525. ISSN 1040-6387. PMID 20807944.
- ^ A b C d Shi, Jianzhong; Wen, Zhiyuan; Zhong, Gongxun; Yang, Huanliang; Wang, Chong; Huang, Baoying; Liu, Renqiang; On, Xijun; Shuai, Lei; Sun, Ziruo; Zhao, Yubo (08.04.2020). „Citlivost fretek, koček, psů a jiných domestikovaných zvířat na SARS – koronavirus 2“. Věda: eabb7015. doi:10.1126 / science.abb7015. ISSN 0036-8075. PMC 7164390. PMID 32269068.
- ^ Sjurseth, Siri Kulberg; Gjerset, Britt; Bragstad, Karoline; Hungnes, Olav; Wisløff, Helene; Er, Chiek; Valheim, Mette; Løtvedt, Siri M .; David, Bruce; Hanssen, Skjalg A .; Hauge, Siri H. (2017). „Přenos chřipky A (H1N1) pdm09 z člověka na zvíře v hejnu chovatelů krůt v Norsku“. Ekologie infekce a epidemiologie. 7 (1): 1416249. doi:10.1080/20008686.2017.1416249. ISSN 2000-8686. PMC 5738641. PMID 29296243.
- ^ Howden, Krista J .; Brockhoff, Egan J .; Caya, Francois D .; McLeod, Laura J .; Lavoie, Martin; Ing, Joan D .; Bystrom, Janet M .; Alexandersen, Soren; Pasick, John M .; Berhane, Yohannes; Morrison, Margaret E. (listopad 2009). „Vyšetřování viru lidské pandemické chřipky (H1N1) 2009 na prasečí farmě v Albertě“. Kanadský veterinární věstník. 50 (11): 1153–1161. ISSN 0008-5286. PMC 2764467. PMID 20119537.
- ^ Song, Min-Suk; Lee, Jun Han; Pascua, Philippe Noriel Q .; Baek, Yun Hee; Kwon, Hyeok-il; Park, Kuk Jin; Choi, Hwan-Woon; Shin, Yeun-Kyung; Song, Jae-Young; Kim, Chul-Joong; Choi, Young-Ki (září 2010). „Důkazy o přenosu chřipkového viru pandemie (H1N1) z roku 2009 v Jižní Koreji“. Journal of Clinical Microbiology. 48 (9): 3204–3211. doi:10.1128 / JCM.00053-10. ISSN 0095-1137. PMC 2937722. PMID 20610681.
- ^ Nelson, Martha I .; Gramer, Marie R .; Vincent, Amy L .; Holmes, Edward C. (říjen 2012). „Globální přenos virů chřipky z lidí na prasata“. The Journal of General Virology. 93 (Pt 10): 2195–2203. doi:10.1099 / vir.0.044974-0. ISSN 0022-1317. PMC 3541789. PMID 22791604.
- ^ Chastagner, Amélie; Dost, Vincent; Peroz, David; Hervé, Séverine; Lucas, Pierrick; Quéguiner, Stéphane; Gorin, Stéphane; Beven, Véronique; Behillil, Sylvie; Leneveu, Philippe; Garin, Emmanuel (říjen 2019). „Obousměrný přenos sezónního chřipky A (H1N1) pdm09 na člověka a prasata v Pig Herd, Francie, 2018“. Vznikající infekční nemoci. 25 (10): 1940–1943. doi:10.3201 / eid2510.190068. ISSN 1080-6040. PMC 6759248. PMID 31538914.
- ^ Seguin, Jennifer C .; Walker, Robert D .; Caron, John P .; Kloos, Wesley E .; George, Carol G .; Hollis, Richard J .; Jones, Ronald N .; Pfaller, Michael A. (May 1999). "Methicillin-Resistant Staphylococcus aureus Outbreak in a Veterinary Teaching Hospital: Potential Human-to-Animal Transmission". Journal of Clinical Microbiology. 37 (5): 1459–1463. doi:10.1128/JCM.37.5.1459-1463.1999. ISSN 0095-1137. PMC 84801. PMID 10203505.
- ^ Price, Lance B.; Stegger, Marc; Hasman, Henrik; Aziz, Maliha; Larsen, Jesper; Andersen, Paal Skytt; Pearson, Talima; Waters, Andrew E.; Foster, Jeffrey T.; Schupp, James; Gillece, John (2012-02-21). "Staphylococcus aureus CC398: Host Adaptation and Emergence of Methicillin Resistance in Livestock". mBio. 3 (1). doi:10.1128/mBio.00305-11. ISSN 2150-7511. PMC 3280451. PMID 22354957.
- ^ Holt, Nathalia (2015-03-24). "We Are in the Midst of an Elephant Tuberculosis Epidemic". Břidlicový časopis. Citováno 2020-04-22.
- ^ Crossley, Beate M.; Mock, Richard E.; Callison, Scott A.; Hietala, Sharon K. (2012-12-12). "Identification and Characterization of a Novel Alpaca Respiratory Coronavirus Most Closely Related to the Human Coronavirus 229E". Viry. 4 (12): 3689–3700. doi:10.3390/v4123689. ISSN 1999-4915. PMC 3528286. PMID 23235471.
- ^ "Preliminary Investigation of Zooanthroponosis in a Nigerian Zoological Garden". medwelljournals.com. Citováno 2020-04-22.
- ^ Willy, M. E.; Woodward, R. A.; Thornton, V. B.; Wolff, A. V.; Flynn, B. M.; Heath, J. L.; Villamarzo, Y. S.; Smith, S.; Bellini, W. J.; Rota, P. A. (February 1999). "Management of a measles outbreak among Old World nonhuman primates". Laboratory Animal Science. 49 (1): 42–48. ISSN 0023-6764. PMID 10090093.
- ^ Every, Alison L.; Selwood, Lynne; Castano-Rodriguez, Natalia; Lu, Wei; Windsor, Helen M.; Wee, Janet LK; Swierczak, Agnieszka; Marshall, Barry J.; Kaakoush, Nadeem O.; Mitchell, Hazel M.; Sutton, Philip (2011-02-07). "Did transmission of Helicobacter pylori from humans cause a disease outbreak in a colony of Stripe-faced Dunnarts (Sminthopsis macroura)?". Veterinární výzkum. 42 (1): 26. doi:10.1186/1297-9716-42-26. ISSN 1297-9716. PMC 3042409. PMID 21314909.
- ^ The Chimpanzees of the Taï Forest: Behavioural Ecology and Evolution. Oxford, New York: Oxford University Press. 2000-06-15. ISBN 978-0-19-850507-5.
- ^ Mackay, Ian M.; Arden, Katherine E.; Speicher, David J.; O’Neil, Nicholas T.; McErlean, Peter K.; Greer, Ristan M.; Nissen, Michael D .; Sloots, Theo P. (2012-04-23). "Co-circulation of Four Human Coronaviruses (HCoVs) in Queensland Children with Acute Respiratory Tract Illnesses in 2004". Viry. 4 (4): 637–653. doi:10.3390/v4040637. ISSN 1999-4915. PMC 3347326. PMID 22590689.
- ^ Corman, Victor M .; Muth, Doreen; Niemeyer, Daniela; Drosten, Christian (2018). "Hosts and Sources of Endemic Human Coronaviruses". Pokroky ve výzkumu virů. 100: 163–188. doi:10.1016/bs.aivir.2018.01.001. ISBN 9780128152010. ISSN 0065-3527. PMC 7112090. PMID 29551135.
- ^ Patrono, Livia V.; Samuni, Liran; Corman, Victor M .; Nourifar, Leila; Röthemeier, Caroline; Wittig, Roman M.; Drosten, Christian; Calvignac-Spencer, Sébastien; Leendertz, Fabian H. (2018-06-27). "Human coronavirus OC43 outbreak in wild chimpanzees, Côte d´Ivoire, 2016". Vznikající mikroby a infekce. 7 (1): 118. doi:10.1038/s41426-018-0121-2. ISSN 2222-1751. PMC 6021434. PMID 29950583.
- ^ Scully, Erik J.; Basnet, Sarmi; Wrangham, Richard W .; Muller, Martin N.; Otali, Emily; Hyeroba, David; Grindle, Kristine A.; Pappas, Tressa E.; Thompson, Melissa Emery; Machanda, Zarin; Watters, Kelly E. (February 2018). "Lethal Respiratory Disease Associated with Human Rhinovirus C in Wild Chimpanzees, Uganda, 2013". Vznikající infekční nemoci. 24 (2): 267–274. doi:10.3201/eid2402.170778. ISSN 1080-6040. PMC 5782908. PMID 29350142.
- ^ Miller, Michele A.; Buss, Peter; Roos, Eduard O.; Hausler, Guy; Dippenaar, Anzaan; Mitchell, Emily; van Schalkwyk, Louis; Robbe-Austerman, Suelee; Waters, W. Ray; Sikar-Gang, Alina; Lyashchenko, Konstantin P. (2019-02-06). "Fatal Tuberculosis in a Free-Ranging African Elephant and One Health Implications of Human Pathogens in Wildlife". Hranice ve veterinární vědě. 6: 18. doi:10.3389/fvets.2019.00018. ISSN 2297-1769. PMC 6373532. PMID 30788347.
- ^ Negrey, Jacob D.; Reddy, Rachna B.; Scully, Erik J.; Phillips-Garcia, Sarah; Owens, Leah A.; Langergraber, Kevin E.; Mitani, John C.; Emery Thompson, Melissa; Wrangham, Richard W .; Muller, Martin N.; Otali, Emily (2019-01-21). "Simultaneous outbreaks of respiratory disease in wild chimpanzees caused by distinct viruses of human origin". Vznikající mikroby a infekce. 8 (1): 139–149. doi:10.1080/22221751.2018.1563456. ISSN 2222-1751. PMC 6455141. PMID 30866768.
- ^ Nizeyi, John Bosco; Innocent, Rwego B.; Erume, Joseph; Kalema, Gladys R. N. N.; Cranfield, Michael R.; Graczyk, Thaddeus K. (April 2001). "Campylobacteriosis, Salmonellosis, and Shigellosis in Free-Ranging Human-Habituated Mountain Gorillas of Uganda". Journal of Wildlife Diseases. 37 (2): 239–244. doi:10.7589/0090-3558-37.2.239. ISSN 0090-3558. PMID 11310873.
