Thioformaldehyd - Thioformaldehyde - Wikipedia
| |||
| Jména | |||
|---|---|---|---|
| Ostatní jména methanethial | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChemSpider | |||
| Číslo ES |
| ||
PubChem CID | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
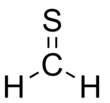
| CH2S | |||
| Molární hmotnost | 46.09 | ||
| Vzhled | neznámý | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Thioformaldehyd je organosírná sloučenina se vzorcem CH2S. Tato sloučenina je velmi zřídka pozorována, protože oligomerizuje na 1,3,5-trithian, což je stabilní bezbarvá sloučenina se stejným empirickým vzorcem. Navzdory své nestabilitě za normálních suchozemských podmínek byla molekula pozorována v mezihvězdné médium[1] a přitahoval velkou pozornost pro svou základní povahu.[2] Tendence thioformaldehydu k tvorbě řetězců a kruhů je projevem pravidlo dvojné vazby.
Ačkoli má thioformaldehyd sklon k oligomerizaci, je známo mnoho kovových komplexů. Jedním příkladem je Os (SCH2) (CO)2(PPh3)2.[3]

Syntéza wolframového thioformaldehydového komplexu.

Syntéza komplexu osmium thioformaldehyd.
Reference
- ^ Despois, D., „Radioline Observation of Molecular and Isotopic Species in Comet C / 1995 O1 (Hale-Bopp) Implications on the Interstellar Origin of Cometary Ices“, Earth, Moon, Planets 1999, 79, 103-124.
- ^ Clouthier, D. J .; Ramsay, D. A. (1983). "Spektroskopie formaldehydu a thioformaldehydu". Roční přehled fyzikální chemie. 34: 31–58. Bibcode:1983ARPC ... 34 ... 31C. doi:10.1146 / annurev.pc.34.100183.000335.
- ^ Schenk, Wolfdieter A. (2011). „Koordinační chemie malých molekul obsahujících síru: osobní pohled“. Dalton Trans. 40 (6): 1209–1219. doi:10.1039 / C0DT00975J. PMID 21088787.