Uroporfyrinogen III - Uroporphyrinogen III
 | |
| Identifikátory | |
|---|---|
| Pletivo | Uroporfyrinogen + III |
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| Vlastnosti | |
| C40H44N4Ó16 | |
| Molární hmotnost | 836,795 g / mol |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
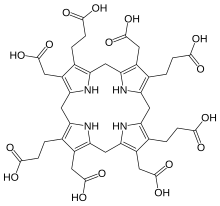
Uroporfyrinogen III je tetrapyrrol, první makrocyklický meziprodukt v biosyntéza z heme, chlorofyl, vitamin B12, a siroheme. Je to bezbarvá sloučenina, jako ostatní porfyrinogeny.[1]
Struktura
The molekulární struktura uroporphyrinogenu III lze popsat jako a hexahydroporphine jádro, kde každý pyrrol prsten má vodík atomy na jeho dvou nejvzdálenějších uhlíky nahrazeno octová kyselina skupina (-CH
2- COOH, „A“) a a kyselina propionová skupina (-CH
2-CH
2- COOH, „P“). Skupiny jsou připojeny asymetrickým způsobem: při procházení makrocyklem je pořadí AP-AP-AP-PA.
Biosyntéza a metabolismus
Obecně biosyntéza porfyrinu dráha, uroporphyrinogen III je odvozen z lineárního tetrapyrrolu preuroporfyrinogen (a substituovaný hydroxymethylbilan ) působením enzym uroporphyrinogen-III cosynthase.[2][3]
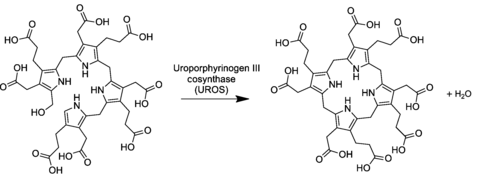
Konverze má za následek obrácení posledního pyrrol jednotka (výměna skupin kyseliny octové a propionové) a a kondenzační reakce který uzavírá makrocyklus vyloučením finále hydroxyl -OH s atomem vodíku prvního kruhu.
V biosyntéze hemů a chlorofylů se uroporfyrinogen III přeměňuje na koproporfyrinogen III enzymem uroporphyrinogen III dekarboxyláza. V biosyntéze sirohemů se uroporfyrinogen III převádí dvěma methyltransferázami na dihydrosirohydrochlorin, který je následně oxidován sirohydrochlorin, předchůdce siroheme protetická skupina.
Lékařský význam
Pokud není přítomna nebo není aktivní uroporphyrinogen-III syntáza, hydroxymethylbilan bude spontánně cyklizovat do strukturní izomer uroporphyrinogen I, který se liší od III izomeru v tom, že skupiny kyseliny octové („A“) a kyseliny propionové („P“) jsou uspořádány v rotačně symetrickém pořadí, AP-AP-AP-AP. V tomto případě byl vytvořen další krok koproporfyrinogen I, který se hromadí - vedoucí k patologické stav vrozená erytropoetická porfyrie[3]
Viz také
Reference
- ^ Dalton, J (1969). "Tvorba makrocyklického kruhu v biosyntéze tetrapyrrolu". Příroda. 223 (5211): 1151–1153. Bibcode:1969Natur.223.1151D. doi:10.1038 / 2231151a0. PMID 5810686.
- ^ Paul R. Ortiz de Montellano (2008). "Hemes v biologii". Wiley Encyclopedia of Chemical Biology. John Wiley & Sons. doi:10.1002 / 9780470048672.wecb221. ISBN 978-0470048672.
- ^ A b S. Sassa a A. Kappas (2000): „Molekulární aspekty zděděných porfyrií“. Journal of Internal Medicine, svazek 247, číslo 2, strany 169-178. doi:10.1046 / j.1365-2796.2000.00618.x
