Post-transkripční modifikace - Post-transcriptional modification
Tento chybí informace o sekcích pro RNA kromě mRNA. (Říjen 2020) |
Post-transkripční modifikace nebo ko-transkripční modifikace je soubor biologických procesů společných většině eukaryotický buňky, kterými RNA primární přepis je chemicky změněn transkripce od a gen k produkci zralé, funkční molekuly RNA, která pak může opustit jádro a vykonávat v buňce jakoukoli z různých funkcí. [1] Existuje mnoho typů post-transkripčních modifikací dosažených prostřednictvím rozmanité třídy molekulárních mechanismů.
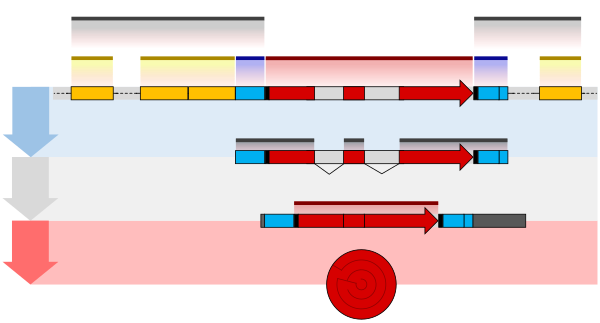
Jedním z příkladů je převod prekurzoru messenger RNA přepisy do zralé messengerové RNA, která je následně schopná být přeloženo do protein. Tento proces zahrnuje tři hlavní kroky, které významně modifikují chemickou strukturu molekuly RNA: přidání a 5 'čepice, přidání 3 ' polyadenylovaný ocas a Sestřih RNA. Takové zpracování je zásadní pro správný překlad eukaryotiky genomy protože počáteční prekurzorová mRNA produkovaná transkripcí často obsahuje obojí exony (kódující sekvence) a introny (nekódující sekvence); sestřih odstraňuje introny a spojuje exony přímo, zatímco čepice a ocas usnadňují transport mRNA do ribozom a chránit jej před molekulární degradací.[2]
Post-transkripční úpravy mohou také nastat během zpracování dalších transkriptů, které se nakonec stanou přenos RNA, ribozomální RNA nebo jakýkoli jiný typ RNA používaný buňkou.
Zpracování mRNA
Molekula pre-mRNA prochází třemi hlavními modifikacemi. Tyto úpravy jsou 5 'zakončení, 3' polyadenylace, a Sestřih RNA, které se vyskytují v buněčné jádro než je RNA přeloženo.[4]
5 'zpracování
Omezení
Uzavření pre-mRNA zahrnuje přidání 7-methylguanosin (m7G) na 5 'konec. K dosažení tohoto cíle vyžaduje terminální 5 'fosfát odstranění, které se provádí pomocí a fosfatáza enzym. Enzym guanosyltransferáza pak katalyzuje reakci, která produkuje difosfát 5 'konec. Difosfátový 5 'konec pak napadá atom alfa fosforu a GTP molekula za účelem přidání guanin zbytek v 5'5 'trifosfátové vazbě. Enzym (guanin -N7-) - methyltransferáza ("cap MTase") přenáší methylovou skupinu z S-adenosyl methionin na guaninový kruh.[5] Tento typ čepice, pouze s (m7G) v pozici se nazývá cap 0 struktura. The ribóza sousedního nukleotid může být také methylován za vzniku víčka 1. Methylace nukleotidů za molekulou RNA produkuje struktury víčka 2, víčka 3 atd. V těchto případech jsou methylové skupiny přidány do 2 'OH skupin ribózového cukru. Víčko chrání 5' konec primárního RNA transkriptu před útokem ribonukleázy které mají specifičnost k 3'5 ' fosfodiesterové vazby.[6]
3 'zpracování
Štěpení a polyadenylace
Zpracování pre-mRNA na 3 'konci molekuly RNA zahrnuje štěpení jejího 3' konce a poté přidání asi 250 adenin zbytky za vzniku a poly (A) ocas. Štěpné a adenylační reakce se vyskytují primárně, pokud a sekvence polyadenylačního signálu (5'- AAUAAA-3 ') se nachází poblíž 3' konce molekuly pre-mRNA, za kterou následuje další sekvence, která je obvykle (5'-CA-3 ') a je místem štěpení. A Sekvence bohatá na GU je také obvykle přítomný dále po proudu na molekule pre-mRNA. Nedávno bylo prokázáno, že alternativní signální sekvence, jako je UGUA proti proudu od místa štěpení, mohou také řídit štěpení a polyadenylaci v nepřítomnosti signálu AAUAAA. Je důležité si uvědomit, že tyto dva signály nejsou vzájemně nezávislé a často koexistují. Po syntéze sekvenčních prvků několik více podjednotek bílkoviny jsou přeneseny do molekuly RNA. Přenos těchto sekvenčně specifických vazebných proteinů faktor štěpení a polyadenylační specificity (CPSF), faktor štěpení I (CF I) a faktor stimulace štěpení (CStF) se vyskytuje od RNA polymeráza II. Tyto tři faktory se vážou na prvky sekvence. Signál AAUAAA je přímo vázán CPSF. V případě zpracovatelských míst závislých na UGUA se vazba komplexu s více proteiny provádí pomocí štěpného faktoru I (CF I). Výsledný vytvořený proteinový komplex obsahuje další štěpné faktory a enzym Polyadenylát polymeráza (PAP). Tento komplex štěpí RNA mezi polyadenylační sekvencí a sekvencí bohatou na GU v místě štěpení označeném (5'-CA-3 ') sekvencemi. Poly (A) polymeráza poté přidá asi 200 adeninových jednotek na nový 3 'konec molekuly RNA pomocí ATP jako předchůdce. Protože je poly (A) ocas syntetizován, váže více kopií protein vázající poly (A), který chrání 3'-konec před trávením ribonukleázou enzymy včetně CCR4-ne komplex.[6]
Spojování intronů
Sestřih RNA je proces, kterým introny, oblasti RNA, které nekódují proteiny, jsou odstraněny z pre-mRNA a zbývající exony připojen k opětovné formě jediné spojité molekuly. Exony jsou části mRNA, které se „exprimují“ nebo se překládají do proteinu. Jsou to kódující části molekuly mRNA.[7] Ačkoli většina sestřihu RNA nastává po úplné syntéze a zakončení pre-mRNA, transkripty s mnoha exony lze sestřihnout transkripčně.[8] Spojovací reakce je katalyzována velkým proteinovým komplexem zvaným spliceosome sestavené z bílkovin a malá jaderná RNA molekuly, které rozpoznávají spojovací weby v pre-mRNA sekvenci. Mnoho pre-mRNA, včetně těch kódujících protilátky, lze spojit několika způsoby k produkci různých zralých mRNA, které kódují různé proteinové sekvence. Tento proces je znám jako alternativní sestřih a umožňuje produkci široké škály proteinů z omezeného množství DNA.
Zpracování histonové mRNA
Histony H2A, H2B, H3 a H4 tvoří jádro a nukleosom a tak se nazývají hlavní histony. Zpracování jádrových histonů se provádí odlišně, protože typické histonové mRNA postrádá několik rysů jiných eukaryotických mRNA, jako je poly (A) ocas a introny. Takové mRNA tedy nepodstoupí sestřih a jejich 3 'zpracování se provádí nezávisle na většině faktorů štěpení a polyadenylace. Základní histonové mRNA mají speciální kmenová smyčka struktura na 3-prime konci, která je rozpoznána a protein vázající kmen-smyčku a downstream sekvence, nazývaná histonový downstream prvek (HDE), která rekrutuje U7 snRNA. Faktor štěpení a polyadenylační specificity 73 řeže mRNA mezi kmenovou smyčkou a HDE[9]
Histonové varianty, jako např H2A.Z nebo H3.3 však mají introny a jsou zpracovávány jako normální mRNA včetně sestřihu a polyadenylace.[9]
Viz také
Reference
- ^ Kiss T (červenec 2001). „Malá transkripční modifikace buněčných RNA vedená malými nukleolárními RNA“. Časopis EMBO. 20 (14): 3617–22. doi:10.1093 / emboj / 20.14.3617. PMC 125535. PMID 11447102.
- ^ Berg, Tymoczko & Stryer 2007, str. 836
- ^ A b Shafee, Thomas; Lowe, Rohan (2017). "Eukaryotická a prokaryotická genová struktura". WikiJournal of Medicine. 4 (1). doi:10.15347 / wjm / 2017.002. ISSN 2002-4436.
- ^ Berg, Tymoczko & Stryer 2007, str. 841
- ^ Yamada-Okabe T, Mio T, Kashima Y, Matsui M, Arisawa M, Yamada-Okabe H (listopad 1999). „Gen Candida albicans pro mRNA 5-cap methyltransferasu: identifikace dalších zbytků nezbytných pro katalýzu“. Mikrobiologie. 145 (Pt 11) (11): 3023–33. doi:10.1099/00221287-145-11-3023. PMID 10589710. Archivovány od originál dne 2012-07-12.
- ^ A b Hames & Hooper 2006, str. 221
- ^ Biologie. Vzdělání Mgraw Hill. 2014. s. 241–242. ISBN 978-981-4581-85-1.
- ^ Lodish HF, Berk A, Kaiser C, Krieger M, Scott MP, Bretscher A, Ploegh H, Matsudaira PT (2007). „Kapitola 8: Post-transkripční kontrola genů“. Molekulární buňka .Biologie. San Francisco: WH Freeman. ISBN 978-0-7167-7601-7.
- ^ A b Marzluff WF, Wagner EJ, Duronio RJ (listopad 2008). "Metabolismus a regulace kanonických histonových mRNA: život bez poly (A) ocasu". Recenze přírody. Genetika. 9 (11): 843–54. doi:10.1038 / nrg2438. PMC 2715827. PMID 18927579.
Další čtení
- Berg JM, Tymoczko JL, Stryer L. (2007). Biochemie (6. vyd.). New York: WH Freeman & Co. ISBN 978-0-7167-6766-4.
- Hames D, Hooper N (2006). Okamžité poznámky biochemie. Annales de Biologie Clinique. 58 (3. vyd.). Leeds: Taylor a Francis. p. 767. ISBN 978-0-415-36778-3. PMID 11098183.
- Sun WJ, Li JH, Liu S, Wu J, Zhou H, Qu LH, Yang JH (leden 2016). „RMBase: zdroj pro dekódování krajiny modifikací RNA z vysoce výkonných sekvenčních dat“. Výzkum nukleových kyselin. 44 (D1): D259-65. doi:10.1093 / nar / gkv1036. PMC 4702777. PMID 26464443.
- Machnicka MA, Milanowska K, Osman Oglou O, Purta E, Kurkowska M, Olchowik A, Januszewski W, Kalinowski S, Dunin-Horkawicz S, Rother KM, Helm M, Bujnicki JM, Grosjean H (leden 2013). „MODOMIKA: databáze cest modifikací RNA - aktualizace 2013“. Výzkum nukleových kyselin. 41 (Problém s databází): D262-7. doi:10.1093 / nar / gks1007. PMC 3531130. PMID 23118484.
- Cantara WA, Crain PF, Rozenski J, McCloskey JA, Harris KA, Zhang X, Vendeix FA, Fabris D, Agris PF (leden 2011). „Databáze modifikace RNA, aktualizace RNAMDB: 2011“. Výzkum nukleových kyselin. 39 (Problém s databází): D195-201. doi:10.1093 / nar / gkq1028. PMC 3013656. PMID 21071406.
- Post-transkripční + RNA + modifikace v americké národní lékařské knihovně Lékařské předměty (Pletivo)