Těkavost fluoridů - Fluoride volatility
Těkavost fluoridů je tendence velmi fluorované molekuly na odpařit se při poměrně nízkých teplotách. Heptafluoridy, hexafluoridy a pentafluoridy mají mnohem nižší teploty varu než nižšímocenství fluoridy. Většina difluoridy a trifluoridy mají vysoké teploty varu, zatímco většina tetrafluoridy a monofluoridy spadnout mezi. Termín „těkavost fluoridů“ je žargon používá se zejména v souvislosti s oddělováním radionuklidy.
Volatilita a valence
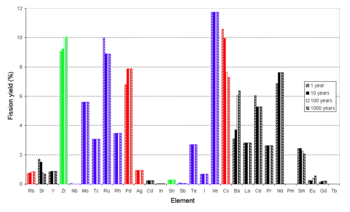
Valence pro většinu prvků je založen na nejvyšší známém fluoridu.
Zhruba lze těkavost fluoridů použít k odstranění prvků s valencí 5 nebo větší: uran, neptunium, plutonium, metaloidy (telur, antimon ), nekovy (selen ), halogeny (jód, bróm ) a uprostřed přechodné kovy (niob, molybden, technecium, ruthenium, a možná rhodium ). Tato frakce zahrnuje aktinidy, které lze nejsnadněji znovu použít jako jaderné palivo v a tepelný reaktor a dva štěpné produkty s dlouhou životností nejvhodnější k likvidaci transmutací, Tc-99 a I-129, stejně jako Se-79.
vzácné plyny (xenon, krypton ) jsou těkavé i bez fluoridace a nebudou kondenzovat kromě při mnohem nižších teplotách.
Zůstali pozadu alkalické kovy (cesium, rubidium ), kovy alkalických zemin (stroncium, baryum ), lanthanoidy, zbývající aktinidy (americium, kurium ), zbývající přechodné kovy (yttrium, zirkonium, palladium, stříbrný ) a post-přechodové kovy (cín, indium, kadmium ). Tato frakce obsahuje štěpné produkty, které představují radiační nebezpečí na stupnici desetiletí (CS-137, Sr-90, Sm-151 ), zbývající čtyři štěpné produkty s dlouhou životností CS-135, Zr-93, Pd-107, Sn-126 z nichž pouze poslední vydává silné záření, většina z neutronové jedy a vyšší aktinidy (americium, kurium, kalifornium ), která představují radiační rizika v rozsahu stovek nebo tisíců let a je obtížné s nimi pracovat kvůli gama záření, ale jsou štěpitelná rychlý reaktor.
Metody přepracování
Oxidy uranu reagují s fluorem za vzniku plynných látek hexafluorid uranu, většina plutonium reaguje za vzniku plynného hexafluoridu plutonia, většina štěpné produkty (zejména elektropozitivní prvky: lanthanoidy, stroncium, baryum, yttrium, cesium ) tvoří netěkavé fluoridy. Několik kovů ve štěpných produktech ( přechodné kovy niob, ruthenium, technecium, molybden a halogen jód ) tvoří těkavé (bod varu <200 ° C) fluoridy, které doprovázejí hexafluoridy uranu a plutonia, spolu s inertní plyny. Destilace Potom se použije k oddělení hexafluoridu uranu od směsi.[1][2]
Nestálý alkalický štěpné produkty a drobné aktinidy je nejvhodnější pro další zpracování „suchým“ elektrochemické zpracovává se (pyrochemický ) nevodné metody. The lanthanid fluoridy se obtížně rozpouštějí v kyselina dusičná používané pro metody vodného přepracování, jako je např PUREX, DIAMEX a SANEX, které používají extrakce rozpouštědlem. Těkavost fluoridů je pouze jedním z několika pyrochemických procesů určených k přepracování použitého jaderného paliva.
The Ústav jaderného výzkumu Řež v Řež v Česká republika testované šnekové dávkovače, které přiváděly mletý oxid uranu (simulující použité palivové pelety) do fluorátoru, kde byly částice spalovány v plynném fluoru za vzniku hexafluorid uranu.[3]
Tabulka příslušných vlastností
| Fluorid | Z | Vařící ° C | Tání ° C | Klíč poločas rozpadu | Výtěžek |
|---|---|---|---|---|---|
| SeF6 | 34 | −46.6 | −50.8 | 79Se: 65ky | .04% |
| TeF6 | 52 | −39 | −38 | 127 mTe: 109 d | |
| LI7 | 53 | 4,8 (1 atm) | 6.5 (tripoint ) | 129I: 15,7 mil | 0.54% |
| MF6 | 42 | 34 | 17.4 | 99Po: 2,75 d | |
| PuF6 | 94 | 62 | 52 | 239Pu: 24ky | |
| TcF6 | 43 | 55.3 | 37.4 | 99Tc: 213ky | 6.1% |
| NpF6 | 93 | 55.18 | 54.4 | 237Np: 2,14 mil | |
| UF6 | 92 | 56,5 (subl) | 64.8 | 233U: 160ky | |
| RuF6 | 44 | 54 | 106Ru: 374d | ||
| RhF6 | 45 | 70 | 103Rh: stabilní | ||
| Odkaz7 | 75 | 73.72 | 48.3 | Ne FP | |
| BrF5 | 35 | 40.25 | −61.30 | 81Br: stabilní | |
| LI5 | 53 | 97.85 | 9.43 | 129I: 15,7 mil | 0.54% |
| XeF2 | 54 | 114.25 (subl ) | 129.03 (tripoint ) | ||
| SbF5 | 51 | 141 | 8.3 | 125Sb: 2,76 roku | |
| RuOF4 | 44 | 184 | 115 | 106Ru: 374d | |
| RuF5 | 44 | 227 | 86.5 | 106Ru: 374d | |
| NbF5 | 41 | 234 | 79 | 95Nb: 35d | nízký |
| PdF4 | 46 | 107Pd: 6,5 mil | |||
| SnF4 | 50 | 750 (subl) | 705 | 121m1Sn: 44 let 126Sn: 230ky | 0.013% ? |
| ZrF4 | 40 | 905 | 932 (tripoint) | 93Zr: 1,5 mil | 6.35% |
| AgF | 47 | 1159 | 435 | 109Ag: stabilní | |
| CsF | 55 | 1251 | 682 | 137Čs: 30,2r 135Cs: 2,3 mil | 6.19% 6.54% |
| BeF2 | 4 | 1327 | 552 | ||
| RbF | 37 | 1410 | 795 | ||
| UF4 | 92 | 1417 | 1036 | 233U: 160ky | |
| FLiBe | 1430 | 459 | stabilní | ||
| FLiNaK | 1570 | 454 | stabilní | ||
| LiF | 3 | 1676 | 848 | stabilní | |
| KF | 19 | 1502 | 858 | 40K: 1,25 Gy | |
| NaF | 11 | 1704 | 993 | stabilní | |
| ThF4 | 90 | 1680 | 1110 | ||
| CdF2 | 48 | 1748 | 1110 | 113 mCd: 14,1r | |
| YF3 | 39 | 2230 | 1150 | 91Y: 58,51 d | |
| InF3 | 49 | >1200 | 1170 | ||
| BaF2 | 56 | 2260 | 1368 | 140Ba: 12,75 d | |
| TbF3 | 65 | 2280 | 1172 | ||
| GdF3 | 64 | 1231 | 159Gd: 18,5 hodiny | ||
| PmF3 | 61 | 1338 | 147Pm: 2,62 r | ||
| EuF3 | 63 | 2280 | 1390 | 155Eu: 4,76 let | |
| NdF3 | 60 | 2300 | 1374 | 147Nd: 11d | |
| PrF3 | 59 | 1395 | 143Pr: 13,57 d | ||
| CeF3 | 58 | 2327 | 1430 | 144Ce: 285d | |
| SmF3 | 62 | 2427 | 1306 | 151Sm: 90y | 0.419% ? |
| SrF2 | 38 | 2460 | 1477 | 90Sr: 29,1r | 5.8% |
| LaF3 | 57 | 1493 | 140La: 1,68 d |
Viz také
Poznámky
- Chybějící špičkové fluoridy:[4]
- PrF4 (protože se rozkládá při 90 ° C)
- TbF4 (protože se rozkládá při 300 ° C)
- CeF4 (protože se rozkládá při 600 ° C)
- Bez stabilních fluoridů: Kr, Xe, Pd[5]
Reference
- ^ Uhlíř, Jan. „Zkušenosti s přepracováním suchého jaderného paliva v České republice“ (PDF). OECD Agentura pro jadernou energii. Citováno 2008-05-21.
- ^ Uhlíř, Jan. „Výzkum a vývoj pyrochemického dělení v České republice“ (PDF). Agentura pro jadernou energii OECD. Citováno 2008-05-21.
- ^ Markvart, Miloš. „Vývoj dávkování prášku oxidu uranu pro proces separace těkavých látek fluoridů“ (PDF). Archivovány od originál (PDF) dne 17. listopadu 2004. Citováno 2008-05-21.
- ^ CRC Handbook of Chemistry and Physics, 88. vydání Archivováno 04.07.2010 na Wayback Machine. (PDF). Citováno 2010-11-14.
- ^ Rafinace drahých kovů plynným fluorem - patent 5076839. Freepatentsonline.com. Citováno 2010-11-14.
externí odkazy
- Studium elektrochemických procesů pro separaci aktinidů a lanthanidů v roztaveném fluoridovém médiu (PDF )
- "Oddělení a čištění UF6 z těkavých fluoridů rektifikací " (PDF). Archivovány od originál (PDF) dne 13. ledna 2005.
- Nízkotlaká destilace části soli nosiče paliva z experimentu reaktoru s roztavenou solí (PDF)
- Využití procesu těkavosti fluoridů k extrakci technecia z přeměněného vyhořelého jaderného paliva (PDF)
- Peer Review of the Strategy for Characterizing Transuranics and Technetium Contamination in Depleted Uranium Hexafluoride Tails Cylinders (PDF)
- FYZIKÁLNÍ KONSTANTY ANORGANICKÝCH SLOUČENIN (PDF)
