Japonská encefalitida - Japanese encephalitis
| Japonská encefalitida | |
|---|---|
| Ostatní jména | Japonská encefalitida B. |
 | |
| Zeměpisné rozšíření japonské encefalitidy (tmavě zelené) | |
| Specialita | Infekční nemoc |
| Příznaky | Bolest hlavy, horečka, zvracení, zmatenost, záchvaty[1] |
| Obvyklý nástup | 5 až 15 dní po infekci[1] |
| Příčiny | Virus japonské encefalitidy (šíří se komáry) |
| Diagnostická metoda | Krev nebo mozkomíšní mok testování[2] |
| Prevence | Vakcína proti japonské encefalitidě, vyhnout se kousnutí komárem[2] |
| Léčba | Podpůrná péče[1] |
| Prognóza | Trvalé neurologické problémy se vyskytují až u poloviny přeživších[2] |
| Frekvence | 68,000[2] |
| Úmrtí | 17,000[2] |
Japonská encefalitida (JE) je infekce mozek způsobené virem japonské encefalitidy (JEV).[3] Zatímco většina infekcí vede k malým nebo žádným příznakům, příležitostně dochází k zánětu mozku.[3] V těchto případech mohou příznaky zahrnovat bolest hlavy, zvracení, horečku, zmatenost a záchvaty.[1] K tomu dochází přibližně 5 až 15 dní po infekci.[1]
JEV se obecně šíří o komáři, konkrétně z Culex typ.[2] Prasata a volně žijící ptáci slouží jako rezervoár viru.[2] Nemoc se většinou vyskytuje mimo města.[2] Diagnóza je založena na krvi nebo mozkomíšní mok testování.[2]
Prevence je obecně u Vakcína proti japonské encefalitidě, což je bezpečné i efektivní.[2] Mezi další opatření patří vyhýbání se kousnutí komárem.[2] Po infikování neexistuje žádná konkrétní léčba péče je podpůrná.[1] To se obvykle provádí v nemocnici.[1] Trvalé problémy se vyskytují až u poloviny lidí, kteří se zotavili z JE.[2]
Nemoc se vyskytuje v Jihovýchodní Asie a Západní Pacifik.[2] Asi 3 miliardy lidí žijí v oblastech, kde se tato nemoc vyskytuje.[2] Asi 68 000 symptomatických případů se vyskytne ročně, s přibližně 17 000 úmrtí.[2] Případy se často vyskytují v ohniska.[2] Nemoc byla poprvé popsána v Japonsku v roce 1871.[2] Přes své jméno je tato choroba v Japonsku v důsledku rozsáhlých imunizačních snah relativně vzácná.[4]
Příznaky a symptomy
Virus japonské encefalitidy (JEV) má inkubační doba 2 až 26 dnů.[5] Drtivá většina infekcí je bez příznaků: pouze u 1 z 250 infekcí se vyvine encefalitida.[6]
Závažné důsledky mohou označit nástup tohoto onemocnění u lidí. Horečka, bolest hlavy a nevolnost jsou jiné nespecifické příznaky onemocnění, které může trvat 1 až 6 dní. Známky, které se vyvinou během akutní encefalitické fáze, zahrnují tuhost krku, kachexie, hemiparéza, křeče a zvýšená tělesná teplota mezi 38–41 ° C (100,4–105,8 ° F). Mentální retardace je obvykle vyvinut. Úmrtnost na toto onemocnění se liší, ale je obecně vyšší u dětí. Bylo zaznamenáno transplacentární rozšíření. Celoživotní neurologické vady, jako je hluchota, emoční labilita a hemiparéza se mohou objevit u těch, kteří měli centrální nervový systém účast. Ve známých případech zahrnují některé účinky také nevolnost, bolesti hlavy, horečku a zvracení.[Citace je zapotřebí ]
Zvýšené mikrogliální Bylo zjištěno, že aktivace po infekci japonskou encefalitidou ovlivňuje výsledek virové patogeneze. Microglia jsou rezidenty imunitní buňky centrálního nervového systému (CNS) a hrají klíčovou roli v obraně hostitele před napadením mikroorganismy. Aktivované mikroglie vylučují cytokiny, jako např interleukin-1 (IL-1) a faktor nekrózy nádorů alfa (TNF-α), který může způsobit toxické účinky v mozku. Navíc, další rozpustné faktory, jako je neurotoxiny, excitační neurotransmitery, prostaglandin, reaktivní kyslík a druhy dusíku jsou vylučovány aktivovanou mikroglií.
V myší modelu JE, bylo zjištěno, že v hipokampus a striatum, počet aktivovaných mikroglií byl více než kdekoli jinde v mozku těsně následovaný počtem v thalamus. V mozkové kůře byl počet aktivovaných mikroglií ve srovnání s jinými oblastmi EU významně nižší myší mozek. Celková indukce diferenciálního vyjádření prozánětlivé cytokiny a chemokiny byly také pozorovány z různých oblastí mozku během progresivní infekce japonskou encefalitidou.
Ačkoli čistým účinkem prozánětlivých mediátorů je zabíjení infekčních organismů a infikovaných buněk a také stimulace produkce molekul, které zesilují rostoucí reakci na poškození, je také zřejmé, že v neregenerujícím orgánu, jako je mozek, je dysregulovaný vrozený imunitní odpověď by byla škodlivá. V JE se zdá být narušena přísná regulace aktivace mikroglií, což vede k autotoxický smyčka mikrogliální aktivace, která možná vede k poškození okolních neuronů.[7] Mezi klíčové příznaky u zvířat patří neplodnost a potrat u prasat, neurologické onemocnění u koní a systémové příznaky včetně horečky, letargie a anorexie.[8]
Způsobit
Je to onemocnění způsobené komár -rozený Virus japonské encefalitidy (JEV).[9]
Virologie
| Virus japonské encefalitidy | |
|---|---|
 | |
| Flavivirová struktura a genom | |
| Klasifikace virů | |
| (bez hodnocení): | Virus |
| Oblast: | Riboviria |
| Království: | Orthornavirae |
| Kmen: | Kitrinoviricota |
| Třída: | Flasuviricetes |
| Objednat: | Amarillovirales |
| Rodina: | Flaviviridae |
| Rod: | Flavivirus |
| Druh: | Virus japonské encefalitidy |
JEV je virus z rodiny Flaviviridae, část Sérokomplex japonské encefalitidy 9 geneticky a antigenně související viry, z nichž některé jsou obzvláště závažné koně a čtyři známé infekce lidí, včetně virus západního Nilu.[10] Zahalený virus úzce souvisí s virus západního Nilu a St. Louis encefalitida virus. Pozitivní smysl jednořetězcový RNA genom je zabalen v kapsid který je tvořen kapsidovým proteinem. Vnější obal je tvořen proteinem obalu a je ochranným antigenem. Pomáhá při vstupu viru do vnitřku buňky. Genom také kóduje několik nestrukturálních proteinů (NS1, NS2a, NS2b, NS3, N4a, NS4b, NS5). NS1 se vyrábí také jako sekreční forma. NS3 je domnělý helikáza a NS5 je virový polymeráza. Bylo poznamenáno, že japonská encefalitida infikuje lumen z endoplazmatické retikulum (ER)[11][12] a rychle akumuluje podstatné množství virových proteinů.
Na základě obalového genu existuje pět genotypů (I – V). Kmen Muar, izolovaný od pacienta v Malajsko v roce 1952 se jedná o prototyp kmene genotypu V. Genotyp IV se jeví jako kmen předků a zdá se, že virus se vyvinul v indonésko-malajské oblasti. První klinické zprávy pocházejí z roku 1870, ale zdá se, že virus se vyvinul v polovině 16. století. Do roku 2010 bylo sekvenováno více než šedesát úplných genomů tohoto viru.
Diagnóza
Japonská encefalitida je diagnostikována komerčně dostupnými testy detekujícími Ig virové protilátky specifické pro JE virus v séru a / nebo mozkomíšní mok například zachycením IgM ELISA.[13]
IgM protilátky proti viru JE jsou obvykle detekovatelné 3 až 8 dní po nástupu nemoci a přetrvávají 30 až 90 dnů, ale delší perzistence byla zdokumentována. Pozitivní protilátky IgM proto občas mohou odrážet minulou infekci nebo očkování. Sérum odebrané do 10 dnů od nástupu nemoci nemusí mít detekovatelný IgM a test by měl být opakován na rekonvalescentním vzorku. U pacientů s protilátkami IgM proti viru JE by mělo být provedeno potvrzující testování neutralizačních protilátek.[Citace je zapotřebí ]Potvrzovací testování v USA je k dispozici pouze u CDC a několika specializovaných referenčních laboratořích. V fatálních případech může být užitečná amplifikace nukleových kyselin a virová kultura pitevních tkání. Virový antigen může být v tkáních prokázán pomocí barvení nepřímými fluorescenčními protilátkami.[8]
Prevence
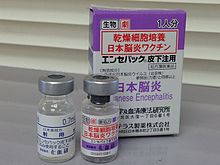
Infekce japonskou encefalitidou je celoživotní imunita. V současné době existují tři vakcíny dostupné: SA14-14-2, IXIARO (IC51, také prodáváno v Austrálii, na Novém Zélandu jako JESPECT a v Indii jako JEEV[14]) a ChimeriVax-JE (prodávaný jako IMOJEV).[15] Všechny současné vakcíny jsou založeny na viru genotypu III.
A formalín -aktivovaná vakcína z myšího mozku byla poprvé vyrobena v Japonsku ve 30. letech a byla validována pro použití na Tchaj-wanu v 60. letech a v Thajsku v 80. letech. Rozšířené používání vakcín a urbanizace vedla ke kontrole této choroby v Japonsku, Koreji, na Tchaj-wanu a v Singapuru. Vysoké náklady na tuto vakcínu, která se pěstuje na živých myších, znamenají, že si chudší země nemohly dovolit ji podat jako součást rutinního imunizačního programu.[9]
Mezi nejčastější nežádoucí účinky patří zarudnutí a bolest v místě vpichu. Méně často, an kopřivka reakce se může vyvinout asi čtyři dny po injekci. Vakcíny vyrobené z myšího mozku mají riziko autoimunitní neurologické komplikace kolem 1 na milion očkování.[16] Pokud se však vakcína nevyrábí v mozcích myší, ale in vitro použitím buněčná kultura ve srovnání s placebo, hlavní vedlejší účinky jsou bolest hlavy a myalgie.[17]
Neutralizující protilátka přetrvává v oběhu nejméně dva až tři roky a možná i déle.[18][19] Celková doba ochrany není známa, ale protože neexistují žádné přesvědčivé důkazy o ochraně nad tři roky, posilovače se doporučují každé tři roky lidem, kteří jsou i nadále ohroženi.[20] Kromě toho také nejsou k dispozici žádné údaje týkající se zaměnitelnosti jiných vakcín proti JE a IXIARO.
Léčba
Neexistuje žádná specifická léčba japonské encefalitidy a léčba je podpůrná,[21] s pomocí poskytnutou pro krmení, dýchání nebo záchvat ovládání podle potřeby. Zvednutý nitrolební tlak lze spravovat pomocí mannitol.[22] Tady není žádný přenos z člověka na člověka, a proto pacienti nemusí být izolováni.
Průlomem v oblasti léčby japonské encefalitidy je identifikace makrofág účast receptoru na závažnosti onemocnění. Nedávná zpráva indické skupiny ukazuje zapojení monocyt a makrofág receptor CLEC5A při těžké zánětlivé reakci u mozkové infekce japonskou encefalitidou. Tento transkriptomický studie poskytuje hypotézu o neurozánět a nový náskok ve vývoji vhodných léčivých přípravků proti japonské encefalitidě.[23][24]
Účinnost intravenózní imunoglobulin léčba encefalitidy je nejasná kvůli nedostatku důkazů.[25] Zdá se, že intravenózní imunoglobulin pro japonskou encefalitidu nemá žádný přínos.[25]
Epidemiologie
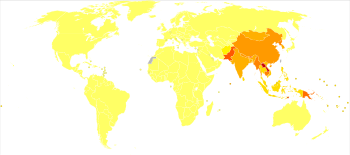
Japonská encefalitida (JE) je hlavní příčinou virové encefalitidy v Asie, s ročním hlášením až 70 000 případů.[26] Míra úmrtnosti se pohybuje od 0,3% do 60% a závisí na populaci a věku. Vyskytly se také vzácné ohniska na území USA v západním Pacifiku. Obyvatelé venkovských oblastí v endemických lokalitách jsou nejvíce ohroženi; Japonská encefalitida se v městských oblastech obvykle nevyskytuje.
Patří sem země, které v minulosti zažily velké epidemie, ale které tuto chorobu zvládly primárně očkováním Čína, Jižní Korea, Japonsko, Tchaj-wan a Thajsko. Mezi další země, které stále mají periodické epidemie, patří Vietnam, Kambodža, Myanmar, Indie, Nepál, a Malajsie. Japonská encefalitida byla hlášena v EU Ostrovy Torres Strait a dva smrtelné případy byly hlášeny na severu pevniny Austrálie v roce 1998. Byly hlášeny případy v Stát Kachin, Myanmar v roce 2013. Šíření viru v Austrálii je obzvláště znepokojeno australskými zdravotníky z důvodu neplánovaného zavedení Culex gelidus, potenciální vektor viru, z Asie. Současná přítomnost na kontinentální Austrálii je však minimální. V Odisině zaostalosti bylo hlášeno 116 úmrtí Malkangiri okres Indie v roce 2016.[Citace je zapotřebí ]
Lidé, dobytek a koně jsou hostitelé ve slepé uličce, protože nemoc se projevuje jako fatální encefalitida. Prasata působí jako zesilující hostitel a mají velmi důležitou roli v epidemiologii nemoci. Infekce u prasat je asymptomatická, s výjimkou březích prasnic, kdy jsou časté potraty a abnormality plodu. Nejdůležitějším vektorem je Culex tritaeniorhynchus, který se přednostně živí dobytkem. Přirozenými hostiteli viru japonské encefalitidy jsou ptáci, nikoli lidé, a mnozí věří, že virus proto nikdy nebude zcela eliminován.[27] V listopadu 2011 byl hlášen virus japonské encefalitidy Culex bitaeniorhynchus v Jižní Korea.[28]
Nedávno celý genom microarray výzkum neurony infikovaní virem japonské encefalitidy prokázali, že neurony hrají důležitou roli v jejich vlastní obraně proti infekci japonskou encefalitidou. I když to zpochybňuje dlouhodobou víru, že neurony jsou imunologicky v klidu, lepší pochopení prozánětlivých účinků odpovědných za imunitní zprostředkování kontroly virové infekce a poškození neuronů během infekce japonskou encefalitidou je zásadním krokem pro vývoj strategií pro omezení závažnosti CNS choroba.[29]
Bylo zkoumáno mnoho léků, které buď snižují replikaci viru, nebo zajišťují neuroprotekci v buněčných liniích nebo ve studiích na myších. Při léčbě lidských pacientů se v současnosti neobhajuje žádný.
- Použití kyselina rosmarinová,[30] arctigenin,[31] a oligosacharidy s stupeň polymerace 6 od Gracilaria sp. nebo Monostroma nitidum[32] prokázáno, že jsou účinné u myšího modelu japonské encefalitidy.
- Kurkumin Bylo prokázáno, že ve studii in vitro poskytuje neuroprotekci proti infekci japonskou encefalitidou. Kurkumin pravděpodobně působí snížením úrovně reaktivních druhů kyslíku v buňkách, obnovením buněk integrita membrány, klesající pro-apoptotický signální molekuly a modulování buněčných hladin proteinů souvisejících se stresem. Bylo také prokázáno, že produkce infekčních virových částic z dříve infikovaných neuroblastom buňky jsou redukovány, čehož je dosaženo inhibicí ubikvitin-proteazomový systém.[33]
- Minocyklin u myší vedlo k výraznému snížení hladin několika markerů, virového titru a hladiny prozánětlivých mediátorů[34] a také brání hematoencefalická bariéra poškození.[35]
Vývoj
Zdá se, že virus pochází z viru předků v polovině 15. století v oblasti Indonésie-Malajsie a vyvinul se tam do pěti různých genotypů a rozšířil se po Asii.[36] Průměrná rychlost evoluce byla odhadnuta na 4,35×10−4 (rozsah: 3,4906×10−4 do 5.303×10−4) nukleotidové substituce na místo za rok.
Reference
- ^ A b C d E F G "Příznaky a léčba". CDC. Srpna 2015. Archivováno z původního dne 17. června 2017. Citováno 29. října 2017.
- ^ A b C d E F G h i j k l m n Ó p q „Japonská encefalitida“. Světová zdravotnická organizace. Prosinec 2015. Archivováno z původního dne 13. července 2017. Citováno 29. října 2017.
- ^ A b „Japonská encefalitida“. CDC. Srpna 2015. Archivováno z původního dne 24. května 2017. Citováno 29. října 2017.
- ^ https://www.nhs.uk/conditions/japanese-encephalitis/causes/
- ^ Moloney, Rachael M .; Kmush, Bretaň; Rudolph, Kara E .; Cummings, Derek A. T .; Lessler, Justin (7. května 2014). „Inkubační období virových infekcí přenášených komáry: systematický přehled“. American Journal of Tropical Medicine and Hygiene. 90 (5): 882–891. doi:10.4269 / ajtmh.13-0403. PMC 4015582. PMID 24639305.
- ^ Simon, LV; Kruse, B (leden 2018). Encefalitida, japonština. StatPearls. PMID 29262148.
- ^ Ghoshal, A; Das, S; Ghosh, S; Mishra, MK; Sharma, V; Koli, P; Sen, E; Basu, A. (2007). „Prozánětlivé mediátory uvolňované aktivovanou mikroglií indukují smrt neuronů u japonské encefalitidy“. Glia. 55 (5): 483–96. doi:10,1002 / glia.20474. PMID 17203475.
- ^ A b Virus japonské encefalitidy Archivováno 18. července 2013 v Wayback Machine přezkoumány a publikovány WikiVet, zpřístupněno 11. října 2011.
- ^ A b Solomon, T. (2006). „Ovládnutí japonské encefalitidy - na dosah?“. New England Journal of Medicine. 355 (9): 869–71. doi:10.1056 / NEJMp058263. PMID 16943399.
- ^ Lobigs M, Diamond MS (2012). „Proveditelnost křížové ochranné vakcinace proti flavivirům sérokomplexu japonské encefalitidy“. Expert Rev vakcíny. 11 (2): 177–87. doi:10.1586 / erv.11.180. PMC 3337329. PMID 22309667.
- ^ He B (březen 2006). „Viry, stres endoplazmatického retikula a reakce interferonu“. Buněčná smrt se liší. 13 (3): 393–403. doi:10.1038 / sj.cdd.4401833. PMID 16397582.
- ^ Su HL, Liao CL, Lin YL (květen 2002). „Infekce virem japonské encefalitidy iniciuje stres endoplazmatického retikula a rozvinutou proteinovou reakci“. J. Virol. 76 (9): 4162–71. doi:10.1128 / JVI.76.9.4162-4171.2002. PMC 155064. PMID 11932381.
- ^ Shrivastva A, Tripathi NK, Parida M, Dash PK, Jana AM, Lakshmana Rao PV (2008). „Srovnání imunosorbentního testu s měrkou spojenou s enzymem a komerčních testů pro detekci specifických protilátek IgM proti viru japonské encefalitidy“. J Postgrad Med. 54 (3): 181–5. doi:10.4103/0022-3859.40959. PMID 18626163.
- ^ „Jeev inaktivovaná japonská vakcína proti encefalitidě spuštěna v Hyderabadu“. pharmabiz.com. 15. září 2012. Archivováno z původního dne 23. října 2012. Citováno 11. ledna 2013.
- ^ Schiøler KL, Samuel M, Wai KL (2007). „Vakcíny pro prevenci japonské encefalitidy“. Cochrane Database Syst Rev (3): CD004263. doi:10.1002 / 14651858.CD004263.pub2. PMC 6532601. PMID 17636750.
- ^ Jelinek T (červenec 2008). „Vakcína proti japonské encefalitidě u cestujících“. Expert Rev vakcíny. 7 (5): 689–93. doi:10.1586/14760584.7.5.689. PMID 18564023. S2CID 34671998.
- ^ Schválení vakcíny EMEA http://www.emea.europa.eu/pdfs/human/opinion/Ixiaro_66231608en.pdf[trvalý mrtvý odkaz ]
- ^ Gambel JM, DeFraites R, Hoke C a kol. (1995). „Vakcína proti japonské encefalitidě: perzistence protilátek až 3 roky po primární dávce se třemi dávkami (písmeno)“. J Infect Dis. 171 (4): 1074. doi:10.1093 / infdis / 171.4.1074. PMID 7706798.
- ^ Kurane I, Takashi T (2000). "Imunogenicita a ochranná účinnost současné inaktivované vakcíny proti japonské encefalitidě proti různým kmenům viru japonské encefalitidy". Vakcína. 18 (Suppl): 33–5. doi:10.1016 / S0264-410X (00) 00041-4. PMID 10821971.
- ^ [1][trvalý mrtvý odkaz ]
- ^ Solomon T, Dung NM, Kneen R, Gainsborough M, Vaughn DW, Khanh VT (2000). „Japonská encefalitida“. Časopis neurologie, neurochirurgie a psychiatrie. 68 (9): 405–15. doi:10.1136 / jnnp.68.4.405. PMC 1736874. PMID 10727474.
- ^ Léčba japonské encefalitidy v eMedicína
- ^ Nimesh Gupta; Vinay Lomash; P.V. Lakshmana Rao (září 2010). "Expresní profil viru japonské encefalitidy vyvolaný neurozánětem a jeho důsledky pro závažnost onemocnění". Journal of Clinical Virology. 49 (1): 04–10. doi:10.1016 / j.jcv.2010.06.009. PMID 20637688.
- ^ Nimesh Gupta; P.V. Lakshmana Rao (březen 2011). „Transkriptomický profil reakce hostitele při infekci virem japonské encefalitidy“. Virology Journal. 8 (92): 92. doi:10.1186 / 1743-422X-8-92. PMC 3058095. PMID 21371334.
- ^ A b Iro, Mildred A .; Martin, Natalie G .; Absoud, Michael; Pollard, Andrew J. (2. října 2017). „Intravenózní imunoglobulin pro léčbu dětské encefalitidy“. Cochrane Database of Systematic Reviews. 10: CD011367. doi:10.1002 / 14651858.CD011367.pub2. ISSN 1469-493X. PMC 6485509. PMID 28967695.
- ^ Campbell GL, Hills SL, Fischer M, Jacobson JA, Hoke CH, Hombach JM, Marfin AA, Solomon T, Tsai TF, Tsu VD, Ginsburg AS (listopad 2011). „Odhadovaný celosvětový výskyt japonské encefalitidy: systematický přehled“. Bull World Health Organ. 89 (10): 766–74. doi:10.2471 / BLT.10.085233. PMC 3209971. PMID 22084515.
- ^ Ghosh D, Basu A (září 2009). Brooker S (ed.). „Japonská encefalitida - patologická a klinická perspektiva“. PLOS Negl Trop Dis. 3 (9): e437. doi:10.1371 / journal.pntd.0000437. PMC 2745699. PMID 19787040.
- ^ Kim, Heung Chul; Terry A. Klein; Ratree Takhampunya; Brian P. Evans; Sirima Mingmongkolchai; Ampornpan Kengluecha; John Grieco; Penny Masuoka; Myung-Soon Kim; Sung-Tae Chong; Jong-Koo Lee a Won-Ja Lee (2011). „Virus japonské encefalitidy u komárů Culicine (Diptera: Culicidae) shromážděných v Daeseongdong, vesnici v demilitarizované zóně Korejské republiky“. Journal of Medical Entomology. 48 (6): 1250–1256. doi:10.1603 / me11091. PMID 22238887.
- ^ Nimesh Gupta; S.R. Santhosh; J. Pradeep Babu; M.M. Parida; P.V. Lakshmana Rao (leden 2010). „Chemokinové profilování buněk myšího neuroblastomu infikovaných virem japonské encefalitidy pomocí mikročipu a RT-PCR v reálném čase: implikace v neuropatogenezi“. Virový výzkum. 147 (1): 107–12. doi:10.1016 / j.virusres.2009.10.018. PMC 7126115. PMID 19896511.
- ^ Swarup V, Ghosh J, Ghosh S, Saxena A, Basu A (září 2007). „Antivirové a protizánětlivé účinky kyseliny rosmarinové v experimentálním myším modelu japonské encefalitidy“. Antimicrob. Agenti Chemother. 51 (9): 3367–70. doi:10.1128 / AAC.00041-07. PMC 2043228. PMID 17576830.
- ^ Swarup V, Ghosh J, Mishra MK, Basu A (březen 2008). „Nová strategie léčby japonské encefalitidy pomocí arctigeninu, rostlinného lignanu“. J. Antimicrob. Chemother. 61 (3): 679–88. doi:10.1093 / jac / dkm503. PMID 18230688.
- ^ Kazłowski B, Chiu YH, Kazłowska K, Pan CL, Wu CJ (srpen 2012). „Prevence infekcí virem japonské encefalitidy nízkým stupněm polymerace sulfatovaných sacharidů z Gracilaria sp. a Monostroma nitidum". Food Chem. 133 (3): 866–74. doi:10.1016 / j.foodchem.2012.01.106.
- ^ Dutta K, Ghosh D, Basu A (květen 2009). „Kurkumin chrání neuronální buňky před smrtí buněk zprostředkovanou virem japonské encefalitidy a také inhibuje tvorbu infekčních virových částic dysregulací systému ubikvitin-proteazom“. J. Neuroimmune Pharmacol. 4 (3): 328–37. doi:10.1007 / s11481-009-9158-2. PMID 19434500. S2CID 24691000.
- ^ Mishra MK, Basu A (červen 2008). „Minocyklin neuroprotektuje, snižuje mikrogliální aktivaci, inhibuje indukci kaspázy 3 a virovou replikaci po japonské encefalitidě“. J. Neurochem. 105 (5): 1582–95. doi:10.1111 / j.1471-4159.2008.05238.x. PMID 18208541.
- ^ Mishra MK, Dutta K, Saheb SK, Basu A (prosinec 2009). „Pochopení molekulárního mechanismu poškození hematoencefalické bariéry v experimentálním modelu japonské encefalitidy: korelace s podáváním minocyklinu jako terapeutického činidla“. Neurochem Int. 55 (8): 717–23. doi:10.1016 / j.neuint.2009.07.006. PMID 19628016. S2CID 26964251.
- ^ Mohammed MA, Galbraith SE, Radford AD, Dove W, Takasaki T, Kurane I, Solomon T (červenec 2011). „Molekulární fylogenetické a evoluční analýzy kmene Muar viru japonské encefalitidy odhalily, že jde o chybějící pátý genotyp“. Infect Genet Evol. 11 (5): 855–62. doi:10.1016 / j.meegid.2011.01.020. PMID 21352956.
externí odkazy
- Centra pro kontrolu a prevenci nemocí Otázky a odpovědi týkající se japonské encefalitidy
- Australské vládní ministerstvo zdravotnictví a stárnutí, Japonská encefalitida, 2012
- Britské ministerstvo zdravotnictví. (2006) Imunizace proti infekční nemoci Kapitola 20: Japonská encefalitida
- Knihovna zdrojů pro japonskou encefalitidu [2]
- CDC Sledování a imunizace japonské encefalitidy - Asie a regiony západního Pacifiku, 2016, MMWR, 9. června 2017, 66 (22); 579–583
- Simon, LV; Kruse, B (leden 2018). Encefalitida, japonština. FL: StatPearls Publishing. PMID 29262148.
