Octacyanomolybdenan draselný (IV) - Potassium octacyanomolybdate(IV) - Wikipedia
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC Oktacyanidomolybdenan draselný (IV) | |
| Ostatní jména Octacyanomolybdenan draselný (IV) | |
| Identifikátory | |
| |
3D model (JSmol ) |
|
PubChem CID |
|
| |
| |
| Vlastnosti | |
| K.4[Mo (CN)8] | |
| Molární hmotnost | 460,47 g / mol (bezvodý) 496,5 g / mol (dihydrát) |
| Vzhled | žlutý prášek |
| Bod tání | > 300 ° C |
| Nebezpečí | |
| Piktogramy GHS |  |
| Signální slovo GHS | Varování |
| H302, H315, H319, H335 | |
| P261, P305 + 351 + 338 | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
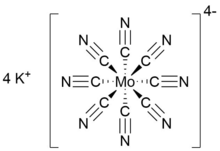
Octacyanomolybdenan draselný (IV) je anorganická sůl vzorce K4[Mo (CN)8]. Je to žlutá pevná látka draselná sůl z homoleptický kyanometalát s koordinační číslo osm. Komplex anion sestává z a molybden kation v oxidační stav IV a osm aniontových kyanid ligandy což vede k celkovému nabít −4, což je vyváženo čtyřmi draslíky kationty. K.4[Mo (CN)8] je často připravován jako dihydrát.
Příprava
Dihydrát K4[Mo (CN)8] · 2 H2O lze připravit redukcí molybdenan (Bučení42-) s borohydrid draselný (KBH4) v řešení s kyanid draselný a octová kyselina.[1] To byla jedna z prvních syntéz, kde molybdenan se snižuje současně s kyanometalát je vytvořen. Výtěžek je obvykle asi 70%. Tato metoda je použitelná pro velké dávky, protože zpracování je efektivnější ve velkém měřítku a výchozí materiály jsou levné.
4 MoO42- + 32 CN− + BH4− + 31 hodin+ → 4 [Mo (CN)8]4- + 16 hodin2O + H3BO3
Molybden má vysokou afinitu k kyslík. Aby se zabránilo štěpení vazby molybdenem na kyslík spotřebovávající energii, začíná alternativní cesta k dihydrátu octacyanomolybdenanu (IV) draselného z MoCl4(Et2Ó)2 přímo z oxidačního stavu IV, takže není nutná žádná redukce. Výnos této cesty je obvykle kolem 70%.[2] Tato syntéza je vhodná pro menší velikosti šarží než dřívější metoda, ale pro MoCl4(Et2Ó)2 je obvykle méně dostupný než molybdenan.
MoCl4(Et2Ó)2 + 8 KCN → K.4[Mo (CN)8] + 4 KCl + 2 Et2Ó
Redox chemie
Jedna elektronová oxidace oktacyanomolybdenanu (IV) vede k paramagnetické octacyanomolybdate (V), což je 17-elektronový komplex používaný v magnetochemie.
Reakce
Protonace [Mo (CN)8]4- v silných kyselinách vede k homoleptice isokyanid vodíku komplex [Mo (CNH)8]4+, společné s mnoha kyanometalát komplexy.[3] Tyto ligandy mohou být substituovány jinými, například H2Ó.
Reference
- ^ J. G. Leipoldt, L. D. C. Bok, P. J. Cilliers, "Příprava dihydrátu oktakyanomolybdenanu draselného", Z. anorg. allg. Chem., 1974, svazek 409, str. 343-44.doi:10.1002 / zaac.19744090310
- ^ G. Handzlik, M. Magott, B. Sielucka, D. Pinkowicz, „Alternativní syntetická cesta k oktakyanidoniobátu draselnému (IV) a jeho molybdenovému kongeneru“, Eur. J. Inorg. Chem., 2016, str. 4872-77.doi:10.1002 / ejic.201600669
- ^ M. Sellin, V. Marvaud, M. Malischewski, „Izolace a strukturní charakterizace osminásobných protonovaných oktacyanometalatů [M (CNH)8]4+ (M = MoIV, ŽIV) from Superacids ", Angew. Chem. Int. Vyd., 2020 svazek 59, str. 10519-10522.doi:10.1002 / anie.202002366
