Haloketon - Haloketone

A haloketon v organická chemie je funkční skupina skládající se z a keton skupina nebo obecněji karbonyl skupina s α-halogen substituent. Obecná struktura je RR'C (X) C (= 0) R, kde R je alkylový nebo arylový zbytek a X kterýkoli z halogenů. Preferovaný konformace haloketonu je to a cisoidní s halogenem a karbonylem sdílející stejnou rovinu jako sterická překážka s karbonylovou alkylovou skupinou je obecně větší.[1]
Syntéza haloketonu
- Haloketony a halogenkarbonylové sloučeniny jsou obecně syntetizovány reakcí karbonyl sloučeniny s halogenačními činidly:
- Halogeny, Brom a chlor dávají monosubstituci, fluor dává polysubstituci
- Tetrabutylamonium tribromid
- N-Bromosukcinimid
- 1,3-Dibrom-5,5-dimethylhydantoin (DBDMH)
- V Hell – Volhard – Zelinsky halogenace A karboxylová kyselina reaguje s bromem v přítomnosti bromid fosforitý.
- V Nierensteinova reakce acylchlorid reaguje s diazomethan
Asymetrická syntéza
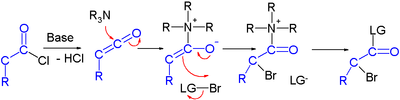
Úsilí je hlášeno v asymetrická syntéza halokarbonylů organokatalýza. V jedné studii chlorid kyseliny se převádí na α-halogen-ester se silnou bází (hydrid sodný ), dárce bromu a organokatalyzátor založený na prolin a chinin:[2]

V navrhovaném mechanismus reakce báze nejprve převede chlorid kyseliny na keten, pak organokatalyzátor zavádí chirality prostřednictvím svého chininoidu terciární amin za vzniku ketenového aduktu.
Haloketonové reakce
Haloketony se účastní několika typů reakcí. V reakci s a nukleofil jsou k dispozici dvě elektrofilní místa a v reakci s a základna několik kyselých protonů existuje kvůli přítomnosti dvou skupiny pro výběr elektronů. Zvyšuje se zkušenost s vazbou uhlík-halogen polarita z indukční účinek karbonylové skupiny, což činí atom uhlíku elektropozitivnějším.
- v nukleofilní alifatická substituce reakce s jodid draselný v aceton, chloraceton reaguje rychleji než 1-chlorpropan faktorem 36 000.
- V Favorskii přesmyk báze abstrahuje nejprve kyselý α-proton a výsledný karbanion pak vytěsní halogen.
- Stejná sekvence je pozorována v Bingelova reakce s fullereny
- V překřížené aldolové reakce mezi haloketony a aldehydy počáteční produkt reakce je a halohydrin který může následně vytvořit oxirane v přítomnosti základny.
- Haloketony jsou důležité v heterocyklická chemie. Příkladem je použití haloketonů v Hantzschova syntéza pyrrolu a Hantzschova syntéza thiazolu.
- Haloketony reagují s fosfity v Perkowova reakce.
- Halogroup lze odstranit v reduktivní dehalogenace halogenketonů
- Historicky bylo ošetření haloketonů zinkovým prachem v Reformatského reakce byla jednou z prvních spolehlivých metod pro generování nestabilizovaného enoláty. Toto bylo do značné míry nahrazeno základnami jako lithium diisopropylamid.
Viz také
Reference
- ^ Erian, Ayman W .; Sherif, Sherif M .; Gaber, Hatem M. (2003). "Chemie a-haloketonů a jejich využití v heterocyklické syntéze" (PDF). Molekuly. 8: 793–865.
- ^ Dogo-Isonagie, Cajetan; Bekele, Tefsit; Francie, Stefan; Wolfer, Jamison; Weatherwax, Anthony; Taggi, Andrew E .; Lectka, Thomas (2006). „Škálovatelná metodika pro katalytickou, asymetrickou α-bromaci chloridů kyselin“. Journal of Organic Chemistry. 71 (23): 8946–8949. doi:10.1021 / jo061522l.
