Favorskii přesmyk - Favorskii rearrangement
| Favorskii přesmyk | |
|---|---|
| Pojmenoval podle | Alexej Yevgrafovič Favorskii |
| Typ reakce | Reakce přesmyku |
| Identifikátory | |
| Portál organické chemie | favorsky reakce |
| RSC ontologické ID | RXNO: 0000385 |
The Favorskii přesmyk, pojmenovaný pro ruského chemika Alexej Yevgrafovič Favorskii, je hlavně přestavbou cyklopropanony a α-halogenketony což vede k karboxylová kyselina deriváty. V případě cyklických α-haloketonů představuje Favorskiiho přeskupení prstencovou kontrakci. K tomuto přeskupení někdy dochází v přítomnosti základny hydroxid, čímž se získá karboxylová kyselina, ale většinou buď alkoxid základna nebo amin výtěžek ester nebo amide, resp. α, α’-dihaloketony eliminují HX za reakčních podmínek za vzniku α, β-nenasycených karbonylových sloučenin.[1][2][3][4][5][6][7][8]
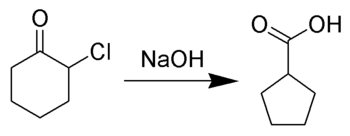
Reakční mechanismus
The mechanismus reakce Předpokládá se, že zahrnuje vytvoření izolovat na straně keton daleko od chlór atom. Toto enolát cyklizuje na a cyklopropanon meziprodukt, který je poté napaden hydroxidem nukleofil.

Druhý krok byl také navržen jako postupný proces, kdy chloridový anion nejprve opustil, aby vytvořil zwitteriontový oxyallylový kation, než dojde k uzavření disrotatického elektrocyklického kruhu, aby se získal meziprodukt cyklopropanonu.[9]
Využití alkoxid anionty, jako je methoxid sodný, místo hydroxidu sodného, dávají prsten kontrakci ester produkt.
Když je tvorba enolátu nemožná, dochází k přeskupení Favorskii alternativním mechanismem, při kterém dochází k přídavku hydroxidu ke ketonu, po kterém následuje společné zhroucení čtyřboký meziprodukt a migrace sousedního uhlíku s vytěsněním halogenidu. Toto je někdy známé jako pseudo-Favorskii přesmyk, i když před studiemi označování se předpokládalo, že všechny přesmyky Favorskii probíhaly prostřednictvím tohoto mechanismu.
 |
| Animace reakčního mechanismu |
Valašská degradace
V souvisejícím Valašská degradace (Otto Wallach, 1918) ne jeden, ale dva atomy halogenu lemují keton, což vede k novému smrštěnému ketonu po oxidaci a dekarboxylace[10][11]
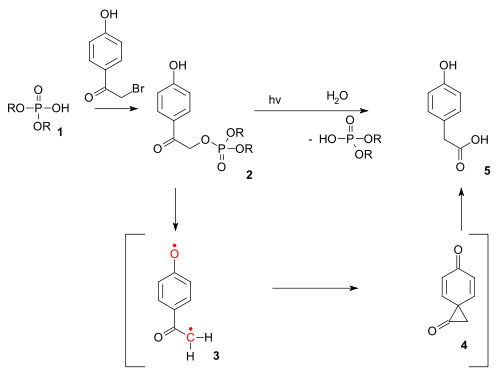
Foto-Favorskii reakce
Typ reakce také existuje jako fotochemická reakce. The foto-Favorskii reakce byl použit při fotochemickém odblokování určitých fosfáty (například z ATP ) chráněný tzv p-hydroxyfenacyl skupiny.[12] Odstranění chránící skupiny probíhá prostřednictvím tripletu diradical (3) a a dione spiro středně pokročilí (4), i když se tento druh detekce zatím vyhýbal.[13]
Viz také
- Klasika kubánský syntéza obsahuje dva Favorskii přesmyky.
- Trimethylenemethanová cykloadice, který může postupovat podobným mechanismem
Reference
- ^ Favorskii, A. E. (1894). J. Russ. Phys. Chem. Soc. 26: 590. Chybějící nebo prázdný
| název =(Pomoc) - ^ Favorskii, A. E. (1905). J. Russ. Phys. Chem. Soc. 37: 643. Chybějící nebo prázdný
| název =(Pomoc) - ^ Faworsky, A. Y. (1913). „Über die Einwirkung von Phosphorhalogenverbindungen auf Ketone, Bromketone und Ketonalkohole“. J. Prakt. Chem. (v němčině). 88 (1): 641–698. doi:10.1002 / prac.19130880148.
- ^ Cope, Artur (1960). Organická reakce Objem XI (1. vyd.). New York: Wiley-Interscience. doi:10,1002 / jps. 2600500225. ISBN 9780471171270.
- ^ Wohllebe, J .; Garbisch, E. W. (1977). „Prstencová kontrakce přes přeskupení typu Favorskii: Cykloundecanone ". Organické syntézy. 56: 107. doi:10.15227 / orgsyn.056.0107.; Kolektivní objem, 6, str. 368
- ^ Shioiri, Takayuki; Kawai, Nobutaka (1978). "Nové metody a činidla v organické syntéze. 2. Jednoduchá přeměna alkylarylketonů na a-arylalkanové kyseliny pomocí difenylfosforazidátu. Jeho aplikace na novou syntézu ibuprofenu a naproxenu, nesteroidních protizánětlivých látek." J. Org. Chem. 43 (14): 2936–2938. doi:10.1021 / jo00408a049.
- ^ Hamada, Yasumasa; Shioiri, Takayuki (1982). "Cycloundecanecarboxylic Acid". Organické syntézy. 62: 191. doi:10.15227 / orgsyn.062.0191.; Kolektivní objem, 7, str. 135
- ^ Goheen, D. W .; Vaughan, W. R. (1963). „Methylester kyseliny cyklopentankarboxylové“. Organické syntézy. 39: 37. doi:10.15227 / orgsyn.039.0037.; Kolektivní objem, 4, str. 594
- ^ Akhrem, AA; Ustynyuk, T K; Titov, Yu A (30. září 1970). "Favorskii přesmyk". Ruské chemické recenze. 39 (9): 732–746. doi:10.1070 / rc1970v039n09abeh002019. ISSN 0036-021X.
- ^ Wallach, O. (1918). „Zur Kenntnis der Terpene und der ätherischen Öle. Über das Verhalten zweifach gebromter hexacyclischer Ketone v Abhängigkeit von der Stellung der Bromatome“. Justus Liebigs Ann. Chem. (v němčině). 414 (3): 271–296. doi:10,1002 / jlac.19184140303.
- ^ Wallach, O. (1918). „Zur Kenntnis der Terpene und der ätherischen Öle“. Justus Liebigs Ann. Chem. (v němčině). 414 (3): 296–366. doi:10,1002 / jlac.19184140304.
- ^ Park, Chan-Ho; Givens, Richard S. (1997). "Nové fotoaktivované ochranné skupiny. 6. str-Hydroxyfenacyl: Phototrigger pro chemické a biochemické sondy “. J. Am. Chem. Soc. 119 (10): 2453–2463. doi:10.1021 / ja9635589.
- ^ Givens, Richard S .; Heger, Dominik; Hellrung, Bruno; Kamdžilov, Yavor; Mac, Marek; Conrad, Peter G .; Cope, Elizabeth; Lee, Jong I .; Mata-Segreda, Julio F .; Schowen, Richard L .; Wirz, Jakob (2008). „Photo-Favorskii reakce z str-Hydroxyfenacylové sloučeniny se iniciují adiabatickým vytlačováním tripletového biradikálu za pomoci vody “. J. Am. Chem. Soc. 130 (11): 3307–3309. doi:10.1021 / ja7109579. PMC 3739295. PMID 18290649.