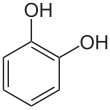
Katechol - Catechol
| |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC Benzen-1,2-diol[1] | |||
| Ostatní jména | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| 471401 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Informační karta ECHA | 100.004.025 | ||
| Číslo ES |
| ||
| 2936 | |||
| KEGG | |||
PubChem CID | |||
| Číslo RTECS |
| ||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| Vlastnosti | |||
| C6H6Ó2 | |||
| Molární hmotnost | 110.112 g · mol−1 | ||
| Vzhled | bílé až hnědé peřové krystaly | ||
| Zápach | slabý fenolový zápach | ||
| Hustota | 1,344 g / cm3, pevný | ||
| Bod tání | 105 ° C (221 ° F; 378 K) | ||
| Bod varu | 245,5 ° C (473,9 ° F; 518,6 K) (sublimuje) | ||
| 430 g / l | |||
| Rozpustnost | velmi rozpustný v pyridin rozpustný v chloroform, benzen, CCl4, éter, ethylacetát | ||
| log P | 0.88 | ||
| Tlak páry | 20 Pa (20 ° C) | ||
| Kyselost (strK.A) | 9.45, 12.8 | ||
| −6.876×10−5 cm3/ mol | |||
Index lomu (nD) | 1.604 | ||
| 2.62±0.03 D [2] | |||
| Struktura | |||
| monoklinický | |||
| Nebezpečí | |||
| Bezpečnostní list | Sigma-Aldrich | ||
| Piktogramy GHS |    | ||
| Signální slovo GHS | Nebezpečí | ||
| H301, H311, H315, H317, H318, H332, H341 | |||
| P261, P301, P330, P331, P310, P302, P352, P312, P305, P351, P338, P310 | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | 127 ° C (261 ° F; 400 K) | ||
| 510 ° C (950 ° F; 783 K) | |||
| Výbušné limity | 1.4%–?[3] | ||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
LD50 (střední dávka ) | 300 mg / kg (potkan, orálně) | ||
| NIOSH (Limity expozice USA pro zdraví): | |||
PEL (Dovolený) | žádný[3] | ||
REL (Doporučeno) | TWA 5 ppm (20 mg / m3) [kůže][3] | ||
IDLH (Okamžité nebezpečí) | N.D.[3] | ||
| Související sloučeniny | |||
Příbuzný benzendioly | Resorcinol Hydrochinon | ||
Související sloučeniny | 1,2-benzochinon | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Katechol (/ˈk…tɪtʃɒl/ nebo /ˈk…tɪkɒl/), také známý jako pyrokatechol nebo 1,2-dihydroxybenzen, je toxická organická sloučenina s molekulárním vzorcem C.6H4(ACH)2. To je ortho izomer ze tří izomerních benzendioly. Tato bezbarvá sloučenina se přirozeně vyskytuje ve stopových množstvích. Poprvé to objevil destruktivní destilace rostlinného extraktu katechin. Asi 20 000 tun katecholu se nyní ročně synteticky vyrábí jako komoditní organická chemikálie, hlavně jako předzvěst pesticidů, příchutí a vonných látek.
Katechol se vyskytuje ve formě bílých krystalů, které jsou velmi rychle rozpustné ve vodě.
Izolace a syntéza
Catechol byl poprvé izolován v roce 1839 Edgarem Hugo Emilem Reinschem (1809–1884) destilací z pevného tříslovinového přípravku katechin, což je reziduum katechu, vařená nebo koncentrovaná šťáva z Mimosa catechu (Acacia catechu ).[4] Po zahřátí katechinu nad jeho bodem rozkladu byla látka, kterou Reinsch poprvé pojmenoval Brenz-Katechusäure (spálená kyselina katechu) sublimovaná jako bílý výkvět. Jednalo se o produkt tepelného rozkladu flavanolů v katechinu. V roce 1841 Wackenroder i Zwenger nezávisle znovuobjevili katechol; při podávání zpráv o svých zjištěních, Filozofický časopis vymyslel jméno pyrokatechin.[5] Do roku 1852, Erdmann si uvědomil, že katechol je benzen se dvěma přidanými atomy kyslíku; v roce 1867, August Kekulé si uvědomil, že katechol je a diol benzenu, takže do roku 1868 byl katechol uveden jako pyrokatechol.[6] V roce 1879 Journal of the Chemical Society doporučil, aby se katechol nazýval „katechol“, a v následujícím roce byl jako takový uveden.[7]
Od té doby se ukázalo, že katechol se přirozeně vyskytuje ve volné formě kino a v Bukové dřevo dehet. Své kyselina sulfonová byl zjištěn v moč koní a lidí.[8]
Katechol se průmyslově vyrábí hydroxylací fenol použitím peroxid vodíku.[9]
- C6H5OH + H2Ó2 → C.6H4(ACH)2 + H2Ó
Dříve se vyráběl hydroxylací salicylaldehydu za použití peroxid vodíku,[10] stejně jako hydrolýza 2-substituovaných fenolů, zejména 2-chlorfenol s horkými vodnými roztoky obsahujícími hydroxidy alkalických kovů. Jeho methyletherový derivát, guajakol, konvertuje na katechol hydrolýzou CH3-O vazba, jak ji propaguje kyselina jodovodíková.[10]
Reakce
Organická chemie
Stejně jako ostatní difunkční benzenové deriváty katechol snadno kondenzuje za vzniku heterocyklické sloučeniny. Cyklický estery vznikají po zpracování dichlorem elektrofily. Například pomocí chlorid fosforitý nebo oxychlorid fosforitý dává cyklický chlorfosfonit nebo chlorfosfonát, v uvedeném pořadí; sulfurylchlorid dává síran; a fosgen dává uhličitan:
- C6H4(ACH)2 + XCl2 → C.6H4(Ó2X) + 2 HCl
- kde X = PCl nebo P (0) Cl; TAK2; CO.
Produkují katecholy chinony s přidáním ceričnan amonný (UMĚT).
S kovovými ionty
Katechol je konjugovaná kyselina chelatačního činidla široce používaného v koordinační chemie. Základní roztoky katecholu reagují se železem (III) za vzniku červeného [Fe (C.6H4Ó2)3]3−. Chlorid železitý dává vodnému roztoku zelené zbarvení, zatímco alkalický roztok se po vystavení vzduchu rychle mění na zelené a nakonec na černé zabarvení.[11] Obsahující železo dioxygenáza enzymy katalyzují štěpení katecholu.
Redoxní chemie
Katechol se vyrábí reverzibilní redukcí dvou elektronů, dvou protonů 1,2-benzochinon (E° = +795 mV vs. ONA; Em (pH 7) = +380 mV vs SHE).[12][13]
Redoxní série katecholát dianion, monoaniontový semichinonát a benzochinon se souhrnně nazývají dioxoleny. Dioxoleny se používají jako ligandy.[14]
Přirozené výskyty
Malé množství katecholu se přirozeně vyskytuje v ovoce a zelenina spolu s enzymem polyfenol oxidáza (také známá jako katecholáza nebo katechol oxidáza). Po smíchání enzymu se substrátem a vystavení kyslíku (jako když a brambor nebo jablko je vyříznut a vynechán), bezbarvý katechol oxiduje na červenohnědé melanoidové pigmenty, deriváty benzochinonu. Enzym se inaktivuje přidáním kyseliny, jako je kyselina citronová obsaženo v citronová šťáva. Vyloučení kyslíku také brání hnědnutí reakce. Aktivita enzymu se však zvyšuje při nižších teplotách. Benzochinon se říká, že je antimikrobiální vlastnost, která zpomaluje znehodnocení poškozených plodů a jiných částí rostlin.
Je to jeden z hlavních přírodních fenolů v arganový olej,[Citace je zapotřebí ] a je součástí castoreum, látka z ricinového žlázy bobři, použito v parfumerie. To je také nalezené v Agaricus bisporus.[15]
Přítomnost katecholového zbytku
Katechol skupiny se také široce vyskytují v přírodním světě. Členovci pokožka skládá se z chitin spojeno katecholem skupina na protein. Kůže může být zesílena zesíťováním (opalování a sklerotizace ), zejména v hmyz a samozřejmě tím biomineralizace.[16] Katecholy jako např DHSA jsou produkovány prostřednictvím metabolismu cholesterol bakteriemi, jako jsou Mycobacterium tuberculosis.[17]
Urushioly jsou přirozeně existující organické sloučeniny, které mají strukturu kostry katecholu a funkčnost difenolu, ale s alkyl skupiny substituované na aromatickém kruhu. Urushioly dráždí pokožku jedy nalezený v rostlinách jako jedovatý břečťan, atd.
Katecholaminy jsou biochemicky významné fenethylamin hormony a neurotransmitery ve kterém fenyl skupina má strukturu kostry katecholu.
Molekula katechin, další přírodní sloučenina přítomná v čaj, obsahuje skupinu katecholu.
Použití
Přibližně 50% syntetického katecholu se spotřebuje při výrobě pesticidů, zbytek se používá jako předzvěst jemných chemikálií, jako jsou parfémy a farmaceutika.[9] Jedná se o běžný stavební blok v organická syntéza.[18] Z katecholu se připravuje několik průmyslově významných příchutí a vůní. Guaiacol se připravuje methylací katecholu a poté se převádí na vanilin v měřítku asi 10 milionů kg ročně (1990). Příbuzný monoethylether katecholu, guethol, je převeden na ethylvanilin, součást čokoládových cukrovinek. 3-Trans-Isocamphylcyclohexanol, široce používaný jako náhrada za santalového oleje, se připravuje z katecholu přes guajakol a kafr. Piperonal, květinová vůně, se připravuje z methylenového dietheru katecholu s následnou kondenzací s glyoxal a dekarboxylace.[19]
Katechol se používá jako černobílý fotografický vývojář, ale až na některé speciální aplikace je jeho použití do značné míry historické. Říká se, že byl krátce použit ve vývojáři Eastman Kodak HC-110 a říká se, že je součástí vývojáře Tetenal Neofin Blau.[20] Je klíčovou součástí společnosti Finol od společnosti Moersch Photochemie v Německu. Průkopníkem vývoje moderního katecholu byl známý fotograf Sandy King. Jeho formulace „PyroCat“ je oblíbená mezi moderními černobílými filmovými fotografy.[21] Kingova práce od té doby inspirovala další vývoj 21. století dalšími, jako je Jay De Fehr s vývojáři Hypercat a Obsidian Acqua a dalšími.[20]
Deriváty katecholu
Kostra katecholu se vyskytuje v různých přírodních produktech, jako jsou urushioly, které dráždí pokožku jedy nalezený v rostlinách jako jedovatý břečťan, a katecholaminy, léky, které je napodobují (např MDMA ), hormony /neurotransmitery, a katechin, který se nachází v čaj. Pro terapeutické aplikace bylo navrženo mnoho derivátů pyrokatechinu.
Nomenklatura
Ačkoli se setkal jen zřídka, oficiálně „upřednostňoval IUPAC name "(PIN) katecholu je benzen-1,2-diol.[22]Triviální jméno pyrokatechol je zachovaný název IUPAC podle Doporučení 1993 pro nomenklaturu organické chemie.[23][24]
Viz také
Reference
- ^ A b „Přední záležitost“. Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 691. doi:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Lander, John J .; Svirbely, W. J. (1945). „Dipólové momenty katecholu, resorcinolu a hydrochinonu“. Journal of the American Chemical Society. 67 (2): 322–324. doi:10.1021 / ja01218a051.
- ^ A b C d NIOSH Kapesní průvodce chemickými nebezpečími. "#0109". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ Hugo Reinsch (1839) „Einige Bemerkungen über Catechu“ (Některá pozorování o catechu), Repertorium für die Pharmacie, 68 : 49-58. Reinsch popisuje přípravu katecholu na str. 56: „Bekanntlich wird die Katechusäure bei der Destillation zerstört, während sich ein geringer Theil davon als krystallinischer Anflug sublimirt, welcher aber noch nicht näher untersucht worden ist. Diese Säure ist vielleicht dieselbe, welche ich bei der (Jak je dobře známo, kyselina katechu je destilací zničena, zatímco její malá část sublimuje jako krystalický výkvět, který však ještě nebyl podrobně prozkoumán. Tato kyselina je možná stejná, kterou jsem získal destruktivní destilací katechu ;…). Na str. 58, Reinsch pojmenoval novou sloučeninu: „Die Eigenschaften dieser Säure sind so bestimmt, dass man sie füglich als eine eigenthümliche Säure betrachten und sie mit dem Namen Brenz-Katechusäure belegen kann.“ (Vlastnosti této kyseliny jsou tak jednoznačné, že ji lze oprávněně považovat za podivnou kyselinu a dát jí název „spálená kyselina katechu“.)
- ^ Vidět:
- H. Wackenroder (1841) „Eigenschaften der Catechusäure“ (Vlastnosti kyseliny katechové), Annalen der Chemie und Pharmacie, 37 : 306-320.
- Constantin Zwenger (1841) „Ueber Catechin“ (Na katechinu), Annalen der Chemie und Pharmacie, 37 : 320-336.
- (Anon.) (1841) „Na katechin (kyselina katechinová) a pyrokatechin (kyselina pyrokatechinová)“, Filozofický časopis, 19 : 194-195.
- ^ Vidět:
- Rudolf Wagner (1852) „Ueber die Farbstoffe des Gelbholzes (Morus tinctoria.)“ (Na barvivu moruši Dyerovy (Morus tinctoria.)), Journal für praktische Chemie, 55 : 65-76. Prosáknout. 65.
- August Kekulé (1867) „Ueber die Sulfosäuren des Phenols“ (O sulfonátech fenolu) Zeitschrift für Chemie, nová série, 3 : 641-646; prosáknout. 643.
- Joseph Alfred Naquet s Williamem Cortisem, trans. a Thomas Stevenson, ed., Principy chemie, založené na moderních teoriích(Londýn, Anglie: Henry Renshaw, 1868), str. 657. Viz také str. 720.
- ^ Vidět:
- V roce 1879 Výbor pro publikace Journal of the Chemical Society vydal pokyny svým abstraktorům „Rozlišovat všechny alkoholy, tj. hydroxylové deriváty uhlovodíků, názvy končícími na ol, např., chinol, katechol,… “Viz: Alfred H. Allen (20. června 1879) „Nomenklatura organických těl“ Anglický mechanik a svět vědy, 29 (743) : 369.
- William Allen Miller, ed., Prvky chemie: Teoretické a praktické, Část III: Chemie uhlíkových sloučenin nebo organická chemie, Oddíl I… , 5. vyd. (Londýn, Anglie: Longmans, Green and Co., 1880), 524.
- ^ Zheng, L. T .; Ryu, G. M .; Kwon, B. M .; Lee, W. H .; Suk, K. (2008). „Protizánětlivé účinky katecholů v buňkách mikroglie stimulovaných lipopolysacharidy: Inhibice mikrogliální neurotoxicity“. European Journal of Pharmacology. 588 (1): 106–13. doi:10.1016 / j.ejphar.2008.04.035. PMID 18499097.
- ^ A b Fiegel, Helmut et al. (2002) „Fenolové deriváty“ v Ullmann's Encyclopedia of Industrial Chemistry„Wiley-VCH: Weinheim. doi:10.1002 / 14356007.a19_313.
- ^ A b „www.orgsyn.org/demo.aspx?prep=CV1P0149“. www.orgsyn.org. Citováno 2016-11-17.
- ^ Anderson, Bryan F .; Buckingham, David A .; Robertson, Glen B .; Webb, John; Murray, Keith S .; Clark, Paul E. (1976). "Modely pro bakteriální chelátový enterochelin transportující železo". Příroda. 262 (5570): 722–724. Bibcode:1976Natur.262..722A. doi:10.1038 / 262722a0. PMID 134287.
- ^ Horner, Leopold; Geyer, Ekkehard (1965). „Zur Kenntnis der Ó-Chinone, XXVII: Redoxpotentiale von Brenzcatechin-Derivaten ". Chemische Berichte. 98 (6): 2016–2045. doi:10.1002 / cber.19650980641.
- ^ Nematollahi, D .; Rafiee, M. (01.05.2004). „Elektrochemická oxidace katecholů v přítomnosti acetylacetonu“. Journal of Electroanalytical Chemistry. 566 (1): 31–37. doi:10.1016 / j.jelechem.2003.10.044.
- ^ Griffith, W. P. (1993). "Nedávný pokrok v chemii dioxolenu". Chemie přechodových kovů. 18 (2): 250–256. doi:10.1007 / BF00139966.
- ^ Delsignore, A; Romeo, F; Giaccio, M (1997). "Obsah fenolických látek v bazidiomycetách". Mykologický výzkum. 101 (5): 552–6. doi:10.1017 / S0953756296003206.
- ^ Briggs DEG (1999). „Molekulární taphonomie živočišných a rostlinných kůžiček: selektivní konzervace a diageneze“. Filozofické transakce Královské společnosti B: Biologické vědy. 354 (1379): 7–17. doi:10.1098 / rstb.1999.0356. PMC 1692454.
- ^ PDB: 2ZI8; Yam KC, D'Angelo I, Kalscheuer R, Zhu H, Wang JX, Snieckus V, Ly LH, Converse PJ, Jacobs WR, Strynadka N, Eltis LD (březen 2009). „Studie dioxygenázy štěpící kruh, osvětlují úlohu metabolismu cholesterolu v patogenezi Mycobacterium tuberculosis.“. PLoS Pathog. 5 (3): e1000344. doi:10.1371 / journal.ppat.1000344. PMC 2652662. PMID 19300498.
- ^ Barner, B. A. (2004) „Catechol“ v Encyklopedie činidel pro organickou syntézu (Ed. L. Paquette), J. Wiley & Sons, New York. doi:10.1002 / 047084289X.
- ^ Fahlbusch, Karl-Georg et al. (2003) "Flavors and Fragrances" v Ullmann's Encyclopedia of Industrial Chemistry„Wiley-VCH: Weinheim doi:10.1002 / 14356007.a11_141.
- ^ A b Stephen G. Anchell (10.09.2012). Temná komora kuchařka. ISBN 978-1136092770.
- ^ Stephen G. Anchell; Bill Troop (1998). Kuchařská kniha o vývoji filmu. ISBN 978-0240802770.
- ^ Preferovaná jména IUPAC. Září 2004, kapitola 6, oddíl 60–64, s. 40 38
- ^ IUPAC, Komise pro nomenklaturu organické chemie. Průvodce nomenklaturou organických sloučenin IUPAC (doporučení 1993) R-5.5.1.1 Alkoholy a fenoly.
- ^ Panico, R .; Powell, W. H., eds. (1994). Průvodce nomenklaturou organických sloučenin IUPAC 1993. Oxford: Blackwell Science. ISBN 978-0-632-03488-8.
![]() Tento článek včlení text z publikace nyní v veřejná doména: Chisholm, Hugh, ed. (1911). "Katechu ". Encyklopedie Britannica (11. vydání). Cambridge University Press.
Tento článek včlení text z publikace nyní v veřejná doména: Chisholm, Hugh, ed. (1911). "Katechu ". Encyklopedie Britannica (11. vydání). Cambridge University Press.