Isoamylacetát - Isoamyl acetate
 | |
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC 3-methylbutylacetát | |
| Systematický název IUPAC 3-methylbutyl ethanoát | |
| Ostatní jména Isopentylacetát Isopentyl ethanoát Isoamylacetát Banánový olej Esence hrušky | |
| Identifikátory | |
3D model (JSmol ) | |
| 1744750 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.004.240 |
| Číslo ES |
|
| 101452 | |
| KEGG | |
PubChem CID | |
| Číslo RTECS |
|
| UNII | |
| UN číslo | 1104 1993 |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C7H14Ó2 | |
| Molární hmotnost | 130.187 g · mol−1 |
| Vzhled | Bezbarvá kapalina |
| Zápach | Jako banán[1] |
| Hustota | 0,876 g / cm3 |
| Bod tání | -78 ° C (-108 ° F, 195 K) |
| Bod varu | 142 ° C (288 ° F; 415 K) |
| 0.3% (20 ° C)[1] | |
| Tlak páry | 4 mmHg nebo 0,533 kPa (20 ° C)[1] |
| −89.4·10−6 cm3/ mol | |
Index lomu (nD) | 1,4020 při 20 ° |
| Nebezpečí | |
| Piktogramy GHS |   |
| Signální slovo GHS | Nebezpečí |
| H226, H315, H319, H335, H336, H372 | |
| P210, P233, P240, P241, P242, P243, P260, P261, P264, P270, P271, P280, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P312, P314, P321, P332 + 313, P337 + 313, P362, P370 + 378, P403 + 233, P403 + 235 | |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | 25 ° C (77 ° F; 298 K) |
| Výbušné limity | 1.0% (100 ° C) - 7,5%[1] |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
LD50 (střední dávka ) | 7422 mg / kg (králík, orální) 16,600 mg / kg (potkan, orálně)[2] |
LChle (nejnižší publikováno ) | 6470 ppm (kočka)[2] |
| NIOSH (Limity expozice USA pro zdraví): | |
PEL (Dovolený) | TWA 100 ppm (525 mg / m3)[1] |
REL (Doporučeno) | TWA 100 ppm (525 mg / m3)[1] |
IDLH (Okamžité nebezpečí) | 1000 ppm[1] |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Isoamylacetát, také známý jako isopentylacetát, je organická sloučenina toto je ester vytvořen z isoamylalkohol a octová kyselina. Je to bezbarvá kapalina, která je jen málo rozpustná ve vodě, ale velmi snadno rozpustná ve většině organických rozpouštědel. Isoamylacetát má silný zápach, který je popsán jako podobný oběma banán a hruška.[3] Čistý isoamylacetát nebo směsi isoamylacetátu, amylacetát a další příchutě lze označit jako Banánový olej.[4]
Výroba
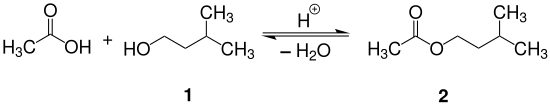
Isoamylacetát se připravuje kyselinou katalyzovanou reakcí (Fischerova esterifikace ) mezi isoamylalkohol a ledové octová kyselina jak je uvedeno v reakční rovnici níže. Typicky, kyselina sírová se používá jako katalyzátor. Alternativně, p-toluensulfonová kyselina nebo může být jako katalyzátor použita kyselá iontoměničová pryskyřice.
Aplikace
Isoamylacetát se používá k udělení banánové chuti v potravinách. Banánový olej běžně označuje roztok isoamylacetátu v ethanol který se používá jako umělá příchuť.
Používá se také jako solventní pro některé laky a nitrocelulózové laky. Jako rozpouštědlo a nosič pro materiály, jako je nitrocelulóza, to bylo široce používán v leteckém průmyslu pro vyztužení a větru odolné textilie létající povrchy, kde to a jeho deriváty byly obecně známé jakodroga letadla '. Nyní, když je většina letadel celokovová, je nyní jejich použití většinou omezeno na historicky přesné reprodukce a zmenšené modely.
Díky své intenzivní, příjemné vůni a nízké toxicitě se k testování účinnosti používá isoamylacetát respirátory nebo plynové masky.[5]
Výskyt v přírodě
Isoamylacetát se přirozeně vyskytuje v banán rostlina[6] a vyrábí se také synteticky.[7]
Isoamylacetát je uvolňován a včelí med je bodnutí aparát, kde slouží jako a feromon maják přilákat další včely a vyprovokovat je k bodnutí.[8]
Reference
- ^ A b C d E F G Kapesní průvodce chemickými riziky NIOSH. "#0347". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ A b "Isoamyl acetát". Koncentrace bezprostředně nebezpečné pro život a zdraví (IDLH). Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ "Iso-amylacetát". chemicalland21.com.
- ^ Karl-Georg Fahlbusch, Franz-Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe, Horst Surburg „Příchutě a vůně“ v Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2002. doi:10.1002 / 14356007.a11_141.
- ^ „Procedury zkoušení způsobilosti (povinné). - 1910.134 App A | Správa bezpečnosti a ochrany zdraví při práci“. www.osha.gov. Citováno 2020-02-04.
- ^ McGee, Harold (2003). O jídle a vaření. New York: Scribner.
- ^ Isoamyl acetát Archivováno 2010-05-28 na Wayback Machine, Správa bezpečnosti a ochrany zdraví při práci
- ^ Boch R; Shearer DA; Stone BC (8. září 1962). „Identifikace isoamylacetátu jako aktivní složky v bodavém feromonu včely medonosné“. Příroda. Anglie: Nature Publishing Group. 195 (4845): 1018–20. doi:10.1038 / 1951018b0. PMID 13870346.