Objev a vývoj inhibitorů NS5A - Discovery and development of NS5A inhibitors

Nestrukturální protein 5A Inhibitory (NS5A) jsou přímo působící antivirová činidla (DAA), která cílí virové proteiny a jejich vývoj byl vyvrcholením zvýšeného porozumění virový životní cyklus v kombinaci s pokrokem v technologii objevování drog.[1][2] Nicméně, jejich mechanismus účinku je složitá a není plně pochopena.[2] Inhibitory NS5A byly středem pozornosti, když se objevily jako součást první léčebné léčby virus hepatitidy C. (HCV) infekce v roce 2014.[3] Příznivé vlastnosti byly zavedeny prostřednictvím různých strukturálních změn a strukturní podobnosti mezi inhibitory NS5A, které jsou klinicky schválené, jsou snadno patrné.[4][5] Navzdory nedávnému zavedení řady nových antivirotik odpor je stále problém a tyto inhibitory se proto vždy používají v kombinace s jinými léky.[6][7]
Virus hepatitidy C.
HCV je a jednořetězcový RNA virus pozitivního smyslu u kterého bylo prokázáno, že se replikuje v hepatocyty lidí i šimpanzů. Jeden HCV polyprotein je přeložen a poté štěpen buněčnými a virovými proteázy do tří strukturní proteiny (jádro, E1 a E2) a sedm nestrukturální proteiny (str. NS2, NS3, NS4A, NS4B, NS5A a NS5B ).[8][9]
HCV patří mezi hlavní příčiny nemoc jater okolo světa. Přenáší se krví a nejčastěji se stahuje pomocí infikovaných jehel.[10] Pacienti trpící chronickou infekcí HCV jsou významně ohroženi cirhóza a hepatocelulární karcinom, což jsou hlavní příčiny úmrtí infikovaných.[11][12]
Virus existuje již více než tisíc let a byl klasifikován do šesti známých genotypy, z nichž každý obsahuje četné podtypy. Sedmá zůstává necharakterizovaná. Smluvní genotyp určuje, které konkrétní způsoby léčby jsou životaschopné.[13]
NS5A receptor
Základní struktura a chemické vlastnosti
NS5A je velký hydrofilní fosfoprotein který je nezbytný pro životní cyklus HCV a nachází se ve spojení s membránovými vezikuly indukovanými virem, nazývaným membránová síť.[14][15] NS5A je protein bohatý na prolin složený z přibližně 447 aminokyseliny, který je rozdělen do tří domén.[16][17] Tyto domény jsou spojeny dvěma sekvencemi s nízkou složitostí, které jsou buď serine- nebo prolin -bohatý.[18] Doména I je doména vázající zinek a rentgenové krystalografické studie ukázaly alternativní dimerní konformace domény I NS5A.[19][20][21] Doména II a III jsou nestrukturované, což ukazují studie NMR.[16][22] Doméně I předchází doména N-terminál amfipatický spirála což umožňuje, aby se protein spojil s endoplazmatické retikulum - odvozené membrány.[22][23][24] Ačkoli rentgenové krystalografické studie odhalily dimerní konformace domény NS5A1, nedávné studie strukturní charakterizace řešení ukázaly, že proteiny NS5A tvoří struktury vyššího řádu dimerními podjednotkami domény NS5A 1. [25] Kromě toho celkový strukturální model NS5A zdůrazňuje variabilitu vnitřních konformací domén D2 a D3 mezi genotypy HCV.[26] Proto stále probíhá debata o tom, která konformace NS5A je funkční a také cílená inhibitory NS5A.
NS5A existuje hlavně ve dvou odlišných fosforylovaný formy, hypofosforylovaný a hyperfosforylovaný forma, ale přesná funkce fosforylace nebyla stanovena.[17][18][27]
Funkce
Protein NS5A hraje důležitou roli v replikace virové RNA, virové shromáždění a komplexní interakce s buněčnými funkcemi.[2][17] Protein byl zapojen do modulace obrany hostitele, apoptóza, buněčný cyklus, a dráhy reagující na stres.[27] Jeho funkce a úplná struktura však musí být ještě objasněna.[16]
Zdá se, že NS5A je klíčem ke spuštění tvorby membránového pásu v nepřítomnosti jiných podobných nestrukturálních proteinů.[15] Mnoho proteinů v hostitelské buňce může být ovlivněno NS5A, např. fosfatidylinositol 4-kináza IIIα (PI4KIIIα), a kináza potřebné pro replikaci HCV. Tato kináza se účastní biosyntéza z fosfatidylinositol 4-fosfát (PI4P) interakcí s NS5A, který stimuluje jeho aktivitu a zdá se, že zlepšuje integritu membránového pásu.[15][28][29]
V poslední době se díky ústřední roli NS5A při virové proliferaci stalo cílem vývoj léků. V důsledku toho byla zavedena nová antivirová činidla pro léčbu HCV.[2]
Mechanismus účinku
Inhibitory NS5A byly vyvinuty k cílení na protein NS5A. Tyto inhibitory dosáhly významného snížení hladin HCV RNA v krvi, a lze je proto považovat za účinná antivirotika. Jejich mechanismus působení je považován za různorodý, ale přesný mechanismus není zcela objasněn.[2][30] Většina studií předpokládá, že inhibitory NS5A působí ve dvou základních fázích životního cyklu HCV; replikace genomové RNA a shromáždění virionů. Další studie navrhují alteraci faktorů hostitelské buňky jako možný třetí mechanismus.[2][15][31]

Struktura inhibitorů NS5A je charakterizována dimerní symetrie. To naznačuje, že inhibitory NS5A působí na dimery NS5A.[32] Ukázala to řada modelových studií daklatasvir, který je inhibitorem NS5A, se váže pouze na dimer NS5A "back-to-back" a že vazba musí být symetrická. Další modelové studie ukázaly, že je možná vazba na jiné konformace NS5A asymetrické vazba.[30] Výzkum ukázal, že cílem daklatasviru je s největší pravděpodobností doména I NS5A.[31] I když mechanismus není zcela objasněn, bylo prokázáno, že inhibitory downregulate Hyperfosforylace NS5A, která vede k potlačení replikace HCV a jeho zpracování polyproteinů, a vede k neobvyklému umístění proteinu.[31][33] Dosud se předpokládalo, že tato inhibice vyžaduje pouze doménu I NS5A, ale nikoli domény II a III.[33] Nedávné studie však ukázaly, že obě domény I a II jsou relevantní pro toto narušení replikace RNA.[34]
Zdá se, že inhibitory NS5A dále narušují tvorbu nových komplexů replikázy, což vede k postupnému zpomalení syntézy virové RNA. Účinek na dříve vytvořené komplexy ještě musí být prokázán.[34][35]
Dostupné důkazy naznačují, že inhibitory NS5A modifikují umístění NS5A uvnitř buňky. To může způsobit neobvyklé sestavení vedoucí k nesprávně tvarovaným virům.[2] Některé studie odhalily, že inhibice shromáždění virů hraje při redukci RNA důležitější roli než redukce replikace viru.[35][36]
Studie prokázaly, že inhibitory NS5A blokují tvorbu membránového pásu, který chrání viry genom a představuje hlavní weby pro replikaci a shromažďování virů.[15][31][37] Předpokládá se, že tento mechanismus je nezávislý na replikaci RNA, ale zdá se, že je ovlivněn inhibitory NS5A blokujícími tvorbu komplexu PI4KIIIα-NS5A, což je nezbytné pro syntézu PI4P, což má za následek sníženou integritu membránové pavučiny, a proto sníženou HCV RNA replikace.[15][28][38]
Dějiny
Výzkum HCV učinil v posledních letech velký pokrok díky objevu a klinickému vývoji mnoha nových léků proti HCV. Mezi těmito léky jsou DAA, které zahrnují inhibitory NS5A.[39]Bylo zjištěno, že inhibitory NS5A jsou zvláště účinné při léčbě HCV, kde se používají v kombinaci s jinými inhibitory proteázy, jako jsou inhibitory NS5B (např. sofosbuvir ), pegylované interferony (např. peginterferon alfa-2a ) a ribonukleové analogy (např. ribavirin ).[40][41][42] Stále přítomné riziko viru kmeny rozvíjející se odpor je hlavním faktorem, proč se používají v kombinaci s jedním nebo více doplňkovými léky.[43]
Nepříznivé účinky a rozsáhlé a komplikované lékové režimy spojené s nízkou mírou dodržování předpisů byly překážkou ve vývoji antivirové léčby. Kombinace inhibitorů NS5A a NS5B přinesla v tomto ohledu pozitivní výsledky.[44]
Objev a vývoj drog
Objev

Objev inhibitorů NS5A se uskutečnil v kontextu snahy o léčbu HCV. NS5A je mezi sedmi nestrukturálními proteiny, které tvoří komplex s virovou RNA v infikovaných buňkách k zahájení replikace HCV.[45] Výzkum HCV přinesl několik DAA včetně inhibitorů NS3A, NS4A a NS5B a také inhibitorů NS5A.[46]
Rozvoj
Vývoj antivirových léčiv schopných interferovat s proteiny odpovědnými za replikaci viru byl úzce spojen s pokrokem v technikách stanovení účinné buněčná kultura potřebné systémy obrazovka pro ně.[46]
V roce 1999 došlo k průlomu, kdy došlo k úplnému konsensuálnímu genomu naklonovaný Bylo zjištěno, že z HCV RNA se replikuje na vysokých úrovních, když transfektovaný do lidského hepatomu buněčná linie.[47] Tato metoda byla od té doby vylepšena použitím mutací adaptivních na buněčnou kulturu, které zvyšují replikaci RNA.[48]
Screening nyní vytvořil řadu inhibitorů NS5A, které byly začleněny do léčby HCV. První v této nové třídě léků byl daklatasvir, který dostal FDA schválení v roce 2015.[49] Od té doby byly schváleny další léky, mezi nimi zejména ledipasvir, které spolu se sofosbuvirem zahrnují lék na HCV Harvoni.[50][51]
Přestože se inhibitory NS5A ukázaly jako účinné antivirotika, musí být používány společně s doplňkovými antivirotiky kvůli tomu, jak rychle vedou k vývoji rezistentní mutace pokud je uveden jako jediný agent.[52] To formovalo zaměření vývoje inhibitorů NS5A, z nichž asymetrické varianty metabolizovat Kromě jiných objevů se objevily i analogie s komplementárními profily rezistence.[53]
Vztah struktura-aktivita
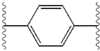
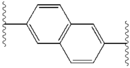
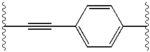
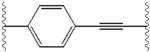
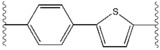
Strukturální podobnosti mezi inhibitory jsou snadno patrné.[4] Přídavky centrálního jádra jsou obvykle symetrické a mají znak imidazol -prolinová struktura.[5] Přírodní L-konfigurace prolin deriváty bylo shledáno kritickým pro inhibici, protože nepřirozené D-konfigurace měl drasticky slabší aktivitu. The potence inhibitorů byla odpovídajícím způsobem citlivá na změny v amin uzavírací prvek. Tato pozorování naznačují, že aminová oblast molekuly hraje důležitou roli v inhibiční aktivitě.[54]
Mezi příznivé vlastnosti inhibitoru NS5A patří vysoká účinnost a dlouhá plazma poločas rozpadu za účelem dosažení dávky jednou denně. Bylo zjištěno, že mírně asymetrické přílohy, jak je vidět v ledipasviru, mají výrazné výhody pro optimalizaci účinnosti inhibitoru a farmakokinetika.[50] Struktura centrálního jádra mění rozteč a projekci příloh, jakož i polohu lipofilita v centrálním jádru, což zejména ovlivňuje inhibiční aktivitu. Struktury s kondenzovanými centrálními kruhy trvale vykazují vyšší inhibiční aktivitu, zatímco méně lipofilní centrální jádra poskytují slabší aktivitu.[4] Symetrické bis-imidazolové struktury, jako je daklatasvir, pociťují ztrátu účinnosti fluoren je nahrazeno pro biaryl skupina. Tato substituce také vede k vážným problémům se stabilitou.[50][55] Menší lipofilní konektor, jako je difluormethylen, však generuje nejúčinnější inhibitor v asymetrické struktuře. Kromě toho poskytuje vylepšené biologická dostupnost a příznivější poločas rozpadu v plazmě. Tam je také pozoruhodné zvýšení účinnosti, když fenyl je nahrazen naftyl jako centrální jádro. Toto zvýšení je významně vyšší u asymetrické struktury než u symetrické struktury.[50][54] V asymetrických strukturách je rozdíl v účinnosti mezi fenyl-alkyn inhibitory prokazuje důležitost polohy lipofilnosti. Centrálněji umístěný alkyn, který je méně lipofilní spojkou než fenyl, zlepšuje účinnost.[4][5][50]
| ||
|---|---|---|
| Struktura | Aktivita | |
| X | IC50 (nM) | Inhibiční aktivita |
| >44 | Žádný |
| >44 | Žádný |
| 11 | Velmi slabá |
| 1.7 | Slabý |
| 0.50 | Mírný |
| 3.7 | Slabý |
| 0.11 | Mírný |
| 0.20 | Mírný |
| ||
|---|---|---|
| Struktura | Aktivita | |
| X | IC50 (nM) | Inhibiční aktivita |
| >44 | Žádný |
| 0.071 | Mírný |
| 2.5 | Slabý |
| 0.38 | Mírný |
| 0.20 | Mírný |
| 0.17 | Mírný |
| 0.040 | Silný |
| ||
|---|---|---|
| Struktura | Aktivita | |
| X | IC50 (nM) | Inhibiční aktivita |
| CH2 | 0.094 | Silný |
| CO | 0.30 | Mírný |
| C (CH3)2 | 1.2 | Slabý |
Odpor
Potenciální rezistence vůči HCV proti lékům DAA vzbuzuje obavy.[6] Mezi HCV kvazidruhy existují již existující varianty s potenciálem udělit rezistenci na inhibitory NS5A, aniž by byly dříve vystaveny těmto lékům. Obecně platí, že replikace těchto variant probíhá pouze v nepatrných množstvích, což je činí současnými technikami nedetekovatelnými. Na druhou stranu je možné selektivně pěstovat imunitní varianty v přítomnosti inhibitorů NS5A.[2] Odolnost proti HCV se vyznačuje určitým únikovým vzorem. Tento vzorec je často spojován s aminokyselinovými substitucemi, které viru propůjčují silnou rezistenci na léčivo, aniž by došlo ke zhoršení virové kondice.[2][56] Bylo zjištěno, že inhibitory NS5A mají relativně nízkou prahovou hodnotu pro rezistenci a bylo prokázáno, že varianty, které jsou spojeny s rezistencí na NS5A, vydrží u pacientů po ukončení léčby až šest měsíců.[57] Kombinované terapie proto produkují vyšší účinnost a kratší léčebné období.[7]
Budoucí výzkum a nové generace inhibitorů NS5A
Vývojáři DAA budou v následujících letech čelit předvídatelným výzvám. Terapeutické mezery pro jednotlivce trpící komplikujícími potížemi, jako je chronické onemocnění ledvin a cirhóza bude muset být přemostěna. Kratší terapie s mírnějšími vedlejšími účinky by přinesly větší adherenci a rýsuje se stále přítomné spektrum rezistence na léky. Vysoce adaptivní HCV se vyvinul do řady různých genomů, které je třeba všechny adekvátně léčit, nejlépe pangenotypickými režimy.[58]
Některé z těchto výzev již mají v dohledu možná řešení. Inhibitor proteázy ABT-493 a inhibitor NS5A nové generace ABT-530 jsou považovány za aktivní proti všem genotypům HCV, včetně těžko léčitelného genotypu 3.[42][58] In vitro vykazovala ABT-530 účinnost proti variantám spojeným s rezistencí, které jsou imunní vůči prvním generacím inhibitorů NS5A, včetně ledipasviru, daklatasviru a ombitasvir.[42] Protože tohle kombinace léků má další kvalitu vylučování z jater, slibuje, že pacienti trpící chronickým onemocněním ledvin a HCV by mohli v blízké budoucnosti dostat bezpečnou léčbu bez použití sofosbuviru.[58]
Připravují se nejméně tři kombinace léků pro léčbu HCV v letech 2016–2017: Sofosbuvir v kombinaci s velpatasvir, ABT-493 v kombinaci s ABT-530 a grazoprevir v kombinaci s elbasvir, z nichž velpatasvir, ABT-530 a elbasvir jsou inhibitory NS5A.[7]
Viz také
Reference
- ^ Gogela, Neliswa A .; Lin, Ming V .; Wisocky, Jessica L .; Chung, Raymond T. (12. března 2015). „Posílení našeho chápání současných terapií pro virus hepatitidy C (HCV)“. Aktuální zprávy o HIV / AIDS. 12 (1): 68–78. doi:10.1007 / s11904-014-0243-7. PMC 4373591. PMID 25761432.
- ^ A b C d E F G h i Pawlotsky, Jean-Michel (srpen 2013). „Inhibitory NS5A při léčbě hepatitidy C“. Journal of Hepatology. 59 (2): 375–382. doi:10.1016 / j.jhep.2013.03.030. PMID 23567084.
- ^ Do, Albert; Mittal, Yash; Liapakis, AnnMarie; Cohen, Elizabeth; Chau, Hong; Bertuccio, Claudia; Sapir, Dana; Wright, Jessica; Eggers, Carol; Drozd, Kristine; Ciarleglio, Maria; Deng, Yanhong; Lim, Joseph K .; Jhaveri, Ravi (27. srpna 2015). „Autorizace léčivých přípravků pro sofosbuvir / ledipasvir (Harvoni) pro chronickou infekci HCV v kohortě v reálném světě: nová bariéra v kaskádě péče o HCV“. PLOS ONE. 10 (8): e0135645. doi:10.1371 / journal.pone.0135645. PMC 4552165. PMID 26312999.
- ^ A b C d E F G h Tong, Ling; Yu, Wensheng; Coburn, Craig A .; Meinke, Peter T .; Nair, Anilkumar G .; Dwyer, Michael P .; Chen, Lei; Selyutin, Oleg; Rosenblum, Stuart B .; Jiang, Yueheng; Fells, James; Hu, Bin; Zhong, Bin; Soll, Richard M .; Liu, Rong; Agrawal, Sony; Xia, Ellen; Zhai, Ying; Kong, Rong; Ingravallo, Paul; Nomeir, Amin; Asante-Appiah, Ernest; Kozlowski, Joseph A. (červenec 2016). „Alternativní vývoj jádra kolem tetracyklické indolové třídy inhibitorů HCV NS5A“. Dopisy o bioorganické a léčivé chemii. 26 (20): 5132–5137. doi:10.1016 / j.bmcl.2016.07.057. PMID 27634194.
- ^ A b C Lemm, J. A .; Leet, J. E.; O'Boyle, D. R .; Romine, J. L .; Huang, X. S .; Schroeder, D. R .; Alberts, J .; Cantone, J. L .; Sun, J.-H .; Nower, P. T .; Martin, S. W .; Serrano-Wu, M. H .; Meanwell, N. A .; Snyder, L. B .; Gao, M. (16. května 2011). „Objev silných inhibitorů viru hepatitidy C NS5A s dimerními strukturami“. Antimikrobiální látky a chemoterapie. 55 (8): 3795–3802. doi:10.1128 / AAC.00146-11. PMC 3147613. PMID 21576451.
- ^ A b Fridell, R. A .; Qiu, D .; Wang, C .; Valera, L .; Gao, M. (28. června 2010). „Analýza rezistence inhibitoru NS5A viru hepatitidy C BMS-790052 v systému in vitro replikonu“. Antimikrobiální látky a chemoterapie. 54 (9): 3641–3650. doi:10.1128 / AAC.00556-10. PMC 2935007. PMID 20585111.
- ^ A b C Asselah, Tarik; Boyer, Nathalie; Saadoun, David; Martinot-Peignoux, Michele; Marcellin, Patrick (leden 2016). „Přímo působící antivirotika k léčbě infekce virem hepatitidy C: optimalizace současné léčby bez IFN a budoucí perspektivy“. Liver International. 36: 47–57. doi:10.1111 / liv.13027. PMID 26725897.
- ^ Halliday, John; Klenerman, Paul; Barnes, Eleanor (9. ledna 2014). „Očkování proti viru hepatitidy C: blížící se úhybnému cíli“. Odborná recenze vakcín. 10 (5): 659–672. doi:10,1586 / erv.11.55. PMC 3112461. PMID 21604986.
- ^ Grakoui, A; Wychowski, C; Lin, C; Feinstone, SM; Rice, C M (1. března 1993). „Exprese a identifikace produktů štěpení polyproteinů viru hepatitidy C“. Journal of Virology. 67 (3): 1385–1395. doi:10.1128 / JVI.67.3.1385-1395.1993. ISSN 0022-538X. PMC 237508. PMID 7679746.
- ^ Chan, Juliana (květen 2014). „Hepatitida C“. Nemoc za měsíc. 60 (5): 201–212. doi:10.1016 / j.disamonth.2014.04.002. PMID 24863270.
- ^ Seeff, Leonard B. (listopad 2002). "Přirozená historie chronické hepatitidy C". Hepatologie. 36 (5): s35 – s46. doi:10.1053 / jhep.2002.36806. PMID 12407575.
- ^ Liang, T. Jake; Rehermann, Barbara; Seeff, Leonard B .; Hoofnagle, Jay H. (15. února 2000). „Patogeneze, přírodní historie, léčba a prevence hepatitidy C“. Annals of Internal Medicine. 132 (4): 296–305. doi:10.7326/0003-4819-132-4-200002150-00008. PMID 10681285.
- ^ Pybus, O. G .; Barnes, E .; Taggart, R .; Lemey, P .; Markov, P. V .; Rasachak, B .; Syhavong, B .; Phetsouvanah, R .; Sheridan, I .; Humphreys, I. S .; Lu, L .; Newton, P. N .; Klenerman, P. (29. října 2008). „Genetická historie viru hepatitidy C ve východní Asii“. Journal of Virology. 83 (2): 1071–1082. doi:10.1128 / JVI.01501-08. PMC 2612398. PMID 18971279.
- ^ Tellinghuisen, T. L .; Foss, K. L .; Treadaway, J. C .; Rice, C. M. (21. listopadu 2007). "Identifikace reziduí požadovaných pro replikaci RNA v doménách II a III proteinu NS5A viru hepatitidy C". Journal of Virology. 82 (3): 1073–1083. doi:10.1128 / JVI.00328-07. PMC 2224455. PMID 18032500.
- ^ A b C d E F Reghellin, V .; Donnici, L .; Fenu, S .; Berno, V .; Calabrese, V .; Pagani, M .; Abrignani, S .; Peri, F .; De Francesco, R .; Neddermann, P. (15. září 2014). „Inhibitory NS5A narušují tvorbu komplexu NS5A-fosfatidylinositol 4-kinázy III a způsobují pokles hladin fosfatidylinositol 4-fosfátu a cholesterolu v membránách souvisejících s virem hepatitidy C“. Antimikrobiální látky a chemoterapie. 58 (12): 7128–7140. doi:10.1128 / AAC.03293-14. PMC 4249536. PMID 25224012.
- ^ A b C Yamasaki, Lilian HT; Arcuri, Helen A; Jardim, Ana Carolina G; Bittar, Cintia; de Carvalho-Mello, Isabel Maria VG; Rahal, Paula (2012). „Nové poznatky týkající se struktury / funkce HCV-NS5A a indikace genotypových rozdílů“. Virology Journal. 9 (1): 14. doi:10.1186 / 1743-422X-9-14. PMC 3271958. PMID 22239820.
- ^ A b C Masaki, T .; Matsunaga, S .; Takahashi, H .; Nakashima, K .; Kimura, Y .; Ito, M .; Matsuda, M .; Murayama, A .; Kato, T .; Hirano, H .; Endo, Y .; Lemon, S. M .; Wakita, T .; Sawasaki, T .; Suzuki, T. (23. dubna 2014). „Zapojení hyperfosforylace viru hepatitidy C NS5A zprostředkované kasein kinázou I - při produkci infekčního viru“. Journal of Virology. 88 (13): 7541–7555. doi:10.1128 / JVI.03170-13. PMC 4054430. PMID 24760886.
- ^ A b Ross-Thriepland, D .; Harris, M. (20. listopadu 2013). „Pohledy na složitost a funkčnost fosforylace viru hepatitidy C NS5A“. Journal of Virology. 88 (3): 1421–1432. doi:10.1128 / JVI.03017-13. PMC 3911623. PMID 24257600.
- ^ Rice, Charles M .; Marcotrigiano, Joseph; Tellinghuisen, Timothy L. (květen 2005). „Struktura domény vázající zinek základní složky replikázy viru hepatitidy C“. Příroda. 435 (7040): 374–379. doi:10.1038 / nature03580. ISSN 1476-4687. PMC 1440517. PMID 15902263.
- ^ Cronin, Ciarán N .; Wells, Peter A .; Hickey, Michael J .; Brodsky, Oleg; Láska, Robert A. (2009-05-01). "Krystalová struktura nové dimerní formy proteinu NS5A domény I z viru hepatitidy C". Journal of Virology. 83 (9): 4395–4403. doi:10.1128 / JVI.02352-08. ISSN 1098-5514. PMC 2668466. PMID 19244328.
- ^ Lambert, Sebastian M .; Langley, David R .; Garnett, James A .; Angell, Richard; Hedgethorne, Katy; Meanwell, Nicholas A .; Matthews, Steve J. (01.06.2014). „Krystalová struktura domény NS5A 1 z genotypu 1a odhaluje nové stopy mechanismu účinku dimerních inhibitorů HCV“. Věda o bílkovinách. 23 (6): 723–734. doi:10.1002 / pro.2456. ISSN 1469-896X. PMC 4093949. PMID 24639329.
- ^ A b Foster, T. L .; Belyaeva, T .; Stonehouse, N. J.; Pearson, A. R .; Harris, M. (30. června 2010). „Všechny tři domény viru hepatitidy C, nestrukturální protein NS5A, přispívají k vazbě RNA“. Journal of Virology. 84 (18): 9267–9277. doi:10.1128 / JVI.00616-10. PMC 2937630. PMID 20592076.
- ^ Fridell, R. A .; Qiu, D .; Valera, L .; Wang, C .; Rose, R.E .; Gao, M. (18. května 2011). "Odlišné funkce NS5A u replikace RNA viru hepatitidy C odhalené studiemi s inhibitorem NS5A BMS-790052". Journal of Virology. 85 (14): 7312–7320. doi:10.1128 / JVI.00253-11. PMC 3126594. PMID 21593143.
- ^ A b Ascher, David B .; Wielens, Jerome; Nero, Tracy L .; Doughty, Larissa; Morton, Craig J .; Parker, Michael W. (23. dubna 2014). „Silné inhibitory hepatitidy C se vážou přímo na NS5A a snižují jeho afinitu k RNA“. Vědecké zprávy. 4: 4765. doi:10.1038 / srep04765. PMC 3996483. PMID 24755925.
- ^ Beldar, Serap; Manimekalai, Malathy Sony Subramanian; Cho, Nam-Joon; Baek, Kwanghee; Grüber, Gerhard; Yoon, Ho Sup (2018). „Vlastní asociace a konformační variace NS5A domény 1 viru hepatitidy C“. Journal of General Virology. 99 (2): 194–208. doi:10.1099 / jgv.0.001000. PMID 29300159.
- ^ Badillo, Aurelie; Receveur-Brechot, Véronique; Sarrazin, Stéphane; Cantrelle, François-Xavier; Delolme, Frédéric; Fogeron, Marie-Laure; Molle, Jennifer; Montserret, Roland; Bockmann, Anja (07.06.2017). "Celkový strukturální model proteinu NS5A z viru hepatitidy C a modulace mutacemi udávajícími odolnost replikace viru na cyklosporin A". Biochemie. 56 (24): 3029–3048. doi:10.1021 / acs.biochem.7b00212. PMID 28535337.
- ^ A b Xiong, Wei; Yang, Jie; Wang, Mingzhen; Wang, Hailong; Rao, Zhipeng; Zhong, Cheng; Xin, Xiu; Mo, Lin; Yu, Shujuan; Shen, Chao; Zheng, Congyi; Diamond, M. S. (15. července 2015). „Vinexin β interaguje s virem hepatitidy C NS5A a moduluje jeho hyperfosforylaci za účelem regulace šíření virů“. Journal of Virology. 89 (14): 7385–7400. doi:10.1128 / JVI.00567-15. PMC 4473562. PMID 25972535.
- ^ A b Reiss, Simon; Rebhan, Ilka; Backes, Perdita; Romero-Brey, Ines; Erfle, Holger; Matula, Petr; Kaderali, Lars; Poenisch, Marion; Blankenburg, Hagen; Hiet, Marie-Sophie; Longerich, Thomas; Diehl, Sarah; Ramirez, Fidel; Balla, Tamas; Rohr, Karl; Kaul, Artur; Bühler, Sandra; Pepperkok, Rainer; Lengauer, Thomas; Albrecht, Mario; Eils, Roland; Schirmacher, Peter; Lohmann, Volker; Bartenschlager, Ralf (leden 2011). „Nábor a aktivace lipid kinázy virem hepatitidy C NS5A je nezbytný pro integritu oddělení membránové replikace“. Mobilní hostitel a mikrob. 9 (1): 32–45. doi:10.1016 / j.chom.2010.12.002. PMC 3433060. PMID 21238945.
- ^ Lim, Y.-S .; Hwang, S. B. (5. února 2011). „Protein NS5A viru hepatitidy C interaguje s fosfatidylinositol 4-kinázou typu III a reguluje šíření virů“. Journal of Biological Chemistry. 286 (13): 11290–11298. doi:10.1074 / jbc.M110.194472. PMC 3064185. PMID 21297162.
- ^ A b Ahmed, Marawan; Pal, Abhishek; Houghton, Michael; Barakat, Khaled (3. srpna 2016). „Komplexní výpočetní analýza pro vazebné režimy inhibitorů NS5A viru hepatitidy C: otázka symetrie“. Infekční choroby ACS. 2 (11): 872–881. doi:10.1021 / acsinfecdis.6b00113. PMID 27933783.
- ^ A b C d Issur, Moheshwarnath; Götte, Matthias (6. listopadu 2014). „Vzory rezistence spojené s inhibitory HCV NS5A poskytují omezený přehled o vazbě na léky“. Viry. 6 (11): 4227–4241. doi:10,3390 / v6114227. PMC 4246218. PMID 25384189.
- ^ Lambert, Sebastian M .; Langley, David R .; Garnett, James A .; Angell, Richard; Hedgethorne, Katy; Meanwell, Nicholas A .; Matthews, Steve J. (červen 2014). „Krystalová struktura domény NS5A 1 z genotypu 1a odhaluje nové stopy mechanismu účinku dimerních inhibitorů HCV“. Věda o bílkovinách. 23 (6): 723–734. doi:10.1002 / pro.2456. PMC 4093949. PMID 24639329.
- ^ A b Qiu, D .; Lemm, J. A .; O'Boyle, D. R .; Sun, J.-H .; Nower, P. T .; Nguyen, V .; Hamann, L. G .; Snyder, L. B .; Deon, D. H .; Ruediger, E .; Meanwell, N. A .; Belema, M .; Gao, M .; Fridell, R. A. (27. července 2011). „Účinky inhibitorů NS5A na fosforylaci NS5A, zpracování a lokalizaci polyproteinů“. Journal of General Virology. 92 (11): 2502–2511. doi:10.1099 / vir.0.034801-0. PMID 21795470.
- ^ A b Belema, Makonen; Lopez, Omar D .; Bender, John A .; Romine, Jeffrey L .; St. Laurent, Denis R .; Langley, David R .; Lemm, Julie A .; O’Boyle, Donald R .; Sun, Jin-Hua; Wang, Chunfu; Fridell, Robert A .; Meanwell, Nicholas A. (13. března 2014). "Objev a vývoj komplexních inhibitorů replikace viru hepatitidy C NS5A". Journal of Medicinal Chemistry. 57 (5): 1643–1672. doi:10,1021 / jm401793m. PMID 24621191.
- ^ A b Guedj, J .; Dahari, H .; Rong, L .; Sansone, N. D .; Nettles, R.E .; Cotler, S. J .; Layden, T. J .; Uprichard, S.L .; Perelson, A. S. (19. února 2013). „Modelování ukazuje, že daklatasvir s inhibitorem NS5A má dva způsoby působení a poskytuje kratší odhad poločasu viru hepatitidy C“. Sborník Národní akademie věd. 110 (10): 3991–3996. doi:10.1073 / pnas.1203110110. PMC 3593898. PMID 23431163.
- ^ McGivern, David R .; Masaki, Takahiro; Williford, Sara; Ingravallo, Paul; Feng, Zongdi; Lahser, Frederick; Asante-Appiah, Ernest; Neddermann, Petra; De Francesco, Raffaele; Howe, Anita Y .; Lemon, Stanley M. (srpen 2014). „Kinetické analýzy odhalují silnou a časnou blokádu sestavy viru hepatitidy C inhibitory NS5A“. Gastroenterologie. 147 (2): 453–462.e7. doi:10.1053 / j.gastro.2014.04.021. PMC 4107048. PMID 24768676.
- ^ Neufeldt, Christopher J .; Joyce, Michael A .; Van Buuren, Nicholas; Levin, Aviad; Kirkegaard, Karla; Gale Jr., Michael; Tyrrell, D. Lorne J .; Wozniak, Richard W .; Kuhn, Richard J. (10. února 2016). „Membranózní web vyvolaný virem hepatitidy C a související zařízení pro jaderný transport omezují přístup receptorů pro rozpoznávání vzorů na stránky replikace virů“. PLOS patogeny. 12 (2): e1005428. doi:10.1371 / journal.ppat.1005428. PMC 4749181. PMID 26863439.
- ^ Berger, Carola; Romero-Brey, Inés; Radujkovic, Danijela; Terreux, Raphael; Zayas, Margarita; Paul, David; Harak, Christian; Hoppe, Simone; Gao, Min; Penin, Francois; Lohmann, Volker; Bartenschlager, Ralf (listopad 2014). „Inhibitory NS5A podobné daklatasviru blokují časnou biogenezi virů hepatitidy C - továrny na membránovou replikaci, nezávislé na RNA replikaci“. Gastroenterologie. 147 (5): 1094–1105.e25. doi:10.1053 / j.gastro.2014.07.019. PMID 25046163.
- ^ A b Zhang, Xingquan (leden 2016). „Přímí agenti anti-HCV“. Acta Pharmaceutica Sinica B. 6 (1): 26–31. doi:10.1016 / j.apsb.2015.09.008. PMC 4724659. PMID 26904396.
- ^ Fung, A .; Jin, Z .; Dyatkina, N .; Wang, G .; Beigelman, L .; Deval, J. (14. dubna 2014). „Účinnost začlenění a ukončení řetězce určuje inhibiční účinnost 2'-modifikovaných nukleotidových analogů proti polymerázě viru hepatitidy C“. Antimikrobiální látky a chemoterapie. 58 (7): 3636–3645. doi:10.1128 / AAC.02666-14. PMC 4068585. PMID 24733478.
- ^ Bruder Costa, Juliana; Dufeu-Duchesne, Tania; Leroy, Vincent; Bertucci, Inga; Bouvier-Alias, Magali; Pouget, Noelle; Brevot-Lutton, Ophelie; Bourliere, Marc; Zoulim, Fabien; Plumas, Joel; Aspord, Caroline; Chemin, Isabelle A (27. června 2016). „Pegylovaný interferon α-2a spouští funkci NK-buněk a specifické reakce T-buněk u pacientů s chronickou infekcí HBV bez sérokonverze HBsAg“. PLOS ONE. 11 (6): e0158297. doi:10.1371 / journal.pone.0158297. PMC 4922676. PMID 27348813.
- ^ A b C Poordad, Fred; Landis, Charles S .; Asatryan, Armen; Jackson, Daniel F .; Ng, Teresa I .; Fu, Bo; Lin, Chih-Wei; Yao, Betty; Kort, Jens (srpen 2016). „Vysoká antivirová aktivita inhibitoru NS5A ABT-530 s paritaprevirem / ritonavirem a ribavirinem proti infekci virem hepatitidy C genotypu 3“. Liver International. 36 (8): 1125–1132. doi:10.1111 / liv.13067. PMC 5067610. PMID 26778412.
- ^ Gaudieri, Silvana; Rauch, Andri; Pfafferott, Katja; Barnes, Eleanor; Cheng, Wendy; McCaughan, Geoff; Shackel, Nick; Jeffrey, Gary P .; Mollison, Lindsay; Baker, Ross; Furrer, Hansjakob; Günthard, Huldrych F .; Freitas, Elizabeth; Humphreys, Isla; Klenerman, Paul; Mallal, Simon; James, Ian; Roberts, Stuart; Nolan, David; Lucas, Michaela (duben 2009). „Rezistence na léky proti viru hepatitidy C a imunitní adaptace: význam pro novou antivirovou terapii“. Hepatologie. 49 (4): 1069–1082. doi:10,1002 / hep.22773. PMID 19263475.
- ^ Archer, Melissa; Steinvoort, Carin; Oderda, Gary. „AKTUALIZACE: Nová kombinace látek s hepatitidou C“ (PDF). Utahské ministerstvo zdravotnictví. Archivovány od originál (PDF) dne 27. prosince 2016. Citováno 8. září 2016.
- ^ Blight, K. J. (8. prosince 2000). "Efektivní zahájení replikace HCV RNA v buněčné kultuře". Věda. 290 (5498): 1972–1974. doi:10.1126 / science.290.5498.1972. PMID 11110665.
- ^ A b Conte, Immacolata; Giuliano, Claudio; Ercolani, Caterina; Narjes, Frank; Koch, Uwe; Rowley, Michael; Altamura, Sergio; Francesco, Raffaele De; Neddermann, Petra; Migliaccio, Giovanni; Stansfield, Ian (březen 2009). „Syntéza a SAR piperazinyl-N-fenylbenzamidů jako inhibitorů replikace RNA viru hepatitidy C v buněčné kultuře“. Dopisy o bioorganické a léčivé chemii. 19 (6): 1779–1783. doi:10.1016 / j.bmcl.2009.01.066. PMID 19216075.
- ^ Lohmann, V. (2. července 1999). „Replikace subgenomových RNA viru hepatitidy C v buněčné linii hepatomu“. Věda. 285 (5424): 110–113. doi:10.1126 / science.285.5424.110. PMID 10390360.
- ^ Lohmann, V .; Hoffmann, S .; Herian, U .; Penin, F .; Bartenschlager, R. (1. března 2003). „Virové a buněčné determinanty replikace RNA viru hepatitidy C v buněčné kultuře“. Journal of Virology. 77 (5): 3007–3019. doi:10.1128 / JVI.77.5.3007-3019.2003. PMC 149776. PMID 12584326.
- ^ „FDA schvaluje novou léčbu chronických infekcí hepatitidou C genotypu 3“. FDA. 27. července 2015. Citováno 29. září 2016.
- ^ A b C d E F G h Link, John O .; Taylor, James G .; Xu, Lianhong; Mitchell, Michael; Guo, Hongyan; Liu, Hongtao; Kato, Darryl; Kirschberg, Thorsten; Sun, Jianyu; Squires, Neil; Parrish, Jay; Keller, Terry; Yang, Zheng-Yu; Yang, Chris; Matles, Mike; Wang, Yujin; Wang, Kelly; Cheng, Guofeng; Tian, Yang; Mogalian, Erik; Mondou, Elsa; Cornpropst, Melanie; Perry, Jason; Desai, Manoj C. (13. března 2014). „Objev ledipasviru (GS-5885): silný perorální inhibitor NS5A pro léčbu infekce virem hepatitidy C jednou denně“. Journal of Medicinal Chemistry. 57 (5): 2033–2046. doi:10,1021 / jm401499g. PMID 24320933.
- ^ Keating, Gillian M. (3. dubna 2015). „Ledipasvir / Sofosbuvir: Přehled jeho použití při chronické hepatitidě C“. Drogy. 75 (6): 675–685. doi:10.1007 / s40265-015-0381-2. PMID 25837989. S2CID 31943736.
- ^ Nakamoto, Shingo (2014). „Inhibitory NS5A viru hepatitidy C a mutace rezistence na léky“. World Journal of Gastroenterology. 20 (11): 2902–12. doi:10,3748 / wjg.v20.i11.2902. PMC 3961994. PMID 24659881.
- ^ Boucle, Sebastien; Tao, Sijia; Amblard, Franck; Stanton, Richard A .; Nettles, James H .; Li, Chengwei; McBrayer, Tamara R .; Whitaker, Tony; Coats, Steven J .; Schinazi, Raymond F. (září 2015). „Návrh, syntéza a hodnocení nových molekul anti-HCV, které dodávají intracelulárně tři vysoce účinné inhibitory NS5A“. Dopisy o bioorganické a léčivé chemii. 25 (17): 3711–3715. doi:10.1016 / j.bmcl.2015.06.031. PMC 4538959. PMID 26099532.
- ^ A b Romine, Jeffrey L .; St. Laurent, Denis R .; Leet, John E .; Martin, Scott W .; Serrano-Wu, Michael H .; Yang, Fukang; Gao, Min; O’Boyle, Donald R; Lemm, Julie A .; Sun, Jin-Hua; Nower, Peter T .; Huang, Xiaohua (Stella); Deshpande, Milind S .; Meanwell, Nicholas A .; Snyder, Lawrence B. (10. března 2011). „Inhibitory HCV NS5A: Od iminothiazolidinonů k symetrickým stilbenům“. Dopisy ACS pro léčivou chemii. 2 (3): 224–229. doi:10,1021 / ml 1002647. PMC 4017990. PMID 24900306.
- ^ Shi, Junxing; Zhou, Longhu; Amblard, Franck; Bobeck, Drew R .; Zhang, Hongwang; Liu, Peng; Bondada, Lavanya; McBrayer, Tamara R .; Tharnish, Phillip M .; Whitaker, Tony; Coats, Steven J .; Schinazi, Raymond F. (květen 2012). "Syntéza a biologické hodnocení nových silných a selektivních inhibitorů HCV NS5A". Dopisy o bioorganické a léčivé chemii. 22 (10): 3488–3491. doi:10.1016 / j.bmcl.2012.03.089. PMID 22507961.
- ^ Strahotin, Cristina Simona; Babich, Michael (2012). „Variabilita hepatitidy C, vzorce rezistence a dopad na léčbu“. Pokroky ve virologii. 2012: 267483. doi:10.1155/2012/267483. PMC 3407602. PMID 22851970.
- ^ Owens, Christopher M .; Brasher, Bradley B .; Polemeropoulos, Alex; Rhodin, Michael H. J .; McAllister, Nicole; Wong, Kelly A .; Jones, Christopher T .; Jiang, Lijuan; Lin, Kai; Nebo Yat Sun (říjen 2016). „Profil preklinické a klinické rezistence EDP-239, nového inhibitoru viru hepatitidy C NS5A“. Antimikrobiální látky a chemoterapie. 60 (10): 6216–6226. doi:10.1128 / AAC.00815-16. PMC 5038316. PMID 27503644.
- ^ A b C Feld, Jordan J .; Foster, Graham R. (říjen 2016). „Druhá generace přímo působících antivirotik - očekáváme zásadní vylepšení?“. Journal of Hepatology. 65 (1): S130 – S142. doi:10.1016 / j.jhep.2016.07.007. PMID 27641983.