Hydroxid kurnatý - Curium hydroxide
 | |
| Jména | |
|---|---|
| Název IUPAC Hydroxid kurnatý | |
| Systematický název IUPAC Oxidanid kuria (3+) | |
| Identifikátory | |
3D model (JSmol ) | |
| |
| |
| Vlastnosti | |
| CmH3Ó3 | |
| Molární hmotnost | 298 g · mol−1 |
| Vzhled | bezbarvá nebo světle žlutá pevná látka |
| nerozpustný | |
| Struktura | |
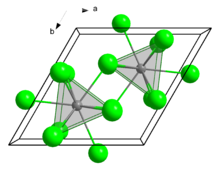
| šestihranný, UCl3 struktura[1] | |
| P63/ m, č. 176[2] | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |

Hydroxid kuriový ve spodní části kužele mikrocentrifugy, podzim 1947
Hydroxid kurnatý [Cm (OH)3] je radioaktivní sloučenina poprvé objevená v měřitelných množstvích v roce 1947. Skládá se z jediné kurium atom a tři hydroxid skupiny. Byla to první sloučenina kuria, která byla kdy izolována.[3][4]
Hydroxid kurnatý je bezvodý, bezbarvý[2] nebo světle žlutá[5] amorfní želatinová pevná látka, která je nerozpustná ve vodě.[1] Díky vlastnímu ozáření byla krystalová struktura 244Cm (OH)3 se rozloží do jednoho dne, zatímco pro hydroxid amerikatý 241Jsem (OH)3 stejný proces trvá 4-6 měsíců.[2]
Viz také
Reference
- ^ A b Macintyre, Jane E. (1992). Slovník anorganických sloučenin. CRC Press. p. 3046. ISBN 978-0-412-30120-9.
- ^ A b C d E Krivovichev, Sergei; Burns, Peter; Tananaev, Ivan (2006). Strukturní chemie anorganických aktinidových sloučenin. Elsevier. p. 68. ISBN 978-0-08-046791-7.
- ^ Seaborg, Glenn T. (1963). Uměle vyrobené transuranové prvky. Prentice-Hall.
- ^ "WebElements Periodic Table: Curium". webelements.com. Citováno 20. ledna 2019.
- ^ Koch, Günter (1972). Transurane Teil C: Die Verbindungen. Gmelins Handbuch (v němčině). Springer-Verlag. p. 35. ISBN 978-3-662-11547-3.
| Tento anorganické sloučenina –Vztahující se článek je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
