Acidobazická extrakce - Acid-base extraction
Acidobazická extrakce je postup používající sekvenční kapalina – kapalné extrakce očistit kyseliny a základny ze směsí na základě jejich chemických vlastností.[1]
Acidobazická extrakce se běžně provádí během vypracovat po chemické syntézy a pro izolaci sloučenin a přírodní produkty jako alkaloidy ze surového výtažky. Produkt je do značné míry bez neutrálních a kyselých nebo zásaditých nečistot. Pomocí této jednoduché metody není možné oddělit chemicky podobné kyseliny nebo zásady.
Teorie
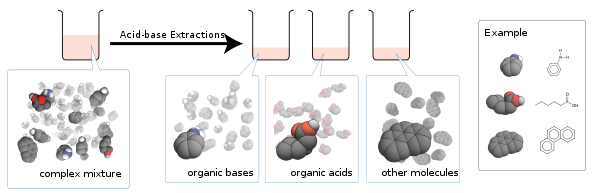
Základní teorie za touto technikou je ta soli, což jsou iontový, bývají rozpustné ve vodě, zatímco neutrální molekuly nebývají.
Přidání kyseliny ke směsi organické báze a kyseliny povede k tomu, že kyselina zůstane nenabitá, zatímco báze bude protonována za vzniku soli. Pokud organická kyselina, jako je a karboxylová kyselina, je dostatečně slabý, jeho samoionizace může být potlačena přidanou kyselinou.
Naopak přidání báze ke směsi organické kyseliny a báze povede k tomu, že báze zůstane nenabitá, zatímco se kyselina deprotonuje, čímž se získá odpovídající sůl. Samoionizace silné báze je opět potlačena přidanou bází.
Postup acidobazické extrakce lze také použít k oddělení velmi slabých kyselin od silnějších kyselin a velmi slabých bází od silnějších zásad, pokud je rozdíl jejich pKA (nebo pKb) konstanty je dostatečně velká. Například:
- Velmi slabé kyseliny s fenolickými OH skupinami fenol, 2-naftol nebo 4-hydroxyindol (pKA asi 10) od silnějších kyselin jako kyselina benzoová nebo kyselina sorbová (pKA kolem 4–5)
- Velmi slabé základy jako kofein nebo 4-nitroanilin (pKb kolem 13–14) ze silnějších základen jako meskalin nebo dimethyltryptamin (pKb kolem 3–4)
Obvykle je pH upraveno na hodnotu zhruba mezi pKA (nebo pKb) konstanty sloučenin, které se mají oddělit. Slabé kyseliny jako kyselina citronová, kyselina fosforečná nebo zředěný kyselina sírová se používají pro mírně kyselé hodnoty pH a kyselina chlorovodíková nebo se pro silně kyselé hodnoty pH používá více koncentrované kyseliny sírové. Podobně jako slabé báze amoniak nebo hydrogenuhličitan sodný (NaHCO3) se používají pro mírně zásadité hodnoty pH, zatímco silnější zásady jako Uhličitan draselný (K.2CO3) nebo hydroxid sodný (NaOH) se používají pro silně alkalické podmínky.
Technika
Obvykle se směs rozpustí ve vhodném rozpouštědle, jako je například dichlormethan nebo diethylether (ether), a nalila do a dělicí nálevka. Přidá se vodný roztok kyseliny nebo báze a pH vodné fáze se upraví tak, aby se požadovaná sloučenina dostala do požadované formy. Po protřepání a umožnění fázové separace se shromáždí fáze obsahující požadovanou sloučeninu. Postup se potom opakuje s touto fází v opačném rozmezí pH. Pořadí kroku není důležité a pro zvýšení separace lze postup opakovat. Často je však vhodné nechat sloučeninu rozpustit v organické fázi po posledním kroku, takže odpařením rozpouštědla se získá produkt.
Omezení
Postup funguje pouze pro kyseliny a zásady s velkým rozdílem v rozpustnosti mezi jejich nabitou a nenabitou formou. Postup nefunguje pro:
- Zwitterions s kyselým a zásaditým funkční skupiny ve stejné molekule, např. glycin které bývají rozpustné ve vodě při maximálním pH.
- Velmi lipofilní aminy, které se snadno nerozpouštějí ve vodné fázi v nabité formě, např. trifenylamin a trihexylamin.
- Velmi lipofilní kyseliny, které se snadno nerozpouštějí ve vodné fázi v nabité formě, např. mastné kyseliny.
- Nižší aminy jako amoniak, methylamin nebo triethanolamin které jsou mísitelné nebo významně rozpustné ve vodě při maximálním pH.
- Hydrofilní kyseliny jako octová kyselina, kyselina citronová a většina anorganické kyseliny jako kyselina sírová nebo kyselina fosforečná.
Alternativy
Alternativy k acidobazické extrakci včetně:
- filtrování směsi přes zátku silikonový gel nebo oxid hlinitý - nabité soli mají tendenci zůstat silně adsorbovány na silikagelu nebo oxidu hlinitém
- iontoměničová chromatografie může oddělit kyseliny, zásady nebo směsi silných a slabých kyselin a zásad podle své různé afinity k médiu kolony při různém pH.
Viz také
- Chromatografie, výkonnější, ale složitější postup pro oddělení sloučenin
- Extrakce
- Vícefázová kapalina
- Oddělovací nálevka
Reference
- ^ Laurence M. Harwood, Christopher J. Moody (13. června 1989). Experimentální organická chemie: Principy a praxe (Ilustrované vydání.). WileyBlackwell. str.118–22. ISBN 978-0-632-02017-1.


