Redukce nitrosloučenin - Reduction of nitro compounds
The redukce nitrosloučenin jsou chemické reakce širokého zájmu o organickou chemii. Konverze může být provedena mnoha činidly. The nitroskupina byl jedním z prvních funkční skupiny být snížena. Alkylové a arylnitrosloučeniny se chovají odlišně. Nejužitečnější je redukce arylnitrosloučenin.
Aromatické nitrosloučeniny
Redukce na aniliny
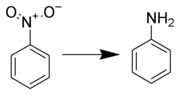
Redukce nitroaromatiky se provádí v průmyslovém měřítku.[1] Existuje mnoho metod, například:
- Katalytická hydrogenace za použití: Raneyova niklu[2] nebo palladium na uhlí,[3] oxid platičitý nebo Urushibara nikl[4].
- Žehlička v kyselém prostředí.[5] Reakční podmínky jsou obvykle jemné. Železo má vysokou toleranci funkčních skupin (viz Redukce Bechamp ).
- Hydrosiřičitan sodný[6]
- Sulfid sodný (nebo sirovodík a základna). Ilustrováno selektivní redukcí dinitrofenolu na nitroaminofenol.[7]
- Chlorid cínatý[8]
- Chlorid titaničitý
- Samarium[9]
- Kyselina jodovodíková[10]
Hydridy kovů se obvykle nepoužívají k redukci arylnitrosloučenin na aniliny, protože mají tendenci produkovat azosloučeniny. (Viz. níže)
Redukce na hydroxylaminy
Bylo popsáno několik způsobů výroby arylu hydroxylaminy z arylnitrosloučenin:
- Raney nikl a hydrazin při 0-10 ° C[11]
- Elektrolytická redukce[12]
- Zinek kov ve vodném chlorid amonný[13]
Redukce na hydrazinosloučeniny
Ošetření nitroarenů přebytkem zinek kov má za následek tvorbu N,N '-diarylhydrazin.[14]
Redukce na azosloučeniny
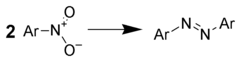
Zpracování aromatických nitrosloučenin hydridy kovů poskytuje dobré výtěžky azosloučeniny. Například lze použít:
- Lithiumaluminiumhydrid[15]
- Zinek kov s hydroxid sodný.[14] (Přebytek zinku redukuje azoskupinu na hydrazinovou sloučeninu.)
Alifatické nitrosloučeniny
Redukce na uhlovodíky
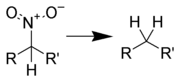
Hydrodenitrace (nahrazení nitroskupiny vodík ) je obtížné dosáhnout, ale lze jej provést katalytickou hydrogenací Platina na silikonový gel při vysokých teplotách.[16]Reakce může být také provedena radikální reakcí s tributylcín hydrid a radikální iniciátor, AIBN jako příklad.[17]
Redukce na aminy

Alifatické nitrosloučeniny lze redukovat na alifatické aminy několika činidly:
- Katalytická hydrogenace za použití oxid platičitý (PtO2)[18] nebo Raney nikl[19]
- Žehlička kov při refluxu octová kyselina[20]
- Samodiumjodid[21]
- Raney nikl, platina na uhlíku nebo zinek prach a kyselina mravenčí nebo mravenčan amonný[4]
α, β-Nenasycené nitrosloučeniny lze redukovat na nasycené aminy pomocí:
- Katalytická hydrogenace skončila palladium na uhlí
- Železný kov
- Lithiumaluminiumhydrid[22] (Poznámka: Typickými nečistotami jsou hydroxylaminy a oximy.)
- Borohydrid lithný nebo borohydrid sodný a trimethylsilylchlorid[23]
- Red-Al[24]
Redukce na hydroxylaminy
Alifatické nitrosloučeniny lze redukovat na alifatické hydroxylaminy použitím diboran.[25]
Reakce může být také provedena s zinek prach a chlorid amonný[Citace je zapotřebí ]:
- R-NO2 + 4 NH4Cl + 2 Zn → R-NH-OH + 2 ZnCl2 + 4 NH3 + H2Ó
Redukce na oximy

Nitrosloučeniny se obvykle redukují na oximy za použití solí kovů, jako jsou chlorid cínatý[26] nebo chlorid chromitý.[27] Kromě toho může katalytická hydrogenace pomocí kontrolovaného množství vodíku generovat oximy.[28]
Reference
- ^ Gerald Booth (2007). Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a17_411.
- ^ Allen, C. F. H .; VanAllan, J. (1955). „2-amino-str-cymen. Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 3, str. 63
- ^ Bavin, P. M. G. (1973). „2-aminofluoren“. Organické syntézy.; Kolektivní objem, 5, str. 30
- ^ A b Adams, J. P. (2002). "Nitro a příbuzné skupiny". Journal of the Chemical Society, Perkin Transactions 1. 0 (23): 2586–2597. doi:10.1039 / b009711j.
- ^ Fox, B. A .; Threlfall, T. L. (1964). "2,3-Diaminopyridin". Organické syntézy. 44: 34. doi:10.15227 / orgsyn.044.0034.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Redemann, C. T .; Redemann, C. E. (1955). „5-Amino-2,3-dihydro-1,4-ftalazindion". Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 3, str. 69
- ^ Hartman, W. W .; Silloway, H. L. (1945). „2-Amino-4-nitrofenol“. Organické syntézy. 25: 5. doi:10.15227 / orgsyn.025.0005.
- ^ Faul, Margaret M .; Thiel, Oliver R. (2005). „Chlorid cínatý“. Encyklopedie činidel pro organickou syntézu. Encyklopedie činidel pro organickou syntézu. doi:10.1002 / 047084289X.rt112.pub2. ISBN 9780470842898.
- ^ Basu, M. K. (2000). „Ultrazvukem podporovaná vysoce účinná redukce aromatických nitrosloučenin na aromatické aminy samariem / chloridem amonným“. Tetrahedron Lett. 41 (30): 5603–5606. doi:10.1016 / S0040-4039 (00) 00917-5.
- ^ Kumar, J. S. Dileep; Ho, ManKit M .; Toyokuni, Tatsushi (2001). "Jednoduchá a chemoselektivní redukce aromatických nitrosloučenin na aromatické aminy: redukce s kyselinou jodovodíkovou znovu navštívena". Čtyřstěn dopisy. 42 (33): 5601–5603. doi:10.1016 / s0040-4039 (01) 01083-8.
- ^ Ayyangar, N.R .; Brahme, K. C .; Kalkote, USA; Srinivasan, K.V. (1984). "Facile Transfer-Reduction of Nitroarenes to N Arylhydroxylamines with Hydrazine in the Presence of Raney Nickel". Syntéza. 1984 (11): 938. doi:10,1055 / s-1984-31027.
- ^ Harman, R. E. (1963). „Chloro-str-benzochinon ". Organické syntézy.; Kolektivní objem, 4, str. 148
- ^ Kamm, O. (1941). "β-fenylhydroxylamin". Organické syntézy.; Kolektivní objem, 1, str. 445
- ^ A b Bigelow, H. E.; Robinson, D. B. (1955). "Azobenzen". Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 3, str. 103
- ^ R. F. Nystrom a W. G. Brown (1948). „Redukce organických sloučenin hydridem lithno-hlinitým. III. Halogenidy, chinony, různé sloučeniny dusíku“. J. Am. Chem. Soc. 70 (11): 3738–3740. doi:10.1021 / ja01191a057. PMID 18102934.
- ^ M. J. Guttieri a W. F. Maier (1984). "Selektivní štěpení vazeb uhlík-dusík platinou". J. Org. Chem. 49 (16): 2875–2880. doi:10.1021 / jo00190a006.
- ^ T. V. (Babu) RajanBabu, Philip C. Bulman Page, Benjamin R. Buckley, „Tri-n-butylstannane“ Encyclopedia of Reagents for Organic Synthesis 2004, John Wiley & Sons. doi: 10.1002 / 047084289X.rt181.pub2
- ^ A. T. Nielsen (1962). „Izomerní dinitrocyklohexany. II. Stereochemie“. J. Org. Chem. 27 (6): 1998–2001. doi:10.1021 / jo01053a019.
- ^ Dauben, Jr., H. J .; Ringold, H. J .; Wade, R. H .; Pearson, D. L .; Anderson, Jr., A. G. (1963). „Cykloheptanon“. Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 4, str. 221
- ^ Senkus, M. (1948). „Ind. Eng. Chem“. 40: 506. Citovat deník vyžaduje
| deník =(Pomoc) - ^ A. S. Kende a J. S. Mendoza (1991). "Řízená redukce nitroalkanů na alkylhydroxylaminy nebo aminy samariumdiodidem". Čtyřstěn dopisy. 32 (14): 1699–1702. doi:10.1016 / S0040-4039 (00) 74307-3.
- ^ A. Burger, M. L. Stein a J. B. Clements (1957). „Některé pyridylnitroalkeny, nitroalkanoly a alkylaminy“. J. Org. Chem. 22 (2): 143–144. doi:10.1021 / jo01353a010.
- ^ Giannis, A .; Sandhoff, K. (1989). „LiBH4 (NaBH4) / Me3SiCl, neobvykle silný a univerzální redukční agent“. Angewandte Chemie International Edition v angličtině. 28 (2): 218–220. doi:10,1002 / anie.198902181.
- ^ Butterick, John R .; Unrau, A. M. (1974). „Redukce β-nitrostyrenu sodnou solí bis- (2-methoxyethoxy) -aluminiumdihydridu. Vhodná cesta k substituovaným fenylisopropylaminům.“. J. Chem. Soc., Chem. Commun. 0 (8): 307–308. doi:10.1039 / c39740000307.
- ^ H. Feuer, R. S. Bartlett, B. F. Vincent a R. S. Anderson (1965). "Redukce diboranu nitrosoli. Nová syntéza N-monosubstituovaných hydroxylaminů". J. Org. Chem. 30 (9): 2880–2882. doi:10.1021 / jo01020a002.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Braun, V. J .; Sobecki, W. (1911). „Über primäre Dinitro-, Nitronitrit- und Dialdoxim-Verbindungen der Fettreihe“. Ber. 44 (3): 2526–2534. doi:10.1002 / cber.19110440377.
- ^ J. R. Hanson a E. Premuzic (1967). "Aplikace chromitého chloridu - II: Redukce některých steroidních nitrosloučenin". Čtyřstěn. 23 (10): 4105–4110. doi:10.1016 / S0040-4020 (01) 97921-9.
- ^ C. Grundmann (1950). „Über die partielle Reduktion von Nitro-cyklohexan“. Angewandte Chemie. 62 (23–24): 558–560. doi:10,1002 / ange.19500622304.

