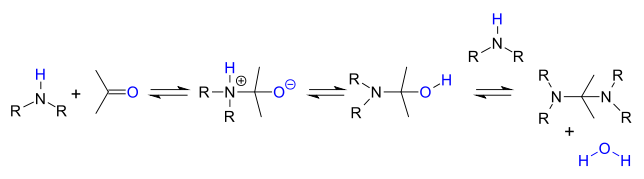Alkylimino-de-oxo-bisubstituce - Alkylimino-de-oxo-bisubstitution
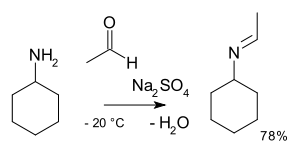
Alkylimino-de-oxo-bisubstituce v organická chemie je organická reakce z karbonyl sloučeniny s aminy na iminy.[2] Název reakce je založen na Nomenklatura IUPAC pro transformace. Reakce je kyselinou katalyzovaný a typ reakce je nukleofilní adice aminu na karbonylovou sloučeninu s následným přenosem a proton z dusíku na kyslík na stabilní hemiaminal nebo karbinolamin. S primárními aminy se voda ztrácí v eliminační reakce do já těžím. S aryl aminy obzvláště stabilní Schiffovy základny jsou vytvořeny.
Reakční mechanismus
Reakční kroky jsou reverzibilní reakce a reakce je dokončena odstraněním vody pomocí azeotropická destilace, molekulární síta nebo chlorid titaničitý. Primární aminy reagují prostřednictvím nestability hemiaminal meziprodukt, který pak odštěpuje vodu.
Sekundární aminy snadno neztrácejí vodu, protože nemají k dispozici proton a místo toho často reagují dále na aminal:
nebo když je a-karbonyl proton přítomen na enamin:
V kyselém prostředí je reakčním produktem iminium sůl ztrátou vody.
Tento typ reakce se vyskytuje u mnoha Heterocykl přípravky například Povarovova reakce a Friedländerova syntéza na chinoliny.
Protože obě složky jsou tak reaktivní, molekula nenese aldehyd a aminoskupinu současně, pokud aminoskupina není vybavena a ochranná skupina. Jako další demonstrace reaktivity jedna studie[3] prozkoumal vlastnosti α-formyl aziridin u kterého bylo zjištěno dimerizovat jako oxazolidin na formaci z odpovídající ester podle organická redukce s DIBAL:[4]

Tvorba iminiových iontů je v této molekule zakázána, protože se říká, že jsou to azirinová skupina a formylová skupina ortogonální.
Rozsah
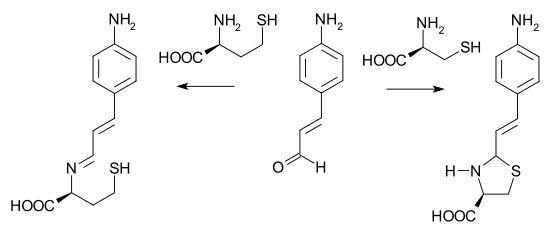
V jedné potenciální aplikaci[5] str-aminocinnamaldehyd je schopen rozlišovat mezi cystein a homocystein. U cysteinu se pufrovaný vodný roztok aldehydu mění ze žluté na bezbarvý v důsledku reakce iminu s uzavřením sekundárního kruhu. Homocystein není schopen uzavřít kruh a barva se nemění.
Reference
- ^ Organické syntézy, Sb. Sv. 6, str. 901 (1988); Sv. 50, str. 66 (1970). Článek Archivováno 2012-07-28 na Wayback Machine
- ^ March Jerry; (1985). Pokročilé reakce, mechanismy a struktura organické chemie (3. vyd.). New York: John Wiley & Sons, Inc. ISBN 0-471-85472-7
- ^ Hili, Ryan; Yudin, Andrei K. (2006). "Snadno dostupné nechráněné aminoaldehydy". Journal of the American Chemical Society. 128 (46): 14772–14773. doi:10.1021 / ja065898s. PMID 17105264.
- ^ Dimer reaguje s borohydrid sodný přes monomer, ve kterém je rovnováha s aziridinem alkohol
- ^ Wang, Weihua; Rusin, Oleksandr; Xu, Xiangyang; Kim, Kyu Kwang; Escobedo, Jorge O .; Fakayode, Sayo O .; Fletcher, Kristin A .; Lowry, Mark; Schowalter, Corin M .; Lawrence, Candace M .; Fronczek, Frank R .; Warner, Isiah M .; Strongin, Robert M. (2005). "Detekce homocysteinu a cysteinu". Journal of the American Chemical Society. 127 (45): 15949–15958. doi:10.1021 / ja054962n. PMC 3386615. PMID 16277539.
externí odkazy
- reakce benzaldehyd a methylamin v Organické syntézy Sb. Sv. 10, s. 312 (2004); Sv. 76, s. 23 (1999). Online článek
- reakce methylbenzylamin s 2-methylcyklohexanonem v Organické syntézy, Sb. Sv. 9, s. 610 (1998); Sv. 70, s. 35 (1992). Článek
- Reakce acetofenon s methylamin v Organické syntézy, Sb. Sv. 6, s. 818 (1988); Sv. 54, s. 93 (1974). Článek
- Chirál Schiffova základna v Molbank 2005, M435 Článek