AGGF1 - AGGF1
Angiogenní faktor s G náplastí a FHA doménami 1 je protein že u lidí je kódován AGGF1 gen.[5][6][7]
AGGF1 je lidský gen, který funguje jako angiogenní faktor s G-patchem a doména spojená s forkhead.[8] Tento gen je převážně exprimován v aktivovaném, kyprém endoteliální buňky a jedná k regulaci angiogeneze a vaskulární vývoj.[9] Je známo, že AGGF1 interaguje s celou řadou proteinů podílejících se na vaskulárním vývoji.[10] Mutace na AGGF1 se podílejí na mnoha rakovinách a je známo, že způsobují vzácný vrozený stav, Klippel-Trenaunayův syndrom.[9][11][12]
Gen
Gen byl původně pojmenován VG5Q, což naznačuje, že se jednalo o vaskulární gen na chromozomu 5, ale název byl později změněn tak, aby odrážel jeho funkci, nikoli pouze jeho umístění.[13]
Promotor genu AGGF1 neobsahuje a TATA box a obsahuje 2 transkripce počáteční weby, které jsou -367 a -364 párů bází před výchozím výchozím místem pro překlad.[13] Genový promotor obsahuje přes 50 CpG ostrovy, což z něj dělá Methylace DNA cílová.[13] AGGF1 je regulován 2 represorovými místy a 2 aktivačními místy.[13] Zatímco přítomnost 2 represorových a 2 aktivačních míst je jasná, jediný známý transkripční faktor, který reguluje AGGF1, je GATA1.[13] GATA1 se váže před promotorem genu AGGF1 na -295 a -300 a vazba GATA1 povede ke zvýšené expresi AGGF1.[9][13] Aby byl gen plně exprimován, musí být obě aktivátorová místa vázána transkripčními faktory, GATA1 a dalším neznámým faktorem.[13]
Protein
K vytvoření proteinu musí být transkript mRNA přepsal z DNA. U AGGF1 obsahuje transkript mRNA 14 exonů a 34 807 nukleotidů.[5]
Tento protein obsahuje 714 aminokyselin a má molekulovou hmotnost 80 997 Da.[14] Obsahuje a doména svinuté cívky na pozicích 18-88 a doména OCRE na N konec.[14] Doména G-patch je umístěna na aminokyselinách 619-663, zatímco doména spojená s vidlicí je umístěna na aminokyselinách 435-508.[14] I když je známo, že tyto domény jsou v proteinu přítomny, jejich role ve funkci proteinu zůstává nejasná.
AGGF1 byl třetí haploinsufficient identifikován lidský gen.[9] Haploinsufficiency znamená, že AGGF1 je „závislý na dávce“, takže může mít jakékoli snížení proteinového produktu fenotypový důsledky na cévní vývoj organismu.
Výraz
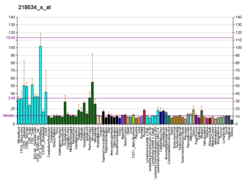
AGGF1 je do značné míry exprimován během specifikace časné embryonální žíly a exprese je zvýšena, když jsou aktivovány endoteliální buňky.[14][8] Zatímco AGGF1 je převážně funkční v endoteliální, buňky hladkého svalstva cév, a osteoblasty, má také činnost v žírné buňky, srdeční buňky, Kupfferovy buňky a hematopoetické kmenové buňky.[13][8][15][16] AGGF1 mRNA byla detekována v srdci, ledvinách a končetinách, což naznačuje, že protein pravděpodobně také funguje v těchto orgánech.[14] Když je exprimován AGGF1, je inhibována proliferace buněk hladkého svalstva cév.[17] Bylo zjištěno, že AGGF1 je vysoce exprimován v některých maligních nádorech, což implikuje AGGF1 v rakovině.[17] In vitro modely ukázaly, že AGGF1 se lokalizuje na periferii buňky a přímo mimo buňku.[16]
V závislosti na typu mutace mohou být mutace AGGF1 smrtelné buď v heterozygotním nebo homozygotním genotypu kvůli jeho haploinsufficienci.[14] Myší modely ukázaly, že heterozygotní mutace mohou způsobit smrt krvácení zatímco homozygotní mutace mohou zabránit správné diferenciaci kmenových buněk.[14]
Homologie
Aggf1 není pro člověka jedinečný. Tento gen je konzervovaný u mnoha druhů, jako jsou šimpanzi, opice Rhesus, psi, krávy, myši, krysy, kuřata a žáby.[7] Existuje 212 organismů, které mají geny, které jsou ortology na AGGF1.[7]
V lidském chromozomu existují pseudogeny související s AGGF1 se nacházejí na chromozomech 3, 4, 10 a 16, které pravděpodobně vznikly v důsledku přemístění Události.[7]
Funkce
Funkce AGGF1 reguluje angiogeneze a vaskulární vývoj.[9] Genová ontologie se také podílí na AGGF1 v buněčné adhezi, pozitivní regulaci angiogeneze a proliferaci endoteliálních buněk.[7] Navíc se ukázalo, že AGGF1 chrání před záněty a ischemickými poraněními.[15] Během embryongeneze je AGGF1 vyžadován pro specifikaci hematopoetických kmenových buněk a pro diferenciaci linií hematopoetických a endoteliálních buněk.[14] Konkrétně reguluje vaskulární endotel kadherin (VE-kadherin) inhibicí fosforylace kadherinu a zvýšením jeho přítomnosti v plazmatická membrána endotelových buněk.[9] AGGF1 je rozhodující pro specifikaci žil a multipotentní hemanigioblasty, protizánětlivé, nádorové angiogeneze a inhibice vaskulární permeability.[18] Navíc se aktivuje autofagie ve specifických typech buněk, jako je endoteliální buňky, srdeční buňky HL1 a H9C2 a buňky hladkého svalstva cév.[9][14][18]
Interakce
AGGF1 přímo a nepřímo interaguje s mnoha proteiny. Mezi AGGF1 a TNFSF12, další vylučovaný angiogenní faktor, který vede ke zvýšené angiogenezi.[16] AGGF1 působí upstream od hemangioblastových genů, jako jsou scl, fil1 a etsrp.[10] AGGF1 funguje podobně jako VEGF - další gen podílející se na vaskulárním růstu.[10] Navíc je známo, že AGGF1 aktivuje katalytické a regulační podjednotky PI3K.[9] To vede k následné aktivaci AKT, GSK3b a p70S6K signální dráha, která vede ke specifikaci žíly a angiogenezi.[9][10] AGGF1 také interaguje s markery specifickými pro žíly, např flt4, dab2, a ephB4.[19] Ccl2 Bylo také prokázáno, že interaguje s AGGF1 v hepatocyty prostřednictvím blokování NF-kB / p65 z vazby na Ccl2.[20] Aktivita AGGF1 je eliminována, když je Elk nadměrně exprimován.[17] AGGF1 reguluje autofagii regulací exprese genů JNK.[17] SMAD7 a Aggf1 přímo interagují v játrech a inhibují fibrogenezi.[15] Přítomnost někoho DNMT3b bude potlačovat AGGF1 působením na promotorovou oblast genu.[15]
Klinický význam
Klippel-Trenaunayův syndrom
Heterogenní mutace v tomto genu způsobující deregulaci exprese mohou vést k vaskulárním malformacím spojeným s Klippel-Trenaunayův syndrom (KTS).[9][13][19] Kvůli haploinsufficient povaze AGGF1, jedinci, kteří mají dokonce jednu mutovanou alelu, mohou mít KTS.[9] Studie provedené na modelech myší ukázaly časté krvácení a zvýšená vaskulární permeabilita byla pozorována u myší, které jsou heterozygotní pro Aggf1.[9] Translokace mezi q-ramenem chromozomu 5 v oblasti 13 v pásmu 3 a p-ramenem chromozomu 11 v oblasti 15 v pásmu 1 byla implikována v KTS.[5] Tato translokace ovlivňuje promotor AGGF1, takže dochází k trojnásobnému zvýšení produkce proteinu.[5] Jednonukleotidové polymorfismy v intronu 11 a exonu 7 byly spojeny s citlivostí na KTS, i když žádný z těchto SNP nevedl ke změně aminokyselin.[5] V jednom okamžiku se alela E133K považovala za mutační hotspot - kvůli změněné fosforylaci způsobující KTS, ale od té doby bylo zjištěno, že až 3,3% populace je nositeli mutace.[16][21]
Srdeční choroba
AGGF1 se také podílí na léčbě po poškození buněk hladkého svalstva cév v důsledku ischemická choroba srdeční a infarkt myokardu.[17] Blokováním vaskulární permeability a regulací fenotypové změny buněk vaskulárního hladkého svalstva je v současné době zkoumána proteinová terapie AGGF1 jako nová metoda léčby obou těchto onemocnění.[17]
Rakovina
Aberantní AGGF1 se podílí na mnoha rakovinách a funkcích při iniciaci a progresi nádoru.[12] Například jak hepatocelulární karcinom, tak přežití rakoviny žaludku souvisí s hladinami exprese AGGF1 v nádorech.[11][12] Bylo zjištěno, že AGGF1 má vyšší expresi v nádorech než okolní tkáně a vyšší hladiny AGGF1 jsou spojeny se špatnou prognózou pacienta.[11][12]
Viz také
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000164252 - Ensembl, Květen 2017
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000021681 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ A b C d E Hu Y, Li L, Seidelmann SB, Timur AA, Shen PH, Driscoll DJ, Wang QK (září 2008). „Identifikace asociace běžných variant AGGF1 s citlivostí na syndrom Klippel-Trenaunay pomocí programu asociační struktury“. Annals of Human Genetics. 72 (Pt 5): 636–43. doi:10.1111 / j.1469-1809.2008.00458.x. PMC 2602961. PMID 18564129.
- ^ Gutierrez S, Magano L, Delicado A, Mori MA, de Torres ML, Fernández L, Palomares M, Fernández E, Tarduchy GR, Molano J, Gracia R, Pajares IL, Lapunzina P (prosinec 2006). „Změna G397A (E133K) v genu AGGF1 (VG5Q) je ve španělské populaci jediným nukleotidovým polymorfismem.“ American Journal of Medical Genetics. Část A. 140 (24): 2832–3. doi:10,1002 / ajmg.a.31532. PMID 17103452. S2CID 19068189.
- ^ A b C d E „Entrez Gene: AGGF1 angiogenní faktor s G náplastí a FHA doménami 1“.
- ^ A b C Zhan M, Hori Y, Wada N, Ikeda J, Hata Y, Osuga K, Morii E (duben 2016). „Angiogenní faktor s G-náplastí a expresí FHA domény 1 (AGGF1) v lidských vaskulárních lézích“. Acta Histochemica et Cytochemica. 49 (2): 75–81. doi:10,1267 / ahc.15035. PMC 4858542. PMID 27222614.
- ^ A b C d E F G h i j k l Zhang T, Yao Y, Wang J, Li Y, He P, Pasupuleti V, Hu Z, Jia X, Song Q, Tian XL, Hu C, Chen Q, Wang QK (prosinec 2016). „Haploinsufficience genu pro Klippel-Trenaunayův syndrom Aggf1 inhibuje vývojovou a patologickou angiogenezi deaktivací PI3K a AKT a narušuje vaskulární integritu aktivací VE-kadherinu“. Lidská molekulární genetika. 25 (23): 5094–5110. doi:10,1093 / hmg / ddw273. PMC 6078640. PMID 27522498.
- ^ A b C d Li L, Chen D, Li J, Wang X, Wang N, Xu C, Wang QK (leden 2014). „Aggf1 působí na špici genetické regulační hierarchie ve specifikaci hemangioblastů u zebrafish“. Krev. 123 (4): 501–8. doi:10.1182 / krev-2013-07-514612. PMC 3901065. PMID 24277077.
- ^ A b C Yao HH, Wang BJ, Wu Y, Huang Q (2017). „Vysoká exprese angiogenního faktoru s G-Patch a doménou FHA1 (AGGF1) předpovídá špatnou prognózu u rakoviny žaludku“. Monitor lékařské vědy. 23: 1286–1294. doi:10,12659 / msm.903248. PMC 5362190. PMID 28289272.
- ^ A b C d Wang W, Li GY, Zhu JY, Huang DB, Zhou HC, Zhong W, Ji CS (duben 2015). „Nadměrná exprese AGGF1 koreluje s angiogenezí a špatnou prognózou hepatocelulárního karcinomu“. Lékařská onkologie. 32 (4): 131. doi:10.1007 / s12032-015-0574-2. PMID 25796501. S2CID 25099244.
- ^ A b C d E F G h i Fan C, Ouyang P, Timur AA, He P, You SA, Hu Y, Ke T, Driscoll DJ, Chen Q, Wang QK (srpen 2009). „Nové role GATA1 v regulaci angiogenního faktoru AGGF1 a funkce endoteliálních buněk“. The Journal of Biological Chemistry. 284 (35): 23331–43. doi:10.1074 / jbc.M109.036079. PMC 2749107. PMID 19556247.
- ^ A b C d E F G h i Liu Y, Yang H, Song L, Li N, Han QY, Tian C, Gao E, Du J, Xia YL, Li HH (srpen 2014). „AGGF1 chrání před ischemickým / reperfuzním poškozením myokardu regulací apoptózy a angiogeneze myokardu“. Apoptóza. 19 (8): 1254–68. doi:10.1007 / s10495-014-1001-4. PMID 24893993. S2CID 7164539.
- ^ A b C d Zhou B, Zeng S, Li L, Fan Z, Tian W, Li M, Xu H, Wu X, Fang M, Xu Y (červen 2016). „Angiogenní faktor s G náplastí a FHA doménami 1 (Aggf1) reguluje fibrózu jater modulací signalizace TGF-β“. Biochimica et Biophysica Acta (BBA) - Molekulární základ choroby. 1862 (6): 1203–13. doi:10.1016 / j.bbadis.2016.02.002. PMID 26850475.
- ^ A b C d Tian XL, Kadaba R, You SA, Liu M, Timur AA, Yang L, Chen Q, Szafranski P, Rao S, Wu L, Housman DE, DiCorleto PE, Driscoll DJ, Borrow J, Wang Q (únor 2004). „Identifikace angiogenního faktoru, který při mutaci způsobí náchylnost k syndromu Klippel-Trenaunay“. Příroda. 427 (6975): 640–5. doi:10.1038 / nature02320. PMC 1618873. PMID 14961121.
- ^ A b C d E F Yao Y, Hu Z, Ye J, Hu C, Song Q, Da X, Yu Y, Li H, Xu C, Chen Q, Wang QK (červen 2017). „Cílení na AGGF1 (angiogenní faktor s G náplastí a doménami FHA 1) pro blokování tvorby neointimy po vaskulárním poranění“. Journal of the American Heart Association. 6 (6): e005889. doi:10.1161 / JAHA.117.005889. PMC 5669188. PMID 28649088.
- ^ A b Lu Q, Yao Y, Hu Z, Hu C, Song Q, Ye J, Xu C, Wang AZ, Chen Q, Wang QK (srpen 2016). „Angiogenní faktor AGGF1 aktivuje autofagii se základní rolí v terapeutické angiogenezi pro srdeční onemocnění“. PLOS Biology. 14 (8): e1002529. doi:10.1371 / journal.pbio.1002529. PMC 4981375. PMID 27513923.
- ^ A b Chen D, Li L, Tu X, Yin Z, Wang Q (březen 2013). „Funkční charakterizace genu pro Klippel-Trenaunayův syndrom AGGF1 identifikuje novou angiogenní signální cestu pro specifikaci diferenciace a angiogeneze žil během embryogeneze.“. Lidská molekulární genetika. 22 (5): 963–76. doi:10,1093 / hmg / dds501. PMID 23197652.
- ^ Xu W, Zeng S, Li M, Fan Z, Zhou B (září 2017). „Aggf1 tlumí zánět jater a aktivaci jaterních hvězdných buněk potlačováním transkripce Ccl2“. Journal of Biomedical Research. 31 (5): 428–436. doi:10.7555 / JBR.30.20160046. PMC 5706435. PMID 28958996.
- ^ Barker KT, Foulkes WD, Schwartz CE, Labadie C, Monsell F, Houlston RS, Harper J (červenec 2006). „Je alela E133K VG5Q spojena s Klippel-Trenaunay a dalšími syndromy přerůstání?“. Journal of Medical Genetics. 43 (7): 613–4. doi:10.1136 / jmg.2006.040790. PMC 2564558. PMID 16443853.
Další čtení
- Timur AA, Driscoll DJ, Wang Q (červenec 2005). „Biomedicína a nemoci: syndrom Klippel-Trenaunay, vaskulární anomálie a vaskulární morfogeneze“. Buněčné a molekulární biologické vědy. 62 (13): 1434–47. doi:10.1007 / s00018-005-4523-7. PMC 1579804. PMID 15905966.
- Kihiczak GG, Meine JG, Schwartz RA, Janniger CK (srpen 2006). „Klippel-Trenaunayův syndrom: multisystémová porucha pravděpodobně vyplývající z patogenního genu pro nadměrný růst cév a tkání“. International Journal of Dermatology. 45 (8): 883–90. doi:10.1111 / j.1365-4632.2006.02940.x. PMID 16911369. S2CID 7238399.
- Dias Neto E, Correa RG, Verjovski-Almeida S, Briones MR, Nagai MA, da Silva W, Zago MA, Bordin S, Costa FF, Goldman GH, Carvalho AF, Matsukuma A, Baia GS, Simpson DH, Brunstein A, de Oliveira PS, Bucher P, Jongeneel CV, O'Hare MJ, Soares F, Brentani RR, Reis LF, de Souza SJ, Simpson AJ (březen 2000). "Brokovnicové sekvenování lidského transkriptomu se značkami sekvencí exprimovanými ORF". Sborník Národní akademie věd Spojených států amerických. 97 (7): 3491–6. doi:10.1073 / pnas.97.7.3491. PMC 16267. PMID 10737800.
- Tian XL, Kadaba R, You SA, Liu M, Timur AA, Yang L, Chen Q, Szafranski P, Rao S, Wu L, Housman DE, DiCorleto PE, Driscoll DJ, Borrow J, Wang Q (únor 2004). „Identifikace angiogenního faktoru, který při mutaci způsobí náchylnost k syndromu Klippel-Trenaunay“. Příroda. 427 (6975): 640–5. doi:10.1038 / nature02320. PMC 1618873. PMID 14961121.
- Callebaut I, Mornon JP (březen 2005). „OCRE: nová doména vyrobená z nedokonalých, aromaticky bohatých oktamerových opakování“. Bioinformatika. 21 (6): 699–702. doi:10.1093 / bioinformatika / bti065. PMID 15486042.
- Rual JF, Venkatesan K, Hao T, Hirozane-Kishikawa T, Dricot A, Li N, Berriz GF, Gibbons FD, Dreze M, Ayivi-Guedehoussou N, Klitgord N, Simon C, Boxem M, Milstein S, Rosenberg J, Goldberg DS, Zhang LV, Wong SL, Franklin G, Li S, Albala JS, Lim J, Fraughton C, Llamosas E, Cevik S, Bex C, Lamesch P, Sikorski RS, Vandenhaute J, Zoghbi HY, Smolyar A, Bosak S, Sequerra R, Doucette-Stamm L, Cusick ME, Hill DE, Roth FP, Vidal M (říjen 2005). „Směrem k mapě interakční sítě lidský protein-protein v měřítku proteomu“. Příroda. 437 (7062): 1173–8. doi:10.1038 / nature04209. PMID 16189514. S2CID 4427026.
- Barker KT, Foulkes WD, Schwartz CE, Labadie C, Monsell F, Houlston RS, Harper J (červenec 2006). „Je alela E133K VG5Q spojena s Klippel-Trenaunay a dalšími syndromy přerůstání?“. Journal of Medical Genetics. 43 (7): 613–4. doi:10.1136 / jmg.2006.040790. PMC 2564558. PMID 16443853.
externí odkazy
- Člověk AGGF1 umístění genomu a AGGF1 stránka s podrobnostmi o genu v UCSC Genome Browser.