Thiofosfát - Thiophosphate
- Pro estery thiofosfátu viz organothiofosfáty.
Thiofosfáty (nebo fosforothioáty, PS) jsou chemické sloučeniny a anionty s generálem chemický vzorec PS
4−XÓ3−
X (X = 0, 1, 2 nebo 3) a příbuzné deriváty, kde jsou organické skupiny připojeny k jednomu nebo více O nebo S. Thiofosfáty obsahují tetrahedrální fosforová (V) centra.[1]
Organické
Organothiofosfáty jsou podtřídou organofosforové sloučeniny které jsou strukturně příbuzné s anorganickými thiofosfáty. Běžní členové mají vzorce typu (RO)3−XRXPS a příbuzné sloučeniny, kde RO je nahrazen RS. Mnoho z těchto sloučenin se používá jako insekticidy, některé mají lékařské aplikace a některé byly použity jako přísady do olejů.[1]
- Vybrané organothiofosfáty

dialkyldithiofosfát zinečnatý, přísada do oleje.[2]

Fosforothioáty jsou základem pro antisense terapie.

Amifostin, který se používá při chemoterapii rakoviny.
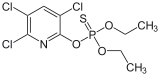
Chlorpyrifos, populární insekticid.
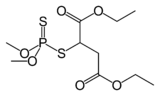
Malathion, populární insekticid.
Oligonukleotid fosforothioáty (OPS) jsou modifikované oligonukleotidy, kde je jeden z atomů kyslíku ve fosfátové části nahrazen sírou. Jsou základem antisense terapie např. léky fomivirsen (Vitravene), oblimersen, alicaforsen, a mipomersen (Kynamro).[3]
Anorganické

Nejjednodušší thiofosfáty mají vzorec [PS4−XÓX]3−. Tyto trianionty jsou pozorovány pouze při velmi vysokém pH, místo toho existují v protonované formě se vzorcem [HnPS4−XÓX](3−n)− (x = 0, 1, 2 nebo 3 a (n = 1, 2 nebo 3).
Monothiofosfát

Monothiofosfát je anion [PO3S]3−, který má C.3v symetrie. Obyčejná sůl je monothiofosforečnan sodný (Na3PO3S). Monothiofosfát se ve výzkumu používá jako analog fosfátu v biochemie. Monothiofosfátové estery jsou biochemické činidla použitý při studiu transkripce,[4] testy substituční interference. "Monothiofosfát" někdy označuje estery, jako je (CH3Ó)2POS−.[5]
Dithiofosfáty
Dithiofosfát má vzorec [PO2S2]3−, který má C.2v symetrie. Dithiofosforečnan sodný, který je bezbarvý, je hlavním produktem reakce sulfid fosforečný s NaOH:[6]
- P2S5 + 6 NaOH → 2 Na3PO2S2 + H2S + 2 H2Ó
Kyselina dithiofosforečná se získá zpracováním dithiofosforečnanu barnatého s kyselina sírová:
- Ba3(PO2S2)2 + 3 H2TAK4 → 3 BaSO4 + 2 H3PO2S2
Oba Na3PO2S2 a zejména H3PO2S2 jsou náchylní k hydrolýze na své monothioderiváty.
Tri- a tetrathiofosfáty
Trithiofosfát je anion [POS3]3−, který má C.3v symetrie. Tetrathiofosfát je anion [PS4]3−, který má Td symetrie.
PXSy: binární thiofosfáty a polyfosfáty

Je známa řada těchto aniontů. Některé přitahovaly zájem jako komponenty v rychlé iontové vodiče pro použití v polovodičových bateriích. Binární thiofosfáty nevykazují rozsáhlou rozmanitost analogických P-O aniontů, ale obsahují podobné strukturní rysy, například P je 4 souřadnice, tvoří se vazby P-S-P a existují vazby P-P. Jeden rozdíl spočívá v tom, že ionty mohou zahrnovat polysulfidové fragmenty 2 nebo více atomů S, zatímco v aniontech P-O existuje pouze reaktivní jednotka -O-O-, peroxo.
- PS−
3 je obdobou dusičnan ion, NE−
3 (tady není žádný PO−
3 analog); byla izolována jako žlutá tetrafenylarsoniová sůl[8] - PS3−
4 je analog síry PO3−
4a podobně PO3−
4 je čtyřboká. - P
2S4−
7 pyrothiofosfátový iont skládající se ze dvou rohových sdílení PS4 čtyřstěn, analogický k pyrofosfáty.[9] - P
2S4−
10 Ion, který lze vizualizovat buď jako dva PS4 čtyřstěn spojený a disulfid článek nebo pyrothiofosfát, kde je přemostění −S− nahrazeno −S4−.[10] - P
2S2−
6 okrajově sdílená bitetrahedrická struktura. Struktura je tedy podobná izoelektronice Al2Cl6 dimer. Analog kyslíku, dimetafosfát P
2Ó2−
6na rozdíl od toho není známo, metafosfáty upřednostňují polymerní struktury řetězců nebo kruhů.[9] - P
2S2−
8 a P
2S2−
10 souvisí s P
2S2−
6 ale jejich dva přemosťující −S− atomy jsou nahrazeny −S − S− in P
2S2−
8 a mostem −S − S − S− v P
2S2−
10.[11] - P2S4−
6 Ty tvoří ve vodě stabilní soli.[12] Anion má etan struktura podobná a obsahuje vazbu P-P. Formální oxidační stav fosforu je +4. Analogem kyslíku je hypodifosfátový anion, P
2Ó4−
6. - P
3S3−
9 obsahuje šestičlennou P3S3 prsten. Amonná sůl se vyrábí reakcí P4S10 v kapalném amoniaku.[13] Dalším způsobem vizualizace struktury je, že se jedná o P4S10 adamantan (Str4Ó10) struktura s PS3+ vrchol odstraněn. - P
4S4−
8 obsahuje čtverec P4 prsten,[8] P
5S5−
10 obsahuje P.5 prsten a P
6S6−
12 a P6 prsten.[11] Tyto (PS−
2)
n cyklické anionty obsahují P s oxidačním stavem +3. Všimněte si, že nejsou trigonální, protože je v nich arsen (III) arzenity, ale jsou čtyřboká se dvěma vazbami na jiné atomy fosforu a dvěma na síru. The P
6S6−
12 anion je analogický k P
6Ó6−
12 kruhový anion.[14] - P
4S2−
2 Neobvyklý iont ve tvaru motýla, SP (str2) PS, které lze vizualizovat jako a P4 molekula, kde dvě vazby P-S nahradí jednu vazbu P-P.[15] - P
7S3−
3 je klastrový anion sulfido heptafosfanu.[8]
Reference
- ^ A b J. Svara, N. Weferling, T. Hofmann "Fosforové sloučeniny, organické" v Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2006. doi:10.1002 / 14356007.a19_545.pub2
- ^ H. Spikes "Historie a mechanismy ZDDP" Tribology Letters, sv. 17, č. 3, říjen 2004. doi:10.1023 / B: TRIL.0000044495.26882.b5.
- ^ Kurreck, J., "Antisense technologie. Zlepšení pomocí nových chemických modifikací", European Journal of Biochemistry 2003, 270, 1628-1644.doi:10.1046 / j.1432-1033.2003.03555.x
- ^ Lorsch JR; Bartel DP; Szostak JW (1995). „Reverzní transkriptáza čte prostřednictvím vazby 2′ – 5 ′ a 2′-thifosfátu v šabloně“. Nucleic Acids Res. 23 (15): 2811–2814. doi:10.1093 / nar / 23.15.2811. PMC 307115. PMID 7544885.
- ^ Poat JC a kol. (1990). „Thiofosfátový můstek heterobimetalový komplex platina-zinek: [(Me2PhP)2Pt {OSP (NEBO)2}2ZnCl2". J. Chem. Soc., Chem. Commun.: 1036–1038.
- ^ R. Klement „Fosfor“ v Příručce preparativní anorganické chemie, 2. vyd. Edited by G. Brauer, Academic Press, 1963, NY. Sv. 1., s. 571.
- ^ Dimitrov, A .; Hartwich, I .; Ziemer, B .; Heidemann, D. ;; Meisel, M. (2005). „Synthese, Charakterisierung und Struktur des donorstabilisierten monomeren [PS3]− - Anionty (monometatrithiofosfáty) ". Zeitschrift für anorganische und allgemeine Chemie. 631: 2439–2444. doi:10.1002 / zaac.200500246.CS1 maint: extra interpunkce (odkaz)
- ^ A b C Greenwood, Norman N.; Earnshaw, Alan (1984). Chemie prvků. Oxford: Pergamon Press. 509–510. ISBN 978-0-08-022057-4.
- ^ A b Phosphorus: Chemistry, Biochemistry and Technology, Sixth Edition, 2013, D.E.C. Corbridge, CRC Pres, Taylor Francis Group, ISBN 978-1-4398-4088-7
- ^ Aitken, Jennifer A .; Canlas, Christian; Weliky, David P .; Kanatzidis, Mercouri G. (2001). „[Str2S10]4−: Nový polythiofosfátový anion obsahující fragment tetrasulfidu ". Anorganická chemie. 40 (25): 6496–6498. doi:10.1021 / ic010664p. ISSN 0020-1669.
- ^ A b Holleman, Arnold Frederik; Wiberg, Egon (2001), Wiberg, Nils (ed.), Anorganická chemie, přeloženo Eaglesonem, Mary; Brewer, William, San Diego / Berlin: Academic Press / De Gruyter, str. 734–735, ISBN 0-12-352651-5
- ^ Gjikaj, Mimoza; Ehrhardt, Claus (2007). „Nové hexachalkogeno – hypodifosfáty alkalických kovů: syntéza, krystalová struktura a vibrační spektrum hydrátů hexathiodifosfátu (IV) K4[Str2S6] · 4 H2O, Rb4[Str2S6] · 6 H2O a Cs4[Str2S6] · 6 H2Ó". Zeitschrift für anorganische und allgemeine Chemie. 633 (7): 1048–1054. doi:10.1002 / zaac.200600339. ISSN 0044-2313.
- ^ Wolf, G.-U .; Meisel, M. (1982). „Beiträge zur Chemie von Phosphorverbindungen mit Adamantanstruktur. VII [1]. Über Darstellung und Eigenschaften von Nonathio-cyclotriphosphat“. Zeitschrift für anorganische und allgemeine Chemie. 494 (1): 49–54. doi:10.1002 / zaac.19824940106. ISSN 0044-2313.
- ^ Ebert, M .; Nassler, J. (1989). „Kruhová kyselina, H6P6Ó12 a Ring Acid, H4P4Ó10 a jejich soli “. Fosfor, síra a křemík a související prvky. 41 (3–4): 462. doi:10.1080/10426508908039741. ISSN 1042-6507.
- ^ Rotter, Christiane; Schuster, Michael; Karaghiosoff, Konstantin (2009). „Neobvyklý binární fosfor - anion teluria a jeho seleneno- a thioanalogy: P
4Ch2−
2 (Ch = S, Se, Te) ". Anorganická chemie. 48 (16): 7531–7533. doi:10,1021 / ic901149m. ISSN 0020-1669.





