Fosforamid - Phosphoramide - Wikipedia
 | |
| Jména | |
|---|---|
| Název IUPAC Triamid fosforečný | |
| Ostatní jména Amid fosforečný; Diaminofosforylamin | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| H6N3ÓP | |
| Molární hmotnost | 95.042 g · mol−1 |
| Vzhled | bílá pevná látka |
| dobrý | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
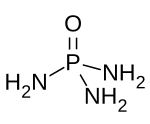
Fosforamid je chemická sloučenina s molekulárním vzorcem O = P (NH2)3. Je to derivát z kyselina fosforečná ve kterém každý z hydroxylové skupiny byly nahrazeny aminoskupina. Fosforamid vzniká reakcí fosforylchloridu s amoniakem. Je to bílá pevná látka, která je rozpustná v polární rozpouštědla. Ve vlhkém vzduchu hydrolyzuje na amonnou sůl:
- 2 H2O + OP (NH2)3 → NH4+[HPO3(NH2)] + NH3
Reaguje s hydroxidem sodným se ztrátou amoniak:[1]
- NaOH + OP (NH2)3 → NaO2P (NH2)2 + NH3
Příbuzná thiofosforylová sloučenina P (= S) (NH2)3 byl vyroben z reakce thiofosforylchlorid s amoniakem.
Fosforamidy
Fosforamid je také základní sloučeninou řady derivátů nazývaných fosforamidy.[2] Příkladem sloučeniny je polární rozpouštědlo hexamethylfosforamid (HMPA).
Reference
- ^ Robert Klement, Otto Koch (1954). „Phosphoroxy ‐ triamid und Phosphorthio ‐ triamid“. Chemische Berichte. 87: 333–340. doi:10,1002 / cber.19540870308.CS1 maint: používá parametr autoři (odkaz)
- ^ IUPAC, Kompendium chemické terminologie, 2. vyd. („Zlatá kniha“) (1997). Online opravená verze: (2006–) “fosforamidy ". doi:10.1351 / goldbook.A00484
externí odkazy
 Média související s fosforamidy na Wikimedia Commons
Média související s fosforamidy na Wikimedia Commons Slovníková definice fosforamid na Wikislovníku
Slovníková definice fosforamid na Wikislovníku
