Salicylaldehyd - Salicylaldehyde
| |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC 2-hydroxybenzaldehyd[1] | |||
| Ostatní jména Salicylaldehyd Salicylová aldehyd Ó-Hydroxybenzaldehyd | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Informační karta ECHA | 100.001.783 | ||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C7H6Ó2 | |||
| Molární hmotnost | 122.123 g · mol−1 | ||
| Hustota | 1,146 g / cm3 | ||
| Bod tání | -7 ° C (26 ° K) | ||
| Bod varu | 196 až 197 ° C (385 až 387 ° F; 469 až 470 K) | ||
| -64.4·10−6 cm3/ mol | |||
| Nebezpečí | |||
| Bezpečnostní list | [2] | ||
| Piktogramy GHS |   | ||
| Signální slovo GHS | Varování | ||
| H302, H315, H317, H319, H335, H411[2] | |||
| P280, P305 + 351 + 338[2] | |||
| Související sloučeniny | |||
Související sloučeniny | Kyselina salicylová Benzaldehyd Salicylaldoxim | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Salicylová aldehyd (2-hydroxybenzaldehyd) je organická sloučenina se vzorcem C.6H4CHO-2-OH.[3] Spolu s 3-hydroxybenzaldehyd a 4-hydroxybenzaldehyd, je to jeden ze tří izomery z hydroxybenzaldehyd. Tato bezbarvá olejovitá kapalina má hořký mandlový zápach při vyšší koncentraci. Salicylaldehyd je klíčovým předchůdcem různých chelatačních činidel, z nichž některá jsou komerčně důležitá.
Výroba
Salicylaldehyd se připravuje z fenol a chloroform vytápěním pomocí hydroxid sodný nebo hydroxid draselný v Reimer – Tiemannova reakce:[4]
Alternativně se vyrábí kondenzací fenolu nebo jeho derivátů s formaldehydem, čímž se získá hydroxybenzylalkohol, který se oxiduje na aldehyd.
Salicylaldehydy lze obecně připravit z odpovídajícího fenolu metodou Duffova reakce nebo ošetřením paraformaldehyd v přítomnosti chlorid hořečnatý a základna.[5]
Přirozené výskyty
Salicylaldehyd byl identifikován jako charakteristická aroma složka pohanka.[6]
Je to také jedna ze složek castoreum, výpotek z kolečkových vaků dospělého bobra severoamerického (Castor canadensis ) a bobr evropský (Ricinové vlákno ), který se používá v parfumerii.
Salicylaldehyd se dále vyskytuje v larválních obranných sekretech několika insekt druhy, které patří do kmene Chrysomelina.[7] Příkladem druhu listového brouka, který produkuje salicylaldehyd, je listový brouk červený topol Chrysomela populi.
Reakce a aplikace
Salicylaldehyd se používá k výrobě:
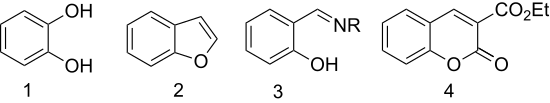
- Oxidace s peroxid vodíku dává katechol (1,2-dihydroxybenzen) (Dakinova reakce ).[8]
- Etherifikace s kyselina chloroctová následovaná cyklizací dává heterocyklus benzofuran (kumaron).[9] {První krok v této reakci na substituovaný benzofuran se nazývá Kondenzace Rap – Stoermer po E. Rapovi (1895) a R. Stoermerovi (1900).[10][11]
- Salicylaldehyd se převádí na chelátování ligandy kondenzací s aminy. S ethylendiamin kondenzuje za vzniku ligandu salen. Hydroxylamin dává salicylaldoxim.
- Kondenzace s diethyl malonát dává 3-karbethoxykumarin (derivát kumarin ) uživatelem kondenzace aldolu.[12]
Reference
- ^ „Přední záležitost“. Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 652. doi:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ A b C Sigma-Aldrich Co., Salicylaldehyd. Citováno 2018-05-24.
- ^ Index společnosti Merck, 11. vydání, 8295
- ^ Brühne, F .; Wright, E. „Benzaldehyd“. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a03_463.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Trond Vidar Hansen; Lars Skattebøl (2005). „Ortho-formylace fenolů; Příprava 3-bromsalicylaldehydu“. Organické syntézy. 82: 64.
- ^ Janeš, D .; Kreft, S. (2008). „Salicylaldehyd je charakteristickou aromatickou složkou pohankových krup“. Chemie potravin. 109 (2): 293–298. doi:10.1016 / j.foodchem.2007.12.032. PMID 26003350.
- ^ Pauls, G., Becker, T. a kol. (2016). Dvě obranné linie v broucích mladistvých; Estery kyseliny 3-nitropropionové v varování před hemolymfou a aposematem. Journal of Chemical Ecology 42 (3) 240-248.
- ^ Dakin, H. D. (1923). "Katechol" (PDF). Organické syntézy. 3: 28.; Kolektivní objem, 1, str. 149
- ^ Burgstahler, A. W .; Worden, L. R. (1966). „Coumarone“ (PDF). Organické syntézy. 46: 28.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 5, str. 251
- ^ Rap, E. (listopad 1895). „Sull 'α-Benzoilcumaron“ [Na α-benzoylcoumaronu]. Gazzetta Chimica Italiana. 2 (4): 285–290.
- ^ Stoermer, R. (1900). „Synthesen und Abbaureactionen in der Cumaronreihe“. Liebigova Annalen der Chemie. 312 (3): 237–336. doi:10.1002 / jlac.19003120302.
- ^ Horning, E. C .; Horning, M. G .; Dimmig, D. A. (1948). „3-karbethoxykumarin“ (PDF). Organické syntézy. 28: 24.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 3, str. 165



