Spojka srdeční excitace-kontrakce - Cardiac excitation-contraction coupling
Spojka srdeční excitace-kontrakce (Srdeční EC spojka) popisuje sérii událostí od produkce AN elektrický impuls (akční potenciál) do kontrakce z svaly v srdce.[1] Tento proces má zásadní význam, protože umožňuje srdce bít kontrolovaně, bez nutnosti vědomého vstupu. Výsledkem EC vazby je postupnost kontrakce z srdeční svaly to umožňuje krev být čerpán, nejprve do plíce (plicní oběh ) a poté kolem zbytku těla (systémový oběh ) rychlostí 60 až 100 tepů každou minutu, když je tělo v klidu.[2] Tuto sazbu však lze změnit pomocí nervy které buď zvyšují srdeční frekvenci (sympatické nervy ) nebo snížit (parasympatické nervy ), jako tělo kyslík požaduje změnu. Nakonec, svalová kontrakce se točí kolem a nabitý atom (iont), vápník (Ca2+),[3] který je zodpovědný za přeměnu elektrické energie na akční potenciál do mechanické energie (kontrakce) svalu. Toho je dosaženo v oblasti svalové buňky, která se nazývá příčný tubul během procesu známého jako uvolňování vápníku indukované vápníkem.[4]
Zahájení
Nachází se ve zdi pravé síně je skupina specializovaných buněk zvaná Sinoatriální uzel (SAN). Tyto buňky, na rozdíl od většiny ostatních buňky v rámci srdce, mohou spontánně produkovat akční potenciály.[5] Tyto akční potenciály cestovat po buněčná membrána (sarkolemma) jako impulsy procházející z jedné buňky do druhé kanály, ve strukturách známých jako mezery křižovatky.[6] Rychlost vedení akční potenciál se liší v různých částech souboru srdce (pro více informací viz systém elektrického vedení srdce ). To je důležité, protože to znamená, že jakmile atria uzavřely smlouvu, došlo k mírnému zpoždění, které umožňuje komory naplnit krví, než se stáhnou.
Uvolňování vápníku vyvolané vápníkem
Některé regiony EU sarcolemma proniknout hluboko do buňka. Tito jsou známí jako příčné tubuly (t-tubuly); které se také nacházejí v buňky kosterního svalstva) a počítat s akční potenciál cestovat do středu buňky.[7] Speciální bílkoviny volala Vápníkové kanály typu L (známé také jako dihydropyridinové receptory (DHPR)) jsou umístěny na membrána t-tubulu, a jsou aktivovány akčním potenciálem. Aktivované DHPR je otevřené, tvoří a kanál, což umožňuje Ca2+ projít do cely. Toto zvýšení Ca2+, pak se naváže na a aktivuje další receptor, nazvaný a ryanodinový receptor typu 2 (RyR2), který se nachází na membráně struktury známé jako sarkoplazmatické retikulum (SR). The SR je Ca.2+ skladovat v buňce a nachází se velmi blízko T-tubulu. Aktivace RyR2 způsobí jeho otevření a uvolnění ještě více Ca.2+ do buňka, toto uvolňování vápníku se nazývá a vápenatá jiskra. To znamená, že počáteční tok Ca2+ do buňka, způsobil větší vydání Ca.2+ v rámci buňka, proto se proces nazývá uvolňování vápníku indukované vápníkem (CICR).[8]
Svalová kontrakce
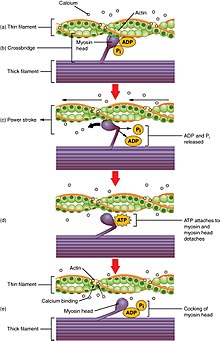
Zvýšení Ca2+, produkovaný CICR, nyní dělá dvě věci. Nejprve se váže na intracelulární stranu DHPR, signalizuje uzavření kanálů a brání dalšímu přílivu Ca2+ do cely. Zadruhé Ca2+ nepřímo aktivuje bílkoviny, volala myofilamenty, což má za následek svalová kontrakce. Dvě hlavní myofilamenta v srdeční (a kosterní ) sval jsou aktin a myosin. Ca.2+ váže se na protein zvaný troponin, který je vázán na aktinové vlákno. Tato vazba způsobí změnu tvaru troponinu, která vystavuje oblasti na aktin, ke kterému vedoucí myosin vlákno se váže. Vazba myosinová hlava na aktin je známý jako křížový most. A molekula, volala adenosintrifosfát (ATP) který je produkován intracelulární strukturou zvanou a mitochondrie, se poté používá jako zdroj energie, aby pomohl pohnout myosinovou hlavou nesoucí aktin. Výsledkem je, že aktin klouže po myosinovém vláknu a zkracuje sval. Tomu se říká energetický zdvih. Myosin pak se oddělí od aktin a resetuje se zpět do své původní polohy a naváže se na další část souboru aktin a vytvoření dalšího silového zdvihu, zkrácení sval dále. Tento proces pokračuje a hlava myosinu se pohybuje podobným pohybem jako veslo veslující na lodi, dokud Ca.2+ úroveň v buňce klesá (viz obrázek 1).[9]
Ukončení kontrakce
Kontrakce končí, když Ca2+ je odstraněn z buňky. Když k tomu dojde, troponin se změní zpět do původního tvaru a zablokuje vazebná místa aktin a zabránění vzniku křížových mostů. Tento pokles Ca.2+ v rámci buňka je vyvolána řadou bílkoviny kolektivně známé jako iontové transportéry. Mezi hlavní zapojená čerpadla patří: sarkoplazmatické retikulum Ca2+-ATPase, který pumpuje Ca.2+ zpět do SR, Sarcolemmal výměník sodíku a vápníku, který jeden pumpuje Ca.2+ z buňky výměnou za 3 ionty sodíku čerpané do buňky, Sarcolemmal Ca2+-ATPase, který k čerpání používá ATP Ca.2+ přímo z buňky a Mitochondriální Ca2+ Uniport systém, který pumpuje Ca.2+ do mitochondrií.[10]
Tepová frekvence
Tepová frekvence je ovlivněn nervy. Sympatické nervy, pocházející z mícha, zvýšit Tepová frekvence, zatímco parasympatické nervy (například vagové nervy ) pracovat na jeho snížení.
Sympatické nervy fungují uvolňováním proteinu (neurotransmiter ) volala noradrenalin který se váže na specifický receptor (beta 1 adrenoreceptor ) se nachází v sarcolemma a membrána t-tubulu z srdeční buňky. To aktivuje protein nazývaný G-protein a vede k řadě reakcí (známých jako a cyklická cesta AMP ) která vede k výrobě a molekula volala tábor (cyklický adenosinmonofosfát ). V SAN tábor váže se na iontový kanál podílí se na iniciaci akčního potenciálu a zrychluje výrobu akční potenciál (vidět sinoatriální uzel pro více podrobností). cAMP také aktivuje a protein volala protein kináza A (PKA ). PKA ovlivňuje jak DHPR a RyR, zvyšující vzestup Ca 2+ uvnitř kontraktilu buňky a proto se zvyšuje míra svalová kontrakce. PKA také ovlivňuje myofilamenty stejně jako a protein volala fosfolamban (PLB; viz sarkoplazmatické retikulum pro více informací), zrychlení rychlosti Ca.2+pokles v cele a tak se zrychluje svalová relaxace.[11]
Parasympatické nervy působí uvolněním neurotransmiteru nazývaného acetylcholin (ACh), který se váže na specifický receptor (M2 muskarinový receptor ) na sarkolemmu jak buněk SAN, tak komorových buněk. Tím se znovu aktivuje a G-protein. Tento G-protein však působí tak, že inhibuje dráhu cAMP, a proto brání sympatickému nervovému systému ve zvyšování srdeční frekvence. Kromě toho v SAN aktivuje G-protein specifický draslíkový kanál, který se staví proti iniciaci akčního potenciálu (viz SAN více podrobností), čímž zpomaluje srdeční frekvenci.[11]
Reference
- ^ Santana, L.F., Cheng, E.P. a Lederer, J.W. (2010) „Jak tvar srdečního akčního potenciálu řídí signalizaci a kontrakci vápníku v srdci?“, 49 (6).
- ^ Gordan, R., Gwathmey, J.K. a Xie, L.-H. (2015) „Autonomní a endokrinní kontrola kardiovaskulárních funkcí“, 7 (4).
- ^ Marks, A.R. (2003) „Vápník a srdce: otázka života a smrti“, 111 (5).
- ^ Wong, A.Y.K., Fabiato, A. a Bassingthwaigthe, J.B. (1992) „MODEL MECHANISMU UVOLŇOVÁNÍ VÁPNÍKU VÁPNĚ V CARDIACU“, 54 (1).
- ^ MONFREDI, O., DOBRZYNSKI, H., MONDAL, T., BOYETT, M.R. a MORRIS, G.M. (2010) „Anatomie a fyziologie současného přehledu Sinoatrial Node-A“, Pacing and Clinical Electrophysiology, 33 (11), str. 1392–1406. doi: 10.1111 / j.1540-8159.2010.02838.x.
- ^ Kurtenbach, S. a Zoidl, G. (2014) „Modulace mezery spojem a její důsledky pro funkci srdce“, 5.
- ^ Hong, T., Shaw, R.M., Institute, C.-S.H., Center, C.-S.M., Angeles, L., Kalifornie a Angeles, C.L. (2017) „Cardiac T-Tubule Microanatomy and function“, Recenze, 97 (1), s. 227–252. doi: 10.1152 / physrev.00037.2015.
- ^ Hinch, R., Greenstein, J.L., Tanskanen, A.J., Xu, L. a Winslow, R.L. (2004) „Zjednodušený lokální kontrolní model uvolňování vápníku indukovaného vápníkem v srdečních komorových myocytech“, 87 (6).
- ^ Lodish, H., Berk, A., Zipursky, L.S., Matsudaira, P., Baltimore, D. a Darnell, J. (2000a) Muscle: Specialized Contractile machine. Dostupné v: https://www.ncbi.nlm.nih.gov/books/NBK21670/ (Přístup: 13. února 2017).
- ^ Balke, C.W., Egan, T.M. a Wier, W.G. (1994) „Procesy, které odstraňují vápník z cytoplazmy během vazby excitace a kontrakce v intaktních buňkách srdce krysy“, 474 (3).
- ^ A b Gordan, R., Gwathmey, J.K. a Xie, L.-H. (2015b) „Autonomní a endokrinní kontrola srdečně-cévních funkcí“, 7 (4).
