Wolfyt (VI) oxytetrachlorid - Tungsten(VI) oxytetrachloride
 | |
 | |
| Jména | |
|---|---|
| Ostatní jména Oxid chlorid wolframový | |
| Identifikátory | |
3D model (JSmol ) | |
| Informační karta ECHA | 100.033.497 |
PubChem CID | |
| |
| |
| Vlastnosti | |
| WOCl4 | |
| Molární hmotnost | 341,651 g / mol |
| Vzhled | červené krystaly |
| Hustota | 11,92 g / cm3 |
| Bod tání | 211 ° C (412 ° F; 484 K) |
| Bod varu | 227,55 ° C (441,59 ° F; 500,70 K) |
| reaguje | |
| Rozpustnost | rozpustný v benzen a CS2 |
| Nebezpečí | |
Klasifikace EU (DSD) (zastaralý) | nezapsáno |
| Související sloučeniny | |
jiný anionty | Wolfyt (VI) oxytetrafluorid Wolfyt (VI) oxytetrabromid |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
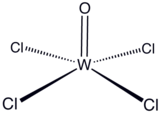
Wolfyt (VI) oxytetrachlorid je anorganická sloučenina s vzorec ŽÓCl4. Tato diamagnetická pevná látka se používá k přípravě dalších komplexy wolframu. Žlutozelená sloučenina je rozpustná v nepolárních rozpouštědlech, ale reaguje s alkoholy a vodou a tvoří se adukty s Lewisovými základnami.
Struktura
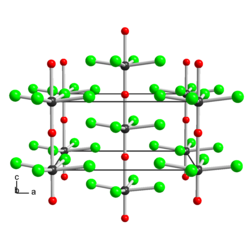
Struktura pevných WOCl4, ilustrující jeho polymerní strukturu s krátkým W≡O a slabé vazby W --- O v řetězcích. Barevný kód: O = červená.
Tato pevná látka sestává ze slabě přidružených čtvercových pyramidových monomerů.[1] Sloučenina je klasifikována jako oxyhalogenid.
Syntéza a reakce
WOCl4 je připraven z oxid wolframový:[2]
WOCl4 je Lewis kyselý. Je předchůdcem katalyzátorů používaných k polymeraci alkyny.[3]
Reference
- ^ Hess, H .; Hartung, H. (1966). „Die Kristallstruktur von Wolframoxidchlorid WOCl4 und Wolframoxidbromid WOBr4". Z. Anorg. Allg. Chem. 34 (3–4): 157–166. doi:10.1002 / zaac.19663440306.
- ^ Nielson, A. J. (1985). „Oxidy wolframu a chloridu molybdenu“. Anorganické syntézy. Inorg. Synth. Anorganické syntézy. 23. str. 195–198. doi:10.1002 / 9780470132548.ch41. ISBN 9780470132548.
- ^ Hayano, S .; Masuda, T. (1999). „Živá polymerace [o- (trifluormethyl) fenyl] acetylenu pomocí WOCl4- Katalyzátory na bázi, jako je WOCl4-n-Bu4Sn-t-BuOH (1: 1: 1) ". Makromolekuly. 32: 7344–7348. doi:10.1002 / zaac.19663440306.
| Tento anorganické sloučenina –Vztahující se článek je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
