DUT (gen) - DUT (gene)
DUTP pyrofosfatáza, také známý jako DUT, je enzym který je u lidí kódován DUT gen na chromozomu 15.[4]
Tento gen kóduje esenciální enzym o nukleotid metabolismus. Kódovaný protein tvoří všudypřítomný, homotrimerní enzym, který hydrolyzuje DUTP na skládka a pyrofosfát. Tato reakce slouží dvěma buněčným účelům: poskytnutí prekurzoru (dUMP) pro syntézu tymin nukleotidy potřebné pro replikace DNA a omezení intracelulárních zásob dUTP. Zvýšené hladiny dUTP vedou ke zvýšenému začlenění uracil do DNA, která indukuje rozsáhlé oprava excize zprostředkovaný uracil glykosyláza. Tento opravný proces, jehož výsledkem je odstranění a opětovné začlenění dUTP, je sebezničující a vede k DNA fragmentace a buněčná smrt. Alternativní sestřih tohoto genu vede k odlišným izoformy že lokalizovat buď mitochondrie nebo jádro. Související pseudogen se nachází na 19. chromozomu.[4]
Struktura
U lidí tento gen kóduje homotrimerický enzym se dvěma izoformami charakterizovanými jejich odlišnými subcelulární lokalizace: jaderná izoforma (DUT-N) a mitochondriální izoforma (DUT-M).[5][6][7]
Gen
Northern blot analýza odhaluje odlišné mRNA přepisy pro DUT-N (1,1 kb) a DUT-M (1,4 kb).[6] Izoformy se vyrábějí z alternativního sestřihu na různých 5 ' exony, přičemž první exon DUT-N se vyskytuje 767 základní páry pod prvním exonem v DUT-M.[6][7] Regulace na jiném promotéři bylo navrženo pro zohlednění rozdílné exprese těchto izoforem.[6]
Protein
Zralé formy DUT-N (22 kDa) a DUT-M (23 kDa) jsou téměř identické, kromě krátké N-terminál region přítomný v DUT-M. Prekurzor DUT-M (31 kDa) obsahuje arginin bohatý, 69-zbytek sekvence mitochondriálního cílení který prochází posttranslační štěpení k provedení mitochondriálního importu.[5][6][7] Mezitím monopartita Sekvence NLS je rozhodující pro funkci a jadernou lokalizaci DUT-N, která by se jinak hromadila v cytoplazma.[5][7] Ačkoli obě izoformy obsahují NLS, sekvence v DUT-M je izolována od příbuzného karyofheriny.[5] The izoelektrické body DUT-N (6,0) a DUT-M (8,1) odpovídají pH příslušných subcelulárních kompartmentů.[6]
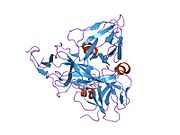
DUT je homotrimer se třemi aktivní stránky tvořený každou ze svých tří podjednotek.[7] Typicky každá podjednotka tvoří osmivláknovou hlaveň, která se vyměňuje C-terminál β-řetězce s ostatními podjednotkami sestavit do struktury trimeru. Kromě záměny β-řetězců tyto podjednotky interagují prostřednictvím rozšířených bimolekulárních rozhraní a trojnásobného centrálního kanálu.[8]Jako člen dUTPase rodina, DUT vyžaduje přítomnost a dvojmocný ion kovu jako Mg2 + pro jejich enzymatickou funkci.[9] DUT-N také obsahuje shodu cyklin-dependentní kináza fosforylační místo, které je fosforylováno na serin jako součást regulace buněčného cyklu.[6]
Funkce
DUT je členem rodiny dUTPase, která je známá pro katalyzování pyrofosforalýza z DUTP na dUMP a anorganické pyrofosfát. Tato funkce přispívá k replikace DNA a opravit přes de novo thymidylát biosyntéza, jako je produkt dUMP methylovaný podle thymidylát syntáza (TS) za vzniku dTMP, což je pak fosforylovaný na dTTP.[5][6][7][10] DUT je také zásadní pro udržení genom integritu snížením úrovně buněčného dUTP, čímž zabrání opakovaným cyklům uracil nesprávné začlenění do DNA a DNA opravit -zprostředkovaná přetržení vlákna, která by vedla k buněčná smrt.[5][6][7][9][10]
Kromě různých lokalizací tyto dvě izoformy DUT zobrazují různé vzorce vyjádření: zatímco DUT-M je konstitutivně vyjádřen, DUT-N je pod buněčný cyklus kontrolu a zejména zvýšenou regulaci během S fáze.[5][6] Tyto vzorce exprese odpovídají jejich rolím v cyklu replikace DNA jejich příslušných genomy, a tím naznačují různé regulační mechanismy ovlivňující každou izoformu.[6]
Mechanismus
Cyklus hydrolýzy dUTP lze popsat v následujících čtyřech enzymatických krocích: (i) rychlá vazba substrátu, (ii) izomerizace enzymuPodklad komplex do katalyticky kompetentní konformace, (iii) hydrolýza substrátu a (iv) rychlé, neřízené uvolňování produktů.[11]
Klinický význam
Protože mnoho chemoterapeutické agenti jako 5-fluorouracil zacházet neoplastická onemocnění, počítaje v to rakovina hlavy a krku, rakovina prsu, a rakovina trávicího traktu zaměřením na TS v metabolismu thymidylátu může DUT chránit před cytotoxický vedlejší účinky působením proti akumulaci dUTP.[6][7][10][12][13] Zároveň byly vysoké hladiny DUT-N spojeny s chemorezistencí a rychlejší progresí nádoru, a proto by mohly sloužit také jako prognostický popisovač pro celkové přežití a reakci na chemoterapii.[6][7][10][11][12] Podobně je DUT významně nadměrně exprimován hepatocelulární karcinom a může sloužit jako prognostický marker pro rakovinu.[14] Je pozoruhodné, že exprese DUT je regulována tumor supresorovým genem p53 aby se podpořila apoptóza nádorových buněk.
Interakce
DUT interaguje s dUTP, aby katalyzoval jeho hydrolýzu na dUMP a pyrofosfát.[4] E2F a Sp1 zvýšit expresi DUT vazbou jeho promotoru, zatímco p53 inhibuje transkripci DUT vazbou svého promotoru. Předpokládané NF-kB vazebné místo bylo také identifikováno v promotoru DUT.[13]
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000128951 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ A b C „Entrez Gene: DUT dUTP pyrophosphatase“.
- ^ A b C d E F G Róna G, Marfori M, Borsos M, Scheer I, Takács E, Tóth J, Babos F, Magyar A, Erdei A, Bozóky Z, Buday L, Kobe B, Vértessy BG (prosinec 2013). „Fosforylace sousedící se signálem o lokalizaci jádra lidské dUTPázy ruší dovoz jaderné energie: strukturální a mechanické pohledy“ (PDF). Acta Crystallographica oddíl D. 69 (Pt 12): 2495–505. doi:10.1107 / S0907444913023354. PMID 24311590.
- ^ A b C d E F G h i j k l m Ladner RD, Caradonna SJ (červenec 1997). "Lidský gen dUTPázy kóduje jaderné i mitochondriální izoformy. Diferenciální exprese izoforem a charakterizace cDNA kódující mitochondriální druhy". The Journal of Biological Chemistry. 272 (30): 19072–80. doi:10.1074 / jbc.272.30.19072. PMID 9228092.
- ^ A b C d E F G h i j Tinkelenberg BA, Fazzone W, Lynch FJ, Ladner RD (červenec 2003). "Identifikace sekvenčních determinantů lokalizace izoformy lidské nukleární dUTPázy". Experimentální výzkum buněk. 287 (1): 39–46. doi:10.1016 / s0014-4827 (03) 00048-x. PMID 12799180.
- ^ Takács E, Barabás O, Petoukhov MV, Svergun DI, Vértessy BG (březen 2009). "Molekulární tvar a prominentní role výměny beta-řetězců v organizaci dUTPázových oligomerů". FEBS Dopisy. 583 (5): 865–71. doi:10.1016 / j.febslet.2009.02.011. PMID 19302784.
- ^ A b Persson R, Cedergren-Zeppezauer ES, Wilson KS (prosinec 2001). "Homotrimerické dUTPázy; strukturní řešení pro specifické rozpoznávání a hydrolýzu dUTP". Současná věda o proteinech a peptidech. 2 (4): 287–300. doi:10.2174/1389203013381035. PMID 12369926.
- ^ A b C d Ladner RD (prosinec 2001). „Role dUTPázy a opravy uracil-DNA v chemoterapii rakoviny“. Současná věda o proteinech a peptidech. 2 (4): 361–70. doi:10.2174/1389203013380991. PMID 12374095.
- ^ A b Tóth J, Varga B, Kovács M, Málnási-Csizmadia A, Vértessy BG (listopad 2007). „Kinetický mechanismus lidské dUTPázy, esenciálního nukleotidového pyrofosfatázového enzymu“. The Journal of Biological Chemistry. 282 (46): 33572–82. doi:10,1074 / jbc.M706230200. PMID 17848562.
- ^ A b Ladner RD, Lynch FJ, Groshen S, Xiong YP, Sherrod A, Caradonna SJ, Stoehlmacher J, Lenz HJ (červenec 2000). „Exprese izoformy nukleotidohydrolázy dUTP v normálních a neoplastických tkáních: souvislost s přežitím a odpovědí na 5-fluorouracil u kolorektálního karcinomu“. Výzkum rakoviny. 60 (13): 3493–503. PMID 10910061.
- ^ A b Wilson PM, Fazzone W, LaBonte MJ, Lenz HJ, Ladner RD (leden 2009). „Regulace exprese genu lidské dUTPázy a transkripční represe zprostředkované p53 v reakci na poškození DNA vyvolané oxaliplatinou“. Výzkum nukleových kyselin. 37 (1): 78–95. doi:10.1093 / nar / gkn910. PMC 2615606. PMID 19015155.
- ^ Takatori H, Yamashita T, Honda M, Nishino R, Arai K, Yamashita T, Takamura H, Ohta T, Zen Y, Kaneko S (březen 2010). „Exprese dUTP pyrofosfatázy koreluje se špatnou prognózou hepatocelulárního karcinomu“. Liver International. 30 (3): 438–46. doi:10.1111 / j.1478-3231.2009.02177.x. PMID 19968781.
Další čtení
- Persson R, Cedergren-Zeppezauer ES, Wilson KS (prosinec 2001). "Homotrimerické dUTPázy; strukturní řešení pro specifické rozpoznávání a hydrolýzu dUTP". Současná věda o proteinech a peptidech. 2 (4): 287–300. doi:10.2174/1389203013381035. PMID 12369926.
- Ladner RD (prosinec 2001). „Role dUTPázy a opravy uracil-DNA v chemoterapii rakoviny“. Současná věda o proteinech a peptidech. 2 (4): 361–70. doi:10.2174/1389203013380991. PMID 12374095.
- McIntosh EM, Ager DD, Gadsden MH, Haynes RH (září 1992). „Lidská dUTP pyrofosfatáza: sekvence cDNA a potenciální biologický význam enzymu“. Sborník Národní akademie věd Spojených států amerických. 89 (17): 8020–4. doi:10.1073 / pnas.89.17.8020. PMC 49847. PMID 1325640.
- Strahler JR, Zhu XX, Hora N, Wang YK, Andrews PC, Roseman NA, Neel JV, Turka L, Hanash SM (červen 1993). "Fáze dozrávání a proliferace závislá exprese dUTPázy v lidských T buňkách". Sborník Národní akademie věd Spojených států amerických. 90 (11): 4991–5. doi:10.1073 / pnas.90.11.4991. PMC 46639. PMID 8389461.
- Ladner RD, McNulty DE, Carr SA, Roberts GD, Caradonna SJ (březen 1996). "Charakterizace odlišných jaderných a mitochondriálních forem lidské deoxyuridin trifosfátové nukleotidohydrolázy". The Journal of Biological Chemistry. 271 (13): 7745–51. doi:10.1074 / jbc.271.13.7745. PMID 8631816.
- Ladner RD, Carr SA, Huddleston MJ, McNulty DE, Caradonna SJ (březen 1996). „Identifikace konsensuálního místa fosforylace kinázy závislé na cyklinu, které je jedinečné pro jadernou formu lidské deoxyuridinkrifosfátové nukleotidohydrolázy“. The Journal of Biological Chemistry. 271 (13): 7752–7. doi:10.1074 / jbc.271.13.7752. PMID 8631817.
- Mol CD, Harris JM, McIntosh EM, Tainer JA (září 1996). „Lidská dUTP pyrofosfatáza: rozpoznávání uracilu vlásenkou beta a aktivní místa tvořená třemi samostatnými podjednotkami“. Struktura. 4 (9): 1077–92. doi:10.1016 / S0969-2126 (96) 00114-1. PMID 8805593.
- Chu R, Lin Y, Rao MS, Reddy JK (listopad 1996). „Klonování a identifikace krysí deoxyuridin trifosfatázy jako inhibitoru receptoru alfa aktivovaného proliferátorem peroxisomu“. The Journal of Biological Chemistry. 271 (44): 27670–6. doi:10.1074 / jbc.271.44.27670. PMID 8910358.
- Cohen D, Heng HH, Shi XM, McIntosh EM, Tsui LC, Pearlman RE (únor 1997). „Přiřazení lidského genu dUTPázy (DUT) k chromozomu 15q15-q21. 1 fluorescenční in situ hybridizací“. Genomika. 40 (1): 213–5. doi:10.1006 / geno.1996.4540. PMID 9070952.
- Ladner RD, Caradonna SJ (červenec 1997). "Lidský gen dUTPázy kóduje jaderné i mitochondriální izoformy. Diferenciální exprese izoforem a charakterizace cDNA kódující mitochondriální druhy". The Journal of Biological Chemistry. 272 (30): 19072–80. doi:10.1074 / jbc.272.30.19072. PMID 9228092.
- Ladner RD, Lynch FJ, Groshen S, Xiong YP, Sherrod A, Caradonna SJ, Stoehlmacher J, Lenz HJ (červenec 2000). „Exprese izoformy nukleotidohydrolázy dUTP v normálních a neoplastických tkáních: souvislost s přežitím a odpovědí na 5-fluorouracil u kolorektálního karcinomu“. Výzkum rakoviny. 60 (13): 3493–503. PMID 10910061.
- Fiser A, Vértessy BG (prosinec 2000). Msgstr "Změněná komunikace podjednotek v podrodinách trimerních dUTPáz". Sdělení o biochemickém a biofyzikálním výzkumu. 279 (2): 534–42. doi:10,1006 / bbrc.2000.3994. PMID 11118321.
- Pugacheva EN, Ivanov AV, Kravchenko JE, Kopnin BP, Levine AJ, Chumakov PM (červenec 2002). „Nový zisk funkční aktivity mutantů p53: aktivace exprese genu dUTPázy vedoucí k rezistenci na 5-fluorouracil“. Onkogen. 21 (30): 4595–600. doi:10.1038 / sj.onc.1205704. PMID 12096336.
- Tinkelenberg BA, Fazzone W, Lynch FJ, Ladner RD (červenec 2003). "Identifikace sekvenčních determinantů lokalizace izoformy lidské nukleární dUTPázy". Experimentální výzkum buněk. 287 (1): 39–46. doi:10.1016 / S0014-4827 (03) 00048-X. PMID 12799180.
- Studebaker AW, Lafuse WP, Kloesel R, Williams MV (únor 2005). "Modulace lidské dUTPázy pomocí malé interferující RNA". Sdělení o biochemickém a biofyzikálním výzkumu. 327 (1): 306–10. doi:10.1016 / j.bbrc.2004.12.021. PMID 15629463.
Tento článek včlení text z United States National Library of Medicine, který je v veřejná doména.