Dřeňová tuková tkáň - Marrow adipose tissue
| Dřeňová tuková tkáň | |
|---|---|
 | |
| Anatomická terminologie |
Dřeňová tuková tkáň (MAT), také známý jako tuková tkáň kostní dřeně (BMAT), je typem tukový vklad v kostní dřeň. Zvyšuje se ve stavech nízké kostní hustoty -osteoporóza,[1][2] mentální anorexie / kalorické omezení,[3][4] kosterní nevážení jako je ta, která se vyskytuje v vesmírné cestování,[5][6] proti-cukrovka terapie.[7]
Původ
Dřeň adipocyty původem z mezenchymální kmenová buňka (MSC) předci které také vedou k osteoblasty, mimo jiné typy buněk.[8] Předpokládá se tedy, že MAT je výsledkem preferenčního MSC diferenciace na adipocyt, spíše než osteoblast, linie v prostředí osteoporózy.[9] Vzhledem k tomu, MAT se zvyšuje v nastavení obezity[10][11][12] a je potlačena vytrvalostním cvičením,[13][10][14][15] nebo vibrace,[16] je pravděpodobné, že se fyziologie MAT v nastavení mechanického vstupu / cvičení blíží fyziologii MAT bílá tuková tkáň (WAT).
Regulace cvičení tukové tkáně dřeně
První studie demonstrující regulaci cvičení MAT v roce 2006 hlodavci byla zveřejněna v roce 2014;[10] Nyní byla u člověka potvrzena regulace cvičení MAT[17] přidávání klinického významu. Několik studií prokázalo snížení zátěže MAT, ke kterému dochází spolu se zvýšením množství kostí [15][13][14][18]. Jelikož cvičení zvyšuje množství kostí, snižuje MAT a zvyšuje expresi markerů oxidace mastných kyselin v kosti, předpokládá se, že MAT poskytuje potřebné palivo pro cvičení vyvolané tvorba kostí nebo anabolismus[14]. Jedna významná výjimka nastává v nastavení kalorických omezení: potlačení cvičení MAT nepřináší zvýšení tvorby kostí a dokonce se zdá, že způsobuje úbytek kostní hmoty[4][19][18]. Vskutku, energie dostupnost se jeví jako faktor ve schopnosti cvičení regulovat MAT.
Vztahy k jiným druhům tuku
MAT má vlastnosti obou bílý a hnědý Tlustý.[20] Podkožní bílý tuk obsahují přebytečnou energii, což naznačuje jasnou evoluční výhodu v době nedostatku. WAT je také zdrojem adipokiny a zánětlivé markery, které mají pozitivní (např. adiponektin )[21] a negativní[22] účinky na metabolické a kardiovaskulární koncové body. Viscerální břišní tuk (DPH) je zřetelný typ WAT, který je „úměrně spojen s negativní metabolickou a kardiovaskulární morbiditou“,[23] regeneruje kortizol,[24] a nedávno byla spojena se sníženou tvorbou kostí[25][26] Oba typy WAT se podstatně liší od hnědá tuková tkáň (BAT) jako skupina proteinů, které pomáhají BAT termogenní role.[27] MAT, podle jeho „konkrétního dřeň umístění a alespoň jeho původ z adipocytů LepR + MSC kostní dřeně je odděleno od ukládání nekostního tuku větší expresí faktorů transkripce kostí ",[28] a pravděpodobně označuje jiný fenotyp tuku.[29] Nedávno bylo zaznamenáno, že MAT „produkuje větší podíl adiponektin - adipokin spojený se zlepšeným metabolismem - než WAT ",[30] což naznačuje endokrinní funkci pro tento sklad, podobný, ale odlišný od toho z WAT.
Dopad na zdraví kostí
MAT se zvyšuje ve stavech křehkosti kostí. Předpokládá se, že MAT je výsledkem preferenční diferenciace MSC na adipocyt, spíše než v linii osteoblastů osteoporóza[31][18] na základě inverzního vztahu mezi kostí a MAT v kostech křehkých osteoporotických stavech. Zvýšení MAT je zaznamenáno v klinických studiích s osteoporózou měřených pomocí MR spektroskopie.[32][33][34] Estrogen terapie v postmenopauzální osteoporóza snižuje MAT.[35] Antiresorpční terapie jako risedronát nebo zoledronát také snížit MAT při zvýšení hustoty kostí, což podporuje inverzní vztah mezi množstvím kosti a MAT. Během stárnutí klesá množství kostí[36][37] a tuk se redistribuuje z podkožního do mimoděložní weby jako kostní dřeň, svalů a jater.[38] Stárnutí je spojena s nižším osteogenním a větším adipogenním předpětím MSC.[39] Toto předpětí MSC související se stárnutím od linie osteoblastů může představovat vyšší bazální PPARy výraz[40] nebo snížil Wnt10b.[41][42][43] Křehkost kostí, osteoporóza a osteoporotické zlomeniny se tedy považují za spojené s mechanismy, které podporují akumulaci MAT.
- Histologické řezy demonstrující kostní adipocyty
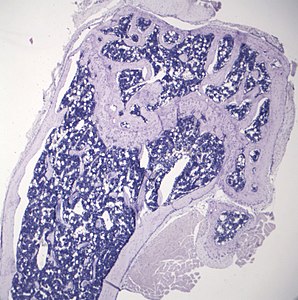
Reprezentativní histologický řez distálního femuru 16týdenní zdravé myši C57BL / 6, který prokazuje typické množství adipocytů dřeně.

Reprezentativní histologický řez distálního femuru 16týdenní myši C57BL / 6 po 6 týdnech kalorického omezení, což prokazuje zvýšené množství adipocytů dřeně.
Údržba hematopoetických kmenových buněk
Adipocyty kostní dřeně vylučují faktory, které podporují obnovu HSC ve většině kostí.[44]
Hematopoetické buňky (také známé jako krvinky) sídlí v kostní dřeni spolu s adipocyty dřeně. Tyto hematopoetické buňky pocházejí z hematopoetické kmenové buňky (HSC), které dávají vzniknout různým buňkám: buňkám krve, imunitnímu systému a buňkám, které štěpí kost (osteoklasty ). K obnově HSC dochází v kostní dřeni výklenek kmenových buněk, mikroprostředí, které obsahuje buňky a vylučované faktory, které podporují vhodnou obnovu a diferenciaci HSC. Studie výklenek kmenových buněk je relevantní pro obor onkologie za účelem zlepšení terapie pro více pacientů hematologické rakoviny. Rakoviny jsou proto často léčeny transplantace kostní dřeně existuje zájem na zlepšení obnovy HSC.
Měření
Abychom pochopili fyziologii MAT, byly použity různé analytické metody. Adipocyty dřeně je obtížné izolovat a kvantifikovat, protože jsou rozptýleny kostními a krvetvorné elementy. Až do nedávné doby se kvalitativní měření MAT spoléhaly na kosti histologie,[45][46] který je předmětem webu zkreslení výběru a nedokáže adekvátně kvantifikovat objem tuku v dřeni. Histologické techniky a fixace nicméně umožňují vizualizaci MAT, kvantifikaci velikosti adipocytů a asociaci MAT s okolním prostředím endosteum, prostředí buněk a vylučované faktory.[47][48][49]
Nedávné pokroky v identifikaci buněčného povrchu a intracelulárního markeru a analýzy jednotlivých buněk vedly k většímu rozlišení a vysoké propustnosti ex-vivo kvantifikace. Průtoková cytometrická kvantifikace může být použita k čištění adipocytů ze stromální vaskulární frakce většiny tukových zásob.[50] Dřívější výzkum s takovým strojním zařízením citoval adipocyty jako příliš velké a křehké na čištění založené na cytometrech, což je činí náchylnými k lýze; v poslední době však došlo ke zlepšení;[51] tato metodika nicméně nadále představuje technické výzvy[52] a je pro většinu výzkumné komunity nepřístupný.
Pro zlepšení kvantifikace MAT, nové zobrazování byly vyvinuty techniky jako prostředek k vizualizaci a kvantifikaci MAT. Ačkoli protonová magnetická rezonanční spektroskopie (1H-MRS) byl úspěšně použit ke kvantifikaci vertebrálního MAT u lidí,[53] je obtížné jej použít u laboratorních zvířat.[54] Zobrazování magnetickou rezonancí (MRI) poskytuje hodnocení MAT v páteřní kostra[55] ve spojení s μCT - měření hustoty kostní dřeně.[56] Nedávno byla vyvinuta volumetrická metoda pro identifikaci, kvantifikaci a lokalizaci MAT v kosti hlodavců osmium barvení kostí a μCT zobrazování,[57] následovaný pokročilými analýza obrazu objemu lipidů vázaných na osmium (v mm3) vzhledem k objemu kostí.[10][14][13] Tato technika poskytuje reprodukovatelnou kvantifikaci a vizualizaci MAT, což umožňuje schopnost důsledně kvantifikovat změny v MAT s dietou, cvičením a agenty, které omezují alokaci linie prekurzoru. Ačkoli je metoda osmium kvantitativně přesná, osmium je toxické a nelze jej porovnávat napříč dávkovými experimenty. Nedávno vědci vyvinuli a ověřili[14] technika 9.4T MRI skeneru, která umožňuje lokalizaci a objemovou (3D) kvantifikaci, kterou lze porovnat napříč experimenty, jako v [4].
- Metody pro kvantifikaci tkáně kostní dřeně (MAT)

Postava. Tento obrázek ukazuje použití metody osmium-μCT s pokročilým zpracováním obrazu pro kvantifikaci MAT. Na tomto obrázku je ukázáno, že běžecké cvičení potlačuje MAT navzdory agonistovi PPARγ. Osmium vazače tuků je zobrazeno pomocí μCT (A) v n = 5 na obrázky překryté skupinou. Je uvedena kvantifikace osmium jako objem MAT / kosti v celé femuru. a, významné kvůli Rosi. b, významné kvůli cvičení. Rosi = rosiglizaone, CTL = kontrola, E = cvičení.
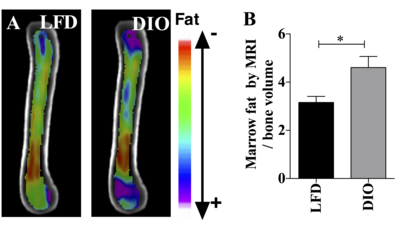
Postava. To ukazuje použití zobrazování MRI (skener 9,4T) spolu s pokročilým zpracováním obrazu pro kvantifikaci MAT. Obrázky a graf ukazují, že MAT je vyšší u obézních ve srovnání s hubenými myšmi. Myši B6 byly krmeny HFD od věku 4 týdnů do věku 16 týdnů. MAT byl kvantifikován pomocí MRI. A) n = 10 průměrných obrázků superponovaných skupin je zobrazeno B) MAT normalizovaný na objem kosti v každé skupině.
Reference
![]() Tento článek zahrnuje text Gabriel M. Pagnotti a Maya Styner k dispozici pod CC BY 4.0 licence.
Tento článek zahrnuje text Gabriel M. Pagnotti a Maya Styner k dispozici pod CC BY 4.0 licence.
- ^ Cohen A, Dempster DW, Stein EM, Nickolas TL, Zhou H, McMahon DJ a kol. (Srpen 2012). „Zvýšená adipozita kostní dřeně u premenopauzálních žen s idiopatickou osteoporózou“. The Journal of Clinical Endocrinology and Metabolism. 97 (8): 2782–91. doi:10.1210 / jc.2012-1477. PMC 3410269. PMID 22701013.
- ^ Meunier P, Aaron J, Edouard C, Vignon G (říjen 1971). „Osteoporóza a nahrazení buněčných populací kostní dřeně tukovou tkání. Kvantitativní studie 84 biopsií kyčelních kostí“. Klinická ortopedie a související výzkum. 80: 147–54. doi:10.1097/00003086-197110000-00021. PMID 5133320.
- ^ Fazeli PK, Horowitz MC, MacDougald OA, Scheller EL, Rodeheffer MS, Rosen CJ, Klibanski A (březen 2013). "Dřeň, tuk a kost - nové perspektivy". The Journal of Clinical Endocrinology and Metabolism. 98 (3): 935–45. doi:10.1210 / jc.2012-3634. PMC 3590487. PMID 23393168.
- ^ A b C McGrath C, Sankaran JS, Misaghian-Xanthos N, Sen B, Xie Z, Styner MA a kol. (Leden 2020). „Cvičení degraduje kosti v kalorickém omezení, navzdory potlačení tkáně tukové tkáně dřeně (MAT)“. Journal of Bone and Mineral Research. 35 (1): 106–115. doi:10,1002 / jbmr.3872. PMC 6980282. PMID 31509274.
- ^ Ahdjoudj S, Lasmoles F, Holy X, Zerath E, Marie PJ (duben 2002). „Transformující růstový faktor beta2 inhibuje diferenciaci adipocytů vyvolanou uvolněním skeletu ve stromatu kostní dřeně krysy“. Journal of Bone and Mineral Research. 17 (4): 668–77. doi:10.1359 / jbmr.2002.17.4.668. PMID 11918224.
- ^ Wronski TJ, Morey ER (01.01.1982). "Abnormality skeletu u potkanů vyvolané simulovanou beztížností". Metabolická kostní nemoc a související výzkum. 4 (1): 69–75. doi:10.1016 / 0221-8747 (82) 90011-X. PMID 7121257.
- ^ Rubin MR, Manavalan JS, Agarwal S, McMahon DJ, Nino A, Fitzpatrick LA, Bilezikian JP (říjen 2014). „Účinky rosiglitazonu vs. metforminu na cirkulující osteoklasty a osteogenní prekurzorové buňky u postmenopauzálních žen s diabetes mellitus 2. typu“. The Journal of Clinical Endocrinology and Metabolism. 99 (10): E1933-42. doi:10.1210 / jc.2013-3666. PMID 24905061.
- ^ Muruganandan S, Roman AA, Sinal CJ (leden 2009). „Adipocytová diferenciace mezenchymálních kmenových buněk odvozených z kostní dřeně: vzájemná komunikace s osteoblastogenním programem“. Buněčné a molekulární biologické vědy. 66 (2): 236–53. doi:10.1007 / s00018-008-8429-z. PMID 18854943. S2CID 5558912.
- ^ Paccou J, Hardouin P, Cotten A, Penel G, Cortet B (říjen 2015). „Úloha tuku v kostní dřeni ve zdraví skeletu: užitečnost a perspektivy pro lékaře“. The Journal of Clinical Endocrinology and Metabolism. 100 (10): 3613–21. doi:10.1210 / jc.2015-2338. PMID 26244490.
- ^ A b C d Styner M, Thompson WR, Galior K, Uzer G, Wu X, Kadari S a kol. (Červenec 2014). „Akumulace kostní dřeně zrychlená stravou s vysokým obsahem tuku je potlačena cvičením“. Kost. 64: 39–46. doi:10.1016 / j.bone.2014.03.044. PMC 4041820. PMID 24709686.
- ^ Scheller EL, Khoury B, Moller KL, Wee NK, Khandaker S, Kozloff KM a kol. (2016). „Změny v kosterní integritě a tukovosti kostní dřeně během diety s vysokým obsahem tuku a po hubnutí“. Hranice v endokrinologii. 7: 102. doi:10.3389 / fendo.2016.00102. PMC 4961699. PMID 27512386.
- ^ Doucette CR, Horowitz MC, Berry R, MacDougald OA, Anunciado-Koza R, Koza RA, Rosen CJ (září 2015). „Dieta s vysokým obsahem tuku zvyšuje tukovou tkáň kostní dřeně (MAT), ale nemění trabekulární nebo kortikální kostní hmotu u myší C57BL / 6J“. Journal of Cellular Physiology. 230 (9): 2032–7. doi:10,1002 / jcp.24954. PMC 4580244. PMID 25663195.
- ^ A b C Styner M, Pagnotti GM, Galior K, Wu X, Thompson WR, Uzer G a kol. (Srpen 2015). "Cvičení regulace kostní dřeně v nastavení léčby agonisty PPARγ u samic myší C57BL / 6". Endokrinologie. 156 (8): 2753–61. doi:10.1210 / cs.2015-1213. PMC 4511140. PMID 26052898.
- ^ A b C d E Styner M, Pagnotti GM, McGrath C, Wu X, Sen B, Uzer G a kol. (Srpen 2017). "Cvičení snižuje tkáň kostní dřeně prostřednictvím ß-oxidace u obézních běžících myší". Journal of Bone and Mineral Research. 32 (8): 1692–1702. doi:10,1002 / jbmr.3159. PMC 5550355. PMID 28436105.
- ^ A b Pagnotti GM, Styner M, Uzer G, Patel VS, Wright LE, Ness KK a kol. (Červen 2019). „Boj proti osteoporóze a obezitě cvičením: využití buněčné mechanosenzitivity“. Recenze přírody. Endokrinologie. 15 (6): 339–355. doi:10.1038 / s41574-019-0170-1. PMC 6520125. PMID 30814687.
- ^ Luu YK, Pessin JE, Judex S, Rubin J, Rubin CT (duben 2009). „Mechanické signály jako neinvazivní prostředek k ovlivnění osudu mezenchymálních kmenových buněk, podporující kost a potlačující fenotyp tuku“. BoneKEy Osteovision. 6 (4): 132–149. doi:10.1138/20090371. PMC 3255555. PMID 22241295.
- ^ Belavy DL, Quittner MJ, Ridgers ND, Shiekh A, Rantalainen T, Trudel G (duben 2018). „Specifická modulace tkáně tukové tkáně obratle podle fyzické aktivity“. Journal of Bone and Mineral Research. 33 (4): 651–657. doi:10,1002 / jbmr.3357. PMID 29336053.
- ^ A b C Little-Letsinger, Sarah E .; Pagnotti, Gabriel M .; McGrath, Cody; Styner, Maya (2020-10-17). „Cvičení a dieta: Odhalení potenciálních mediátorů křehkosti kostí v tukové tkáni kostí a dřeně“. Aktuální zprávy o osteoporóze. doi:10.1007 / s11914-020-00634-r. ISSN 1544-1873.
- ^ Southmayd, Emily A; Williams, Nancy I; Mallinson, Rebecca J; De Souza, Mary Jane (2019-03-21). „Energetický nedostatek potlačuje kostní obrat při cvičení žen s poruchami menstruace“. The Journal of Clinical Endocrinology & Metabolism. 104 (8): 3131–3145. doi:10.1210 / jc.2019-00089. ISSN 0021-972X. PMID 30896746.
- ^ Krings A, Rahman S, Huang S, Lu Y, Czernik PJ, Lecka-Czernik B (únor 2012). „Tuk v kostní dřeni má vlastnosti hnědé tukové tkáně, které jsou oslabeny stárnutím a cukrovkou“. Kost. 50 (2): 546–52. doi:10.1016 / j.bone.2011.06.016. PMC 3214232. PMID 21723971.
- ^ Ye R, Scherer PE (duben 2013). „Adiponektin, řidič nebo spolujezdec na cestě k citlivosti na inzulín?“. Molekulární metabolismus. 2 (3): 133–41. doi:10.1016 / j.molmet.2013.04.001. PMC 3773837. PMID 24049728.
- ^ Tilg H, Moschen AR (říjen 2006). "Adipocytokiny: mediátory spojující tukovou tkáň, zánět a imunitu". Recenze přírody. Imunologie. 6 (10): 772–83. doi:10.1038 / nri1937. PMID 16998510. S2CID 29865593.
- ^ Wronska A, Kmiec Z (červen 2012). "Strukturální a biochemické charakteristiky různých skladů bílé tukové tkáně". Acta Physiologica. 205 (2): 194–208. doi:10.1111 / j.1748-1716.2012.02409.x. PMID 22226221.
- ^ Masuzaki H, Paterson J, Shinyama H, Morton NM, Mullins JJ, Seckl JR, Flier JS (prosinec 2001). "Transgenní model viscerální obezity a metabolického syndromu". Věda. 294 (5549): 2166–70. Bibcode:2001Sci ... 294,2166M. doi:10.1126 / science.1066285. PMID 11739957. S2CID 768303.
- ^ Bredella MA, Lin E, Gerweck AV, Landa MG, Thomas BJ, Torriani M a kol. (Listopad 2012). „Determinanty mikroarchitektury kostí a mechanické vlastnosti u obézních mužů“. The Journal of Clinical Endocrinology and Metabolism. 97 (11): 4115–22. doi:10.1210 / jc.2012-2246. PMC 3485587. PMID 22933540.
- ^ Cohen A, Dempster DW, Recker RR, Lappe JM, Zhou H, Zwahlen A a kol. (Červen 2013). „Břišní tuk je spojen s nižší tvorbou kostí a horší kvalitou kostí u zdravých premenopauzálních žen: studie biopsie transiliální kosti“. The Journal of Clinical Endocrinology and Metabolism. 98 (6): 2562–72. doi:10.1210 / jc.2013-1047. PMC 3667251. PMID 23515452.
- ^ Wu J, Cohen P, Spiegelman BM (únor 2013). „Adaptivní termogeneze v adipocytech: je béžová nová hnědá?“. Geny a vývoj. 27 (3): 234–50. doi:10.1101 / gad.211649.112. PMC 3576510. PMID 23388824.
- ^ Al-Nbaheen M, Vishnubalaji R, Ali D, Bouslimi A, Al-Jassir F, Megges M a kol. (Únor 2013). „Lidské stromální (mezenchymální) kmenové buňky z kostní dřeně, tukové tkáně a kůže vykazují rozdíly v molekulárním fenotypu a diferenciačním potenciálu“. Recenze a zprávy o kmenových buňkách. 9 (1): 32–43. doi:10.1007 / s12015-012-9365-8. PMC 3563956. PMID 22529014.
- ^ Gimble JM, Zvonic S, Floyd ZE, Kassem M, Nuttall ME (květen 2006). "Hra s kostmi a tuky". Journal of Cellular Biochemistry. 98 (2): 251–66. doi:10.1002 / jcb.20777. PMID 16479589.
- ^ Cawthorn WP, Scheller EL, Learman BS, Parlee SD, Simon BR, Mori H a kol. (Srpen 2014). „Tuková tkáň kostní dřeně je endokrinní orgán, který přispívá ke zvýšení cirkulujícího adiponektinu během kalorického omezení“. Buněčný metabolismus. 20 (2): 368–375. doi:10.1016 / j.cmet.2014.06.003. PMC 4126847. PMID 24998914.
- ^ Paccou J, Hardouin P, Cotten A, Penel G, Cortet B (říjen 2015). „Úloha tuku v kostní dřeni ve zdraví skeletu: užitečnost a perspektivy pro lékaře“. The Journal of Clinical Endocrinology and Metabolism. 100 (10): 3613–21. doi:10.1210 / jc.2015-2338. PMID 26244490.
- ^ Duque G, Li W, Adams M, Xu S, Phipps R (květen 2011). "Účinky risedronátu na adipocyty kostní dřeně u postmenopauzálních žen". Osteoporóza mezinárodní. 22 (5): 1547–53. doi:10.1007 / s00198-010-1353-8. PMID 20661545. S2CID 27850362.
- ^ Yeung DK, Griffith JF, Antonio GE, Lee FK, Woo J, Leung PC (srpen 2005). „Osteoporóza je spojena se zvýšeným obsahem tuku v dřeni a sníženým nenasycením tuku v dřeni: studie protonové MR spektroskopie“. Journal of Magnetic Resonance Imaging. 22 (2): 279–85. doi:10.1002 / jmri.20367. PMID 16028245.
- ^ Li X, Kuo D, Schafer AL, Porzig A, Link TM, Black D, Schwartz AV (duben 2011). „Kvantifikace obsahu tuku v vertebrální kostní dřeni pomocí 3 Tesla MR spektroskopie: reprodukovatelnost, variabilita obratlů a aplikace při osteoporóze“. Journal of Magnetic Resonance Imaging. 33 (4): 974–9. doi:10,1002 / jmri.22489. PMC 3072841. PMID 21448966.
- ^ Syed FA, Oursler MJ, Hefferanm TE, Peterson JM, Riggs BL, Khosla S (září 2008). "Účinky estrogenové terapie na adipocyty kostní dřeně u postmenopauzálních osteoporotických žen". Osteoporóza mezinárodní. 19 (9): 1323–30. doi:10.1007 / s00198-008-0574-6. PMC 2652842. PMID 18274695.
- ^ Khosla S, Riggs BL, Atkinson EJ, Oberg AL, McDaniel LJ, Holets M a kol. (Leden 2006). „Účinky pohlaví a věku na kostní mikrostrukturu v ultradistálním poloměru: populační neinvazivní hodnocení in vivo“. Journal of Bone and Mineral Research. 21 (1): 124–31. doi:10.1359 / jbmr.050916. PMC 1352156. PMID 16355281.
- ^ Glatt V, Canalis E, Stadmeyer L, Bouxsein ML (srpen 2007). „Změny trabekulární architektury související s věkem se liší u samic a samců myší C57BL / 6J“. Journal of Bone and Mineral Research. 22 (8): 1197–207. doi:10.1359 / jbmr.070507. PMID 17488199.
- ^ Tchkonia T, Morbeck DE, Von Zglinicki T, Van Deursen J, Lustgarten J, Scrable H a kol. (Říjen 2010). „Tuková tkáň, stárnutí a stárnutí buněk“. Stárnoucí buňka. 9 (5): 667–84. doi:10.1111 / j.1474-9726.2010.00608.x. PMC 2941545. PMID 20701600.
- ^ Kassem M, Marie PJ (duben 2011). „Vnitřní mechanismy dysfunkcí osteoblastů spojené se stárnutím“. Stárnoucí buňka. 10 (2): 191–7. doi:10.1111 / j.1474-9726.2011.00669.x. PMID 21210937.
- ^ Moerman EJ, Teng K, Lipschitz DA, Lecka-Czernik B (prosinec 2004). „Stárnutí aktivuje adipogenní a potlačuje osteogenní programy ve stromatu / kmenových buňkách mezenchymální dřeně: role transkripčního faktoru PPAR-gama2 a signálních drah TGF-beta / BMP“. Stárnoucí buňka. 3 (6): 379–89. doi:10.1111 / j.1474-9728.2004.00127.x. PMC 1850101. PMID 15569355.
- ^ Stevens JR, Miranda-Carboni GA, Singer MA, Brugger SM, Lyons KM, Lane TF (říjen 2010). „Nedostatek Wnt10b má za následek úbytek kostní hmoty závislý na věku a postupné snižování mezenchymálních progenitorových buněk“. Journal of Bone and Mineral Research. 25 (10): 2138–47. doi:10,1002 / jbmr.118. PMC 3153316. PMID 20499361.
- ^ Bennett CN, Ouyang H, Ma YL, Zeng Q, Gerin I, Sousa KM a kol. (Prosinec 2007). „Wnt10b zvyšuje postnatální tvorbu kostí zvýšením diferenciace osteoblastů“. Journal of Bone and Mineral Research. 22 (12): 1924–32. doi:10.1359 / jbmr.070810. PMID 17708715.
- ^ Chen Q, Shou P, Zheng C, Jiang M, Cao G, Yang Q a kol. (Červenec 2016). „Osudové rozhodnutí mezenchymálních kmenových buněk: adipocyty nebo osteoblasty?“. Buněčná smrt a diferenciace. 23 (7): 1128–39. doi:10.1038 / cdd.2015.168. PMC 4946886. PMID 26868907.
- ^ Zhou BO, Yu H, Yue R, Zhao Z, Rios JJ, Naveiras O, Morrison SJ (srpen 2017). „Adipocyty kostní dřeně podporují regeneraci kmenových buněk a hematopoézu vylučováním SCF“. Přírodní buněčná biologie. 19 (8): 891–903. doi:10.1038 / ncb3570. PMC 5536858. PMID 28714970.
- ^ Bielohuby M, Matsuura M, Herbach N, Kienzle E, Slawik M, Hoeflich A, Bidlingmaier M (únor 2010). „Krátkodobé vystavení nízkotučné stravě s vysokým obsahem tuků způsobuje nízkou kostní minerální hustotu a snižuje tvorbu kostí u potkanů.“ Journal of Bone and Mineral Research. 25 (2): 275–84. doi:10.1359 / jbmr.090813. PMID 19653818.
- ^ Spatz JM, Ellman R, Cloutier AM, Louis L, van Vliet M, Suva LJ a kol. (Duben 2013). „Protilátka proti sklerostinu inhibuje poškození skeletu v důsledku sníženého mechanického zatížení“. Journal of Bone and Mineral Research. 28 (4): 865–74. doi:10,1002 / jbmr.1807. PMC 4076162. PMID 23109229.
- ^ Rosen CJ, Ackert-Bicknell CL, Adamo ML, Shultz KL, Rubin J, Donahue LR a kol. (Listopad 2004). „Kongenní myši s nízkým sérovým IGF-I mají zvýšený tělesný tuk, sníženou minerální hustotu kostí a pozměněný program diferenciace osteoblastů“. Kost. 35 (5): 1046–58. doi:10.1016 / j.bone.2004.07.008. PMID 15542029.
- ^ Naveiras O, Nardi V, Wenzel PL, Hauschka PV, Fahey F, Daley GQ (červenec 2009). „Adipocyty kostní dřeně jako negativní regulátory hematopoetického mikroprostředí“. Příroda. 460 (7252): 259–63. Bibcode:2009Natur.460..259N. doi:10.1038 / nature08099. PMC 2831539. PMID 19516257.
- ^ David V, Martin A, Lafage-Proust MH, Malaval L, Peyroche S, Jones DB a kol. (Květen 2007). „Mechanické zatížení snižuje regulaci gama receptoru aktivovaného proliferátorem peroxisomu ve stromálních buňkách kostní dřeně a podporuje osteoblastogenezi na úkor adipogeneze“. Endokrinologie. 148 (5): 2553–62. doi:10.1210 / en.2006-1704. PMID 17317771.
- ^ Majka SM, Miller HL, Sullivan T, Erickson PF, Kong R, Weiser-Evans M a kol. (Říjen 2012). „Specifikace tukové linie myeloidních buněk odvozených z kostní dřeně“. Adipocyt. 1 (4): 215–229. doi:10,4161 / adip.21496. PMC 3609111. PMID 23700536.
- ^ Majka SM, Miller HL, Helm KM, Acosta AS, Childs CR, Kong R, Klemm DJ (2014). "Analýza a izolace adipocytů průtokovou cytometrií". Metody biologie tukové tkáně, část A. Metody v enzymologii. 537. str. 281–96. doi:10.1016 / b978-0-12-411619-1.00015-x. ISBN 9780124116191. PMC 4143162. PMID 24480352.
- ^ Bernstein RL, Hyun WC, Davis JH, Fulwyler MJ, Pershadsingh HA (červenec 1989). "Průtoková cytometrická analýza zralých adipocytů". Cytometrie. 10 (4): 469–74. doi:10,1002 / cyto.990100416. PMID 2766892.
- ^ Bredella MA, Torriani M, Ghomi RH, Thomas BJ, Brick DJ, Gerweck AV a kol. (Leden 2011). „Tuk v kostní dřeni je pozitivně spojen s viscerálním tukem a inverzně spojen s IGF-1 u obézních žen“. Obezita. 19 (1): 49–53. doi:10.1038 / oby.2010.106. PMC 3593350. PMID 20467419.
- ^ de Paula FJ, Dick-de-Paula I, Bornstein S, Rostama B, Le P, Lotinun S a kol. (Září 2011). „VDR haploinsufficiency ovlivňuje složení těla a získávání koster způsobem specifickým pro pohlaví“. Kalcifikovaná tkáňová mezinárodní. 89 (3): 179–91. doi:10.1007 / s00223-011-9505-1. PMC 3157554. PMID 21637996.
- ^ Fazeli PK, Bredella MA, Freedman L, Thomas BJ, Breggia A, Meenaghan E a kol. (Září 2012). "Hladiny tuku v kostní dřeni a preadipocytového faktoru 1 se snižují s obnovou u žen s mentální anorexií". Journal of Bone and Mineral Research. 27 (9): 1864–71. doi:10,1002 / jbmr.1640. PMC 3415584. PMID 22508185.
- ^ Rantalainen T, Nikander R, Heinonen A, Cervinka T, Sievänen H, Daly RM (květen 2013). „Diferenciální účinky cvičení na hustotu tibiální dřeně u mladých atletek“. The Journal of Clinical Endocrinology and Metabolism. 98 (5): 2037–44. doi:10.1210 / jc.2012-3748. PMID 23616150.
- ^ Scheller EL, Troiano N, Vanhoutan JN, Bouxsein MA, Fretz JA, Xi Y a kol. (2014). "Použití barvení oxidem osmičelým s mikropočítačovou tomografií k vizualizaci a kvantifikaci tukové tkáně kostní dřeně in vivo". Metody biologie tukové tkáně, část A. Metody v enzymologii. 537. str. 123–39. doi:10.1016 / b978-0-12-411619-1.00007-0. ISBN 9780124116191. PMC 4097010. PMID 24480344.
Další čtení
- „Tuková tkáň kostní dřeně vylučuje hormon, který pomáhá tělu zůstat zdravým“. Michiganská univerzita. 3. července 2014. Archivovány od originál dne 15. března 2015.
- „Další důvod pro cvičení: Spalování kostního tuku je klíčem k lepšímu zdraví kostí“. Věda denně. 18. května 2017.




