Cyklopropanon - Cyclopropanone
 | |
| Jména | |
|---|---|
| Název IUPAC cyklopropanon | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C3H4Ó | |
| Molární hmotnost | 56.06326 |
| Hustota | 0,867 g / ml při 25 ° C |
| Bod tání | −90 ° C (−130 ° F; 183 K) |
| Bod varu | 50 až 53 ° C (122 až 127 ° F; 323 až 326 K) při 22 mmHg |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
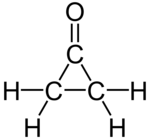
Cyklopropanon je organická sloučenina s molekulární vzorec (CH2)2CO sestávající z a cyklopropan uhlíkový rámec s a keton funkční skupina. Mateřská sloučenina je labilní a je vysoce citlivá i na slabé nukleofily. Mezi náhražky cyklopropanonu patří acetály.[1][2]
Příprava
Cyklopropanon byl připraven reakcí keten s diazomethan při -145 ° C.[3][4] Deriváty cyklopropanonu jsou zajímavé organická chemie.[5]
Deriváty
Cyklopropanony jsou meziprodukty v Favorskii přesmyk s cyklickými ketony kde karboxylová kyselina tvorba je doprovázena kontrakcí prstence.
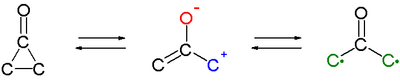
Cyklopropanony reagují jako 1,3-dipóly v cykloadice například s cyklickými dienes, jako je furan.[6][7] Oxyallylový meziprodukt nebo valenční tautomer (vytvořený štěpením vazby C2-C3) se navrhuje jako aktivní meziprodukt nebo dokonce a biradical struktura (ve srovnání se související trimethylenemethan ).
Experimentální důkazy nejsou přesvědčivé. Prostřednictvím tohoto meziproduktu probíhají další reakce cyklopropanonů. Například enantiopure (+)-trans-2,3-di-terc-butylcyklopropanon racemizuje při zahřátí na 80 ° C.[8]
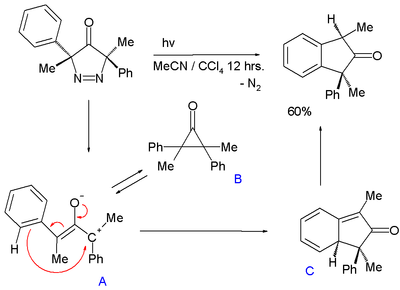
Oxyallylový meziprodukt je také navržen v fotochemické přeměna 3,5-dihydro-4H-pyrazol-4-onu s vyloučením dusíku na an indane:[9]
V této reakci oxyallylový meziprodukt A, v chemická rovnováha s cyklopropanonem B útočí na fenyl zvonit skrz jeho karbokace tvořící přechodný jev 1,3-cyklohexadien C (s UV stopou podobnou isotoluen ) následovanou rearomatizací. Energetický rozdíl mezi A a B je 5 až 7 kcal /mol (21 až 29 kJ / mol).
Viz také
- Jiné cyklické ketony: cyklobutanon, cyklopentanon, cyklohexanon
- Další deriváty cyklopropanu: cyklopropen, cyklopropenon
Reference
- ^ Salaün, J .; Margueritedoi = 10,15227 / orgsyn.063.0147, J. (1985). "Cyklopropanon Ethyl Hemiacetal z Ethyl 3-Chloropropanoate". Organické syntézy. 63: 147. doi:10.15227 / orgsyn.063.0147.
- ^ Datový list komerční dodavatel Odkaz
- ^ Turro, N.J .; Hammond, W.B. (1968). „Cyklopropanony - VIII“. Čtyřstěn. 24 (18): 6017–6028. doi:10.1016 / S0040-4020 (01) 90985-8.
- ^ Rothgery, E. F .; Holt, R. J .; McGee, H. A. (1975). "Kryochemická syntéza a molekulární energetika cyklopropanonu a některých příbuzných sloučenin". Journal of the American Chemical Society. 97 (17): 4971–4973. doi:10.1021 / ja00850a034.
- ^ Turro, Nicholas J. (1969). „Cyklopropanony“. Účty chemického výzkumu. 2: 25–32. doi:10.1021 / ar50013a004.
- ^ Turro, Nicholas J .; Edelson, Simon S .; Williams, John R .; Darling, Thomas R .; Hammond, Willis B. (1969). „Cyklopropanony. XII. Cykloadiční reakce cyklopropanonů“. Journal of the American Chemical Society. 91 (9): 2283–2292. doi:10.1021 / ja01037a018.
- ^ Edelson, Simon S .; Turro, Nicholas J. (1970). „Cyklopropanony. XVII. Kinetika cykloadiční reakce cyklopropanonů s 1,3-dieny“. Journal of the American Chemical Society. 92 (9): 2770–2773. doi:10.1021 / ja00712a030.
- ^ Greene, Frederick D .; Sclove, David B .; Pazos, Jose F .; Camp, Ronald L. (1970). "Tepelné reakce cyklopropanonu. Racemizace a dekarbonylace trans-2,3-di-terc-butylcyklopropanonu". Journal of the American Chemical Society. 92 (25): 7488. doi:10.1021 / ja00728a051.
- ^ Moiseev, Andrey G .; Abe, Manabu; Danilov, Evgeny O .; Neckers, Douglas C. (2007). "První přímá detekce 2,3-dimethyl-2,3-difenylcyklopropanonu". The Journal of Organic Chemistry. 72 (8): 2777–2784. doi:10.1021 / jo062259r. PMID 17362038.