Chlorid sírový pentafluorid - Sulfur chloride pentafluoride
| |||
| Jména | |||
|---|---|---|---|
| Ostatní jména Pentafluorochlorsulfanyl | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChemSpider | |||
| Informační karta ECHA | 100.034.014 | ||
PubChem CID | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| SClF 5 | |||
| Molární hmotnost | 162,510 g mol−1 | ||
| Vzhled | Bezbarvý plyn | ||
| Hustota | 6,642 g dm−3 | ||
| Bod tání | -64 ° C (-83 ° F; 209 K) | ||
| Bod varu | −19 ° C (−2 ° F; 254 K) | ||
| Nebezpečí | |||
| Hlavní nebezpečí | Toxický | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
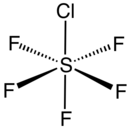
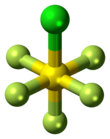
Chlorid sírový pentafluorid je anorganická sloučenina se vzorcem SF
5Cl. Existuje jako bezbarvý plyn při pokojové teplotě a je vysoce toxický, jako většina anorganických sloučenin obsahujících pentafluorosulfid (SF5) funkční skupina.[1] Sloučenina přijímá oktaedrickou geometrii s C
4v symetrie. Chlorid sírový pentafluorid je jediným komerčně dostupným činidlem pro přidání SF
5 skupina na organické sloučeniny.[2][3]
Reaktivita
Na rozdíl od vysoké reaktivity a toxicity SF
5Cl, fluorid sírový (SF
6), je inertní a netoxický, přestože má blízce příbuzný chemický vzorec. Tento rozdíl zdůrazňuje labilitu vazby S-Cl v této molekule.
Pod volné radikály podmínky, SF
5Cl přidává přes dvojné vazby. Následující reakce zahrnuje reakci propen:
- CH
3CHCH
2 + SF
5Cl → CH3CH (Cl) CH2SF5
Adiční reakce je katalyzována Et
3B při asi -30 ° C. SF
5Br se používá obdobně.[2]
SF
5Cl je také předchůdcem O (SF5)2 a F2NSF5 (z tetrafluorhydrazin ).
Syntéza
Chlorpentafluorid síry lze syntetizovat několika způsoby, počínaje dvěma fluoridy s nižší sírou, tetrafluorid síry a disulfur dekafluorid:[1]
- SF
4 + Cl
2 + CsF → SF
5Cl + CsCl - ClF + SF
4 → SF
5Cl - S
2F
10 + Cl
2 → 2 SF
5Cl
Korespondence SF
5Br je připraven podobně z generovaného in-situ bromfluorid.[4]
Reference
- ^ A b Nyman, F., Roberts, H. L., Seaton, T. "Pentafluoride chlorid sírový", Anorganic Syntheses, 1966, svazek 8, s. 1. 160. doi:10.1002 / 9780470132395.ch42
- ^ A b Dolbier, William R .; et al. (2006). "Pohodlná a účinná metoda pro zabudování pentafluorosulfanylu (SF5) substituenty na alifatické sloučeniny “. Journal of Fluorine Chemistry. 127 (10): 1302–10. doi:10.1016 / j.jfluchem.2006.05.003.
- ^ Savoie, Paul R .; Welch, John T. (2015). „Příprava a použitelnost organických sloučenin obsahujících pentafluorosulfanyl“. Chemické recenze. 115 (2): 1130–1190. doi:10.1021 / cr500336u. PMID 25341449.
- ^ Winter, Rolf; Terjeson, Robin J .; Gard, Gary L. (1998). „Vylepšená a snadná příprava SF5Br ". Journal of Fluorine Chemistry. 89: 105–106. doi:10.1016 / S0022-1139 (98) 00094-3.
| Tento anorganické sloučenina –Vztahující se článek je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |