Kyselina sulfanilová - Sulfanilic acid
 | |
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Kyselina 4-aminobenzen-l-sulfonová[1] | |
| Ostatní jména Kyselina 4-aminobenzensulfonová p-Aminobenzensulfonová kyselina Kyselina sulfanilová (nezachycená)[1]) | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| Informační karta ECHA | 100.004.075 |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C6H7NE3S | |
| Molární hmotnost | 173.19 |
| Hustota | 1.485 |
| Bod tání | 288 ° C (550 ° F; 561 K) |
| 12,51 g / l | |
| Kyselost (strK.A) | 3,23 (H2Ó)[2] |
| Související sloučeniny | |
Příbuzné sulfonové kyseliny | Kyselina benzensulfonová kyselina p-toluensulfonová |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Kyselina sulfanilová (Kyselina 4-aminobenzensulfonová) je špinavě bílá krystalická pevná látka, která najde uplatnění v kvantitativní analýza z dusičnan a dusitany ionty. Pevná kyselina existuje jako a zwitterion a má neobvykle vysokou hodnotu bod tání.[3]
Syntéza
Kyselinu sulfanilovou lze vyrobit pomocí sulfonace z anilin:[4]
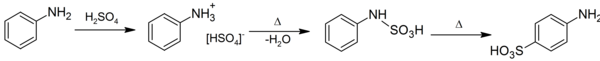
Aplikace
Jak se sloučenina snadno tvoří diazo sloučeniny, používá se k výrobě barviv a sulfa léky.[3] Tato vlastnost se také používá pro kvantitativní analýza z dusičnan a dusitany ionty diazoniová vazebná reakce s N- (1-naftyl) ethylendiamin, což má za následek azobarvivo a koncentraci dusičnan nebo dusitany ionty byly odvozeny z intenzity barvy výsledného červeného roztoku pomocí kolorimetrie.[5]
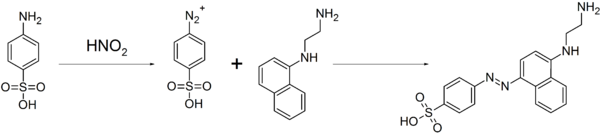
Používá se také jako standard v analýza spalování a v Pauly reakce.
Deriváty
- Methylová oranžová (azo vazba s dimethylanilin )
- Kyselina oranžová 7 (azo vazba s 2-naftol )
- Chrysoinový resorcinol (azo vazba s resorcinol )
Konečné použití
Kyselina sulfanilová má čtyři primární konečné použití. Používá se jako meziprodukt při výrobě žlutého potravinářského barviva, specifických farmaceutických aplikací, optických zjasňovačů pro bílý papír a jako přísada do betonu. Meziprodukt obsahující kyselinu sulfanilovou lze zakoupit ve čtyřech různých třídách: technická, čistá, roztok sulfanilátu sodného a suchý prášek sulfanilátu sodného.
Viz také
Reference
- ^ A b Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 789. doi:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
Název „kyselina sulfanilová“ se nezachoval.
- ^ Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (97. vydání). CRC Press. p. 5–88. ISBN 978-1498754286.
- ^ A b "Kyselina sulfanilová". Slovník chemie. Oxford University Press, 2000. Oxford Reference Online. Oxford University Press.
- ^ Siegfried Hauptmann: Organische Chemie, 2. vydání, VEB Deutscher Verlag für Grundstoffindustrie, Lipsko, 1985, s. 511, ISBN 3-342-00280-8.
- ^ G. H. Jerffery; J. Bassett; J. Mendham; R. C. Denney (1989). "Kolorimetrie a spektrofotometrie". Vogelova učebnice kvantitativní chemické analýzy, 5. vydání. Longman. p. 702. ISBN 0-582-44693-7.
