Skandium (III) trifluormethansulfonát - Scandium(III) trifluoromethanesulfonate
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC Scandium trifluormethansulfonát | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.157.499 |
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C3F9Ó9S3Sc | |
| Molární hmotnost | 492,16 g / mol |
| Nebezpečí | |
| Bezpečnostní list | Oxford MSDS |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Scandium trifluormethansulfonát, běžně nazývaný skandium triflát, je chemická sloučenina se vzorcem Sc (SO3CF3)3, a sůl skládající se z skandium kationty Sc3+ a triflate TAK3CF3− anionty.
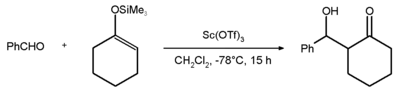
Skandium triflát se používá jako činidlo v organické chemii jako a Lewisova kyselina.[1] Ve srovnání s jinými Lewisovými kyselinami je toto činidlo stabilní vůči vodě a lze jej často použít organické reakce jako pravda katalyzátor spíše než jeden použitý ve stechiometrických množstvích. Sloučenina se připraví reakcí oxid skandia s kyselina trifluormethansulfonová.
Příkladem vědeckého použití skandium triflátu je Přidání Mukaiyama aldolu reakce mezi benzaldehyd a silyl enol ether z cyklohexanon s 81% výtěžek.[2]
Reference
- ^ Deborah Longbottom (1999). „SYNLETT Spotlight 12: Scandium Triflate“. Synlett. 1999 (12): 2023. doi:10.1055 / s-1999-5997.
- ^ S. Kobayashi (1999). „Scandium Triflate v organické syntéze“. Eur. J. Org. Chem. 1999: 15–27. doi:10.1002 / (SICI) 1099-0690 (199901) 1999: 1 <15 :: AID-EJOC15> 3.0.CO; 2-B. Archivovány od originál dne 05.01.2013.