Příprava vzorků v hmotnostní spektrometrii - Sample preparation in mass spectrometry
Příprava vzorků pro hmotnostní spektrometrii se používá k optimalizaci vzorku pro analýzu v a hmotnostní spektrometr (SLEČNA). Každá ionizační metoda má určité faktory, které je třeba vzít v úvahu, aby tato metoda byla úspěšná, například objem, koncentrace, fáze vzorku a složení analyt řešení. Pravděpodobně nejdůležitějším aspektem při přípravě vzorku je vědět, v jaké fázi musí být vzorek, aby byla analýza úspěšná. V některých případech musí být samotný analyt před vstupem do iontový zdroj. V jiných situacích matice nebo vše v roztoku obklopujícím analyt je nejdůležitějším faktorem, který je třeba zvážit a upravit. Samotné přípravě vzorků pro hmotnostní spektrometrii lze často zabránit spojením hmotnostní spektrometrie s a chromatografie před vstupem do hmotnostního spektrometru. V některých případech musí být samotný analyt upraven tak, aby byla možná analýza, například v hmotnostní spektrometrie proteinů, kde obvykle protein zkoumaná oblast se před analýzou štěpí na peptidy, buď trávení v gelu nebo proteolýza v řešení.
Ukázková fáze
| Ukázková fáze | Ionizační metoda |
|---|---|
| Pevný | Polní desorpce |
| Desorpce plazmy | |
| Fast Atom Bombardment (FAB) | |
| Sekundární iont (SIMS) | |
| Okolní ionizace | |
| Řešení | Maticová laserová desorpční ionizace (MALDI) |
| Elektrosprej (ESI) | |
| Chemická ionizace za atmosférického tlaku (APCI) | |
| Okolní ionizace | |
| Plyn | Elektronová ionizace |
| Fotoionizace | |
| Chemická ionizace |
Prvním a nejdůležitějším krokem při přípravě vzorku pro hmotnostní spektrometrii je určení, v jaké fázi se vzorek musí nacházet. Různé ionizační metody vyžadují různé fáze vzorku. Vzorky v pevné fázi mohou být ionizovány způsoby, jako je polní desorpce, plazmatická desorpce, rychlé bombardování atomy, a sekundární iontová ionizace. Kapaliny, v nichž je analyt rozpuštěn, nebo roztoky, mohou být ionizovány metodami, jako je např laserová desorpce podporovaná matricí , ionizace elektrosprejem, a chemická ionizace za atmosférického tlaku. Mohou být ionizovány pevné i kapalné vzorky ionizace okolí techniky.
Vzorky plynů nebo těkavé vzorky lze ionizovat pomocí metod, jako je např elektronová ionizace, fotoionizace, a chemická ionizace.
Tyto seznamy jsou nejčastěji používaným stavem hmoty pro každou ionizační metodu, ale ionizační metody nejsou nutně omezeny na tyto stavy hmoty. Například ionizace bombardováním rychlými atomy se obvykle používá k ionizaci pevných vzorků, ale tato metoda se obvykle používá na pevných látkách rozpuštěných v roztocích a lze ji také použít k analýze složek, které vstoupily do plynné fáze.[1][2][3]
Chromatografie jako metoda přípravy vzorku
U mnoha ionizačních metod hmotnostní spektrometrie musí být vzorek v kapalné nebo plynné fázi, aby ionizační metoda fungovala. Příprava vzorku pro zajištění správné ionizace může být obtížná, ale lze ji usnadnit připojením hmotnostního spektrometru k některému chromatografickému zařízení. Plynová chromatografie (GC) nebo kapalinová chromatografie (LC) lze použít jako metodu přípravy vzorku.
Plynová chromatografie

GC je metoda zahrnující separaci různých analytů ve vzorku směsných plynů. Oddělené plyny lze detekovat několika způsoby, ale jednou z nejúčinnějších detekčních metod pro plynovou chromatografii je hmotnostní spektrometrie. Poté, co se plyny oddělí, vstupují do hmotnostního spektrometru a jsou analyzovány. Tato kombinace nejen odděluje analyty, ale poskytuje strukturální informace o každém z nich. Vzorek GC musí být nestálý, nebo schopné vstoupit do plynné fáze, přičemž je také tepelně stabilní, takže se nerozkládá, protože je zahříváno pro vstup do plynné fáze.[4][5] Obdobné obavy mají i ionizační techniky hmotnostní spektrometrie vyžadující, aby byl vzorek v plynné fázi.
Elektronová ionizace (EI) v hmotnostní spektrometrii vyžaduje vzorky, které jsou malé molekuly, těkavé a tepelně stabilní, podobné jako u plynové chromatografie. Tím je zajištěno, že pokud je na vzorku prováděno GC před vstupem do hmotnostního spektrometru, bude vzorek připraven na ionizaci pomocí EI.[6][7]
Chemická ionizace (CI) je další metoda, která vyžaduje, aby vzorky byly v plynné fázi. To proto, aby vzorek mohl reagovat s a činidlo plyn za vzniku iontu, který lze analyzovat hmotnostním spektrometrem. CI má mnoho stejných požadavků na přípravu vzorku jako EI, jako je těkavost a tepelná stabilita vzorku. GC je také užitečné pro přípravu vzorků pro tuto techniku.[8] Jednou výhodou CI je, že větší molekuly oddělené GC mohou být analyzovány touto ionizační metodou. CI má větší hmotnostní rozsah než EI a může analyzovat molekuly, které EI nemusí být schopen. CI má také tu výhodu, že je méně škodlivé pro molekulu vzorku, takže méně fragmentace dojde a lze zjistit více informací o původním analytu.[6][9]
Fotoionizace (PI) byla metoda, která byla poprvé použita jako ionizační metoda k detekci plynů oddělených GC.[10] O několik let později byl také použit jako detektor pro LC, ačkoli vzorky musí být nejprve odpařeny, aby byly detekovány fotoionizačním detektorem. Nakonec byl PI aplikován na hmotnostní spektrometrii, zejména jako ionizační metoda pro plynová chromatografie - hmotnostní spektrometrie.[11] Příprava vzorku pro PI zahrnuje nejprve zajištění, že je vzorek v plynné fázi. PI ionizuje molekuly tím, že excituje molekuly vzorku fotony světla. Tato metoda funguje pouze v případě, že vzorek a další složky v plynné fázi jsou excitovány různými vlnové délky světla. Při přípravě vzorku nebo zdroje fotonu je důležité, aby byly vlnové délky ionizace upraveny tak, aby vzrušovaly vzorek analytu a nic jiného.[6]
Kapalinová chromatografie

Kapalinová chromatografie (LC) je metoda, která je v některých ohledech výkonnější než GC, ale lze ji stejně snadno spojit s hmotnostní spektrometrií. V LC mohou být obavy týkající se přípravy vzorku minimální. V LC může jak stacionární, tak mobilní fáze ovlivnit oddělení, zatímco v GC by měla mít vliv pouze stacionární fáze. To umožňuje, aby příprava vzorku byla minimální, pokud je člověk ochoten upravit stacionární fázi nebo mobilní fázi před spuštěním vzorku. Primárním zájmem je koncentrace analytu. Pokud je koncentrace příliš vysoká, může být separace neúspěšná, ale hmotnostní spektrometrie jako metoda detekce nevyžaduje úplnou separaci, což ukazuje další výhodu vazby LC na hmotnostní spektrometr.[12]
LC lze spojit s hmotnostní spektrometrií odpařováním kapalných vzorků při jejich vstupu do hmotnostního spektrometru. Tato metoda umožňuje ionizační metody, které vyžadují použití plynných vzorků, zejména CI nebo PI chemická ionizace za atmosférického tlaku nebo fotoionizace za atmosférického tlaku, která umožňuje více interakcí a více ionizace.[6][13] Jiné ionizační metody nemusí vyžadovat odpaření kapalného vzorku a mohou analyzovat samotný kapalný vzorek. Jedním příkladem je ionizace bombardováním rychlými atomy, která umožňuje tekutým vzorkům odděleným LC proudit do ionizační komory a snadno je ionizovat.[1] Nejběžnější ionizační metodou spojenou s LC je nějaká forma ionizace postřikem, která zahrnuje termosprejovou ionizaci a častěji ionizaci elektrosprejem (ESI).
Termosprej byl poprvé vyvinut jako způsob, jak efektivně odstranit solventní a snadněji odpařovat vzorky. Tato metoda zahrnuje kapalný vzorek z LC protékající elektricky vyhřívaným odpařovačem, který jednoduše ohřívá vzorek, odstraňuje veškeré rozpouštědlo a proto uvádí vzorek do plynné fáze.[14] Elektrosprej ionizace (ESI) je obdobou termospreje v principu co největšího odstraňování kapalného rozpouštědla ze vzorku a vytváření molekul nabitého vzorku buď v malých kapičkách, nebo ve formě plynu. Studie ukázaly, že ESI může být až desetkrát citlivější než jiné ionizační metody spojené s LC.[12] Metody postřiku jsou zvláště užitečné vzhledem k tomu, že pomocí této metody lze snadno analyzovat netěkavé vzorky, protože samotný vzorek se nezmění na plyn, kapalina se jednoduše odstraní a vtlačí vzorek do plynné nebo mlžné fáze.[14]
Jeden problém přípravy vzorku s kapalinová chromatografie - hmotnostní spektrometrie je možné matice účinky v důsledku přítomnosti molekul pozadí. Ukázalo se, že tyto maticové efekty snižují signál v metodách, jako je PI a ESI, až o 60% v závislosti na analyzovaném vzorku. Efekt matice může také způsobit zvýšení signálu a produkovat falešně pozitivní výsledky. To lze napravit co největším vyčištěním vzorku před provedením LC, ale v případě analýzy vzorků prostředí, kde je vše ve vzorku znepokojující, nemusí být příprava vzorku ideálním řešením k vyřešení problému. Další metodou, kterou lze použít k nápravě problému, je použití standardní metody přidání.[12][15]
Rychlé bombardování atomy
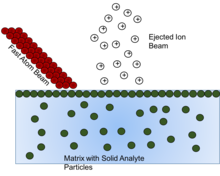
Rychlé bombardování atomy (FAB) je metoda zahrnující použití paprsku vysoké energie atomy narazit na povrch a generovat ionty. Tyto pevné částice analytu musí být rozpuštěny v nějaké formě matice nebo energeticky nezávislé kapalina pro ochranu a pomoc při ionizaci pevného analytu. Ukázalo se, že jak je matice vyčerpána, tvorba iontů klesá, takže výběr správné matricové sloučeniny je zásadní.[16]
Celkovým cílem maticové sloučeniny je představit vzorek paprsku atomu na vysoce pohyblivém povrchu koncentrace. Pro maximální citlivost by měl vzorek tvořit perfektní jednovrstvá na povrchu a Podklad s nízkou volatilitou.[17] Tento efekt monovrstvy lze vidět v tom, že jakmile se dosáhne určité koncentrace analytu v matrici, jakákoli koncentrace vyšší, než je ta, která nemá žádný účinek, protože jakmile se vytvoří monovrstva, jakýkoli další analyt je pod monovrstvou, a tudíž není ovlivněn paprsek atomu. Je vidět, že koncentrace potřebná k vyvolání tohoto efektu se mění, jak se mění množství netěkavé matrice. Při přípravě roztoku pro analýzu je tedy třeba vzít v úvahu koncentraci pevného analytu, aby nezmeškal signál ze „skrytého“ analytu.[17]
Při výběru matice pro každý pevný analyt je třeba vzít v úvahu tři kritéria. Nejprve by měl rozpustit pevnou sloučeninu, která má být analyzována (s nebo bez pomocného rozpouštědla nebo přísady), což umožní molekulám této sloučeniny šířit k povrchovým vrstvám a doplnění vzorku molekuly které byly ionizovány nebo zničeny interakcí s paprskem rychlých atomů. Další mechanismus pro vysvětlení tvorby iontů ve FAB zahrnuje myšlenku, že k naprašování dochází spíše z objemu než z povrchu, ale v tom případě rozpustnost je stále velmi důležité zajistit stejnorodost pevného analytu v objemovém roztoku.[16][17] Zadruhé, matice by měla mít nízkou těkavost za podmínek hmotnostního spektrometru. Jak již bylo zmíněno výše, jak je matice vyčerpána, ionizace také klesá, takže udržování matice je životně důležité. Za třetí, matice by neměla reagovat s dotyčným pevným analytem, nebo pokud reaguje, měla by být srozumitelná a reprodukovatelná.[16] Tím je zajištěna reprodukovatelnost analýzy a identifikace skutečného analytu spíše než a derivát analytu.
Nejčastěji používané sloučeniny jako matrice jsou varianty glycerol, jako je glycerol, deuteroglycerol, thioglycerol a aminoglycerol. Pokud se vzorek nemůže rozpustit ve vybrané matrici, jako je glycerol, lze s matricí smíchat pomocné rozpouštědlo nebo přísadu, aby se usnadnilo rozpouštění pevného analytu. Například, chlorofyl A je zcela nerozpustný v glycerolu, ale smícháním v malém množství Triton X-100, derivát polyethylenglykol se chlorofyl stává vysoce rozpustným v matrici.[17][18] Je důležité si uvědomit, že ačkoli dobrého signálu lze dosáhnout pomocí glycerolu nebo glycerolu s přísadou, mohou existovat další matricové sloučeniny, které mohou nabídnout ještě lepší signál. Optimalizace maticových sloučenin a koncentrace pevného analytu jsou pro měření FAB zásadní.
Hmotnostní spektrometrie sekundárních iontů
Hmotnostní spektrometrie sekundárních iontů (SIMS) je metoda velmi podobná metodě FAB v tom, že paprsek částic je vypalován na povrch vzorku, aby způsobil prskání, ve kterém molekuly vzorku ionizují a opouštějí povrch, což umožňuje analýzu iontů nebo vzorku. Hlavní rozdíl spočívá v tom, že v SIMS je iontový paprsek vystřelen na povrch, ale ve FAB je paprsek atomu vystřelen na povrch. Další primární rozdíl, který tuto stránku více zajímá, je, že na rozdíl od FAB se SIMS obvykle provádí na pevném vzorku s malou potřebnou přípravou vzorku.[19]
Hlavním hlediskem u SIMS je zajistit, aby byl vzorek stabilní pod ultravysoké vakuum nebo tlaky menší než 10−8 torr. Povaha ultravysokého vakua spočívá v tom, že zajišťuje, že vzorek zůstane během analýzy konstantní, a také zajistí, že na vzorek zasáhne iontový paprsek s vysokou energií. Ultravysoké vakuum řeší mnoho problémů, které je třeba vzít v úvahu během přípravy vzorku.[20] Při přípravě vzorku k analýze je třeba vzít v úvahu tloušťku filmu. Typicky, pokud lze tenkou monovrstvu uložit na povrch a ušlechtilý kov, analýza by měla být úspěšná.[21] Pokud je tloušťka filmu příliš velká, což je v analýze v reálném světě běžné, lze problém vyřešit metodami, jako je nanášení perforované stříbrné fólie přes niklovou mřížku na povrch fólie. To poskytuje podobné výsledky jako tenké filmy nanášené přímo na ušlechtilý kov.[19]
Maticová laserová desorpce / ionizace
Pro laserová desorpce / ionizace za pomoci matice (MALDI) hmotnostní spektrometrie, kde je pevný nebo kapalný vzorek smíchán s a matice řešení, aby se vzorek vyhnul procesům, jako je agregace nebo srážky, a zároveň pomáhá vzorku zůstat stabilní během ionizačního procesu.[22][23] Matice krystalizuje se vzorkem a poté se uloží na desku se vzorkem, která může být vyrobena z řady materiálů, od inertní kovy na inertní polymery. Matrice obsahující molekuly vzorku je poté přenesena do plynná fáze pulzně laser ozáření. Během přípravy vzorku je nesmírně důležité složení matice, interakce mezi vzorkem a matricí a způsob ukládání vzorku, aby byly zajištěny nejlepší možné výsledky.
Výběr matice je prvním krokem při přípravě vzorků pro analýzu MALDI. Primárním cílem matice je absorbovat energii z laseru, a tím ji přenést na molekuly analytu, a oddělit molekuly analytu od sebe navzájem.[24] Při výběru matice je třeba vzít v úvahu to, jaký typ iontu analytu se očekává nebo požaduje. Znalost kyselosti nebo zásaditosti molekuly analytu ve srovnání například s kyselostí nebo zásaditostí matrice je cennou znalostí při výběru matrice. Matice by neměla soutěžit s molekulou analytu, takže by matice neměla chtít vytvářet stejný typ iontu jako analyt. Například pokud má požadovaný analyt vysoké množství kyselosti, bylo by logické zvolit matrici s velkým množstvím zásaditosti, aby se zabránilo konkurenci a usnadnila se tvorba iontu.[25] PH matrice lze také použít k výběru vzorku, pro který chcete získat spektra. Například v případě bílkovin velmi kyselý pH může ukázat velmi málo z peptid komponenty, ale může ukázat velmi dobrý signál pro ty komponenty, které jsou větší. Pokud se pH zvýší směrem k zásaditějšímu pH, bude menší složka lépe viditelná.[26]

Koncentrace soli ve vzorku je faktor, který je třeba vzít v úvahu i při přípravě vzorku MALDI. Solí může pomoci MALDI spektrum tím, že zabrání agregaci nebo srážení při stabilizaci vzorku. Lze však pozorovat rušivé signály v důsledku vedlejších reakcí matice se vzorkem, například v případě interakce matice s alkalický kov ionty, které mohou narušit analýzu spekter. Typicky se množství soli v matrici stává problémem pouze ve velmi vysokých koncentracích, jako je například 1 molární.[23] Problém s příliš vysokou koncentrací soli ve vzorku lze vyřešit tak, že se roztok nejprve nechá projít kapalinovou chromatografií, která pomůže vyčistit vzorek, ale tato metoda je časově náročná a vede ke ztrátě části analyzovaného vzorku. Další metoda je zaměřena na čištění, jakmile je roztok vzorku nanesen na sondu. Mnoho vzorkových sond může být navrženo tak, aby měly na povrchu membránu, která může selektivně vázat dotyčný vzorek na povrch sondy. Poté lze povrch opláchnout, aby se odstranily všechny zbytečné soli nebo molekuly pozadí. Matrice vhodné koncentrace soli pak může být nanesena přímo na vzorek na povrch sondy a tam krystalizovat.[23] Navzdory těmto negativním účinkům koncentrace solí není obvykle v případě bílkoviny, protože výběr vhodných nárazník soli brání vzniku tohoto problému.[27]
Při přípravě vzorku je třeba vzít v úvahu také to, jak je vzorek a matrice ukládány na povrch sondy. Metoda sušených kapek je nejjednodušší metodou nanášení. Matrice a roztok vzorku se smísí a poté se malá kapka směsi umístí na povrch sondy vzorku a nechá se zaschnout, čímž dojde ke krystalizaci. Sendvičová metoda zahrnuje uložení vrstvy matrice na povrch sondy a její vysušení. Kapka vzorku následovaná kapkou další matrice se poté nanese na vrstvu sušené matrice a nechá se také zaschnout.[28] Varianty sendvičové techniky zahrnují nanášení matrice na povrch a následné nanášení vzorku přímo na matrici. Obzvláště užitečná metoda spočívá v nanášení roztoku matrice na povrch sondy vzorku v rozpouštědle, které bude odpaří se velmi rychle, čímž se vytvoří velmi tenká jemná vrstva matrice. Roztok vzorku se poté umístí na horní část matricové vrstvy a nechá se pomalu odpařovat, čímž se integruje vzorek do horní vrstvy matrice, když se roztok vzorku odpařuje.[29] Další obavou při ukládání vzorku na povrch sondy je rozpustnost vzorku v matrici. Pokud je vzorek nerozpustný v matrici, musí být použity další metody. Metoda použitá v tomto případě zahrnuje mechanické mletí a míchání pevných vzorků a krystalů pevné matrice. Jakmile je tento prášek dobře promíchán, může být nanesen na povrch vzorkovací sondy ve formě volného prášku nebo jako pilulka. Další možnou metodou je umístění vzorku na povrch sondy a nanesení odpařené matrice na sondu vzorku, aby se matrice kondenzovala kolem vzorku.[30]
Elektrosprejová ionizace
Elektrosprejová ionizace (ESI) je technika, která zahrnuje použití vysokého napětí k vytvoření elektrosprej nebo pokuta aerosol vytvořené vysokými napětími.[31] Příprava vzorku ESI může být velmi důležitá a kvalita výsledků může být silně určena charakteristikami vzorku.[32] ESI experimenty mohou být prováděny online nebo offline. Při on-line měření je hmotnostní spektrometr připojen k a kapalinový chromatograf a jelikož jsou vzorky odděleny, jsou ionizovány do hmotnostního spektrometru systémem ESI; příprava vzorku se skutečně provádí před LC separací.[33] Při off-line měření se roztok analytu aplikuje přímo na hmotnostní spektrometr pomocí kapiláry ve spreji. Off-line příprava vzorků má mnoho ohledů, například skutečnost, že použitá kapilára umožňuje aplikaci objemů v rozsahu nanoliterů, které mohou obsahovat příliš malou koncentraci pro analýzu mnoha sloučenin, jako jsou proteiny. Dalším problémem může být ztráta signálu ESI v důsledku interference mezi vzorkem analytu a složkami pozadí. Bohužel se ukázalo, že samotná příprava vzorku může tento problém jen mírně zmírnit, což je způsobeno spíše povahou samotného analytu než přípravkem.[34] V ESI principiální problém nepochází z reakcí v plynné fázi, ale spíše z problémů zahrnujících fázi řešení samotných kapiček. Problémy mohou být způsobeny netěkavými látkami, které zůstávají v kapkách, což může změnit účinnost tvorby kapiček nebo odpařování kapiček, což zase ovlivňuje množství nabitých iontů v plynné fázi, které nakonec dosáhnou hmotnostního spektrometru. Tyto problémy lze opravit několika způsoby, včetně zvýšení množství koncentrace analytu ve srovnání s matricí v roztoku vzorku nebo spuštěním vzorku pomocí rozsáhlejší chromatografické techniky před analýzou.[35][36] Příklad chromatografické techniky, která může pomoci při signálu v ESI, zahrnuje použití 2-D kapalinové chromatografie nebo spuštění vzorku dvěma samostatnými chromatografické kolony, což umožňuje lepší oddělení analytu od matrice.[37][38]

ESI variace

Existují některé metody ESI, které vyžadují malou nebo žádnou přípravu vzorku. Jednou z takových metod je metoda nazývaná extrakční elektrosprejová ionizace (EESI). Tato metoda zahrnuje elektrosprej rozpouštědla namířený pod úhlem proti jinému rozprašování roztoku vzorku, produkovaného samostatným rozprašovačem. Tato metoda nevyžaduje žádnou přípravu vzorku, protože elektrosprej rozpouštědla extrahuje vzorek ze složité směsi a účinně odstraňuje veškeré kontaminující látky v pozadí.[39] Další obzvláště silná variace na ESI je desorpční elektrosprejová ionizace (DESI), který zahrnuje směrování elektrospreje na povrch se vzorkem naneseným na něj. Vzorek je ionizován v elektrospreji, když stříká z povrchu a poté putuje do hmotnostního spektrometru. Tato metoda je důležitá, protože pro tuto metodu není nutná žádná příprava vzorku. Vzorek je třeba jednoduše uložit na povrch, například na papír.[40] Chemická ionizace za atmosférického tlaku (APCI) je podobný ESI v tom, že vzorek je rozprášen v kapičkách, které jsou poté odpařeny a zanechávají za sebou nabitý iont, který má být analyzován. APCI zažívá několik negativních účinků matrice, které zažívá ESI kvůli skutečnosti, že v této metodě dochází k ionizaci v plynné fázi, spíše než uvnitř kapiček kapaliny jako v ESI, a skutečnosti, že v APCI je nadbytek reakčního plynu, tedy minimalizace účinku matrice na ionizační proces.[41][42]
Protein ESI
Hlavní aplikací pro ESI je oblast hmotnostní spektrometrie proteinů. Zde se MS používá pro identifikaci a stanovení velikosti proteinů. Identifikaci vzorku proteinu lze provést v ESI-MS pomocí sekvenování peptidů de novo (použitím tandemová hmotnostní spektrometrie ) nebo peptidové hromadné otisky prstů. Obě metody vyžadují předchozí trávení proteinů na peptidy, které se většinou provádí enzymaticky proteázy. Stejně tak pro trávení v roztoku, jako pro trávení v gelu jsou potřebná pufrovaná řešení, jejichž obsah solí je příliš vysoký a v analytu je příliš nízký pro úspěšné měření ESI-MS. Proto se provádí kombinovaný krok odsolování a koncentrace. Obvykle obrácená fáze kapalinová chromatografie se používá, ve kterém peptidy zůstávají navázané na chromatografie matrice, zatímco soli jsou odstraněny promytím. Peptidy lze eluovat z matrice použitím malého objemu roztoku obsahujícího velkou část organický rozpouštědlo, což má za následek snížení konečného objemu analytu. v LC-MS odsolování / koncentrace je realizována pre-kolonou, při off-line měřeních jsou použity mikro kolony s reverzní fází, které mohou být použity přímo s mikrolitrem pipety. Zde se peptidy eluují rozprašovacím roztokem obsahujícím příslušnou část organického rozpouštědla. Výsledný roztok (obvykle několik mikrolitrů) je obohacen o analyt a po přenosu do rozprašovací kapiláry může být přímo použit v MS.
Viz také
Reference
- ^ A b Caprioli, Richard M. (1990-04-15). „Hmotnostní spektrometrie s rychlým atomovým bombardováním s kontinuálním tokem“. Analytická chemie. 62 (8): 477A - 485A. doi:10.1021 / ac00207a715. PMID 2190496.
- ^ Takayama, Mitsuo (1995-07-21). „Hmotnostní spektrometrie s bombardováním rychlými atomy v plynné fázi“. International Journal of Mass Spectrometry and Ion Processes. 152 (1): 1–20. Bibcode:1996IJMSI.152 .... 1T. doi:10.1016/0168-1176(95)04298-9.
- ^ Kralj, B .; Kramer, V .; Vrscaj, V. (1983). "Rychlé atomové bombardování molekul v plynném stavu". International Journal of Mass Spectrometry and Ion Physics. 46: 399–402. Bibcode:1983IJMSI..46..399K. doi:10.1016/0020-7381(83)80136-3.
- ^ James M. Miller (16. prosince 2005). Chromatografie: koncepty a kontrasty. John Wiley & Sons. ISBN 978-0-471-98059-9.
- ^ Mondello, Luigi; Tranchida, Peter Quinto; Dugo, Paola; Dugo, Giovanni (2008). „Komplexní dvourozměrná plynová chromatografie - hmotnostní spektrometrie: přehled“. Recenze hmotnostní spektrometrie. 27 (2): 101–124. Bibcode:2008MSRv ... 27..101M. doi:10. 1002 / mas.20158. ISSN 0277-7037. PMID 18240151.
- ^ A b C d Chhabil Dass (11. května 2007). Základy současné hmotnostní spektrometrie. John Wiley & Sons. ISBN 978-0-470-11848-1.
- ^ Aiken, Allison C .; DeCarlo, Peter F .; Jimenez, Jose L. (2007). "Elementární analýza organických druhů pomocí elektronové ionizace s vysokým rozlišením hmotnostní spektrometrie". Analytická chemie. 79 (21): 8350–8358. doi:10.1021 / ac071150w. ISSN 0003-2700. PMID 17914892.
- ^ Angerosa, Franca; d'Alessandro, Nicola; Corana, Federica; Mellerio, Giorgio (1996). "Charakterizace fenolických a secoiridoidních aglykonů přítomných v panenském olivovém oleji plynovou chromatografií a chemickou ionizační hmotnostní spektrometrií". Journal of Chromatography A. 736 (1–2): 195–203. doi:10.1016 / 0021-9673 (95) 01375-X. ISSN 0021-9673.
- ^ Field, Frank H. (1968). "Hmotnostní spektrometrie s chemickou ionizací". Účty chemického výzkumu. 1 (2): 42–49. doi:10.1021 / ar50002a002. ISSN 0001-4842.
- ^ Driscoll, John N. (1977). "Hodnocení nového fotoionizačního detektoru pro organické sloučeniny". Journal of Chromatography A. 134 (1): 49–55. doi:10.1016 / S0021-9673 (00) 82568-6. ISSN 0021-9673.
- ^ Raffaelli, Andrea; Saba, Alessandro (2003). "Hmotnostní spektrometrie s fotoionizací za atmosférického tlaku". Recenze hmotnostní spektrometrie. 22 (5): 318–331. Bibcode:2003MSRv ... 22..318R. doi:10,1002 / mas. 10060. ISSN 0277-7037. PMID 12949917.
- ^ A b C Petrović, Mira; Hernando, Maria Dolores; Díaz-Cruz, M. Silvia; Barceló, Damià (2005). „Kapalinová chromatografie – tandemová hmotnostní spektrometrie pro analýzu farmaceutických zbytků ve vzorcích prostředí: přehled“. Journal of Chromatography A. 1067 (1–2): 1–14. doi:10.1016 / j.chroma.2004.10.110. ISSN 0021-9673. PMID 15844508.
- ^ Robb, Damon B .; Covey, Thomas R .; Bruins, Andries P. (2000). "Atmosférický tlakový fotoionizace: Ionizační metoda pro kapalinovou chromatografii - hmotnostní spektrometrii". Analytická chemie. 72 (15): 3653–3659. doi:10.1021 / ac0001636. ISSN 0003-2700. PMID 10952556.
- ^ A b Blakley, C. R .; Vestal, M. L. (1983). "Rozhraní pro termosprej pro kapalinovou chromatografii / hmotnostní spektrometrii". Analytická chemie. 55 (4): 750–754. doi:10.1021 / ac00255a036. ISSN 0003-2700.
- ^ Benijts, Tom; Přehrady, Riet; Lambert, Willy; De Leenheer, André (2004). „Počítání účinků matrice v kapalinové chromatografii na prostředí - elektrosprejová ionizace tandemová hmotnostní spektrometrie s analýzou vody pro chemikálie narušující endokrinní systém“. Journal of Chromatography A. 1029 (1–2): 153–159. doi:10.1016 / j.chroma.2003.12.022. ISSN 0021-9673.
- ^ A b C Gower, John Leveson (1985). "Maticové sloučeniny pro hmotnostní spektrometrii bombardování rychlými atomy". Biologická hmotnostní spektrometrie. 12 (5): 191–196. doi:10,1002 / bms.1200120502. ISSN 1052-9306.
- ^ A b C d Barber, Michael; Bordoli, Robert S .; Elliott, Gerald J .; Sedgwick, R. Donald; Tyler, Andrew N. (1982). „Mass Atom Bombardment Mass Spectrometry“. Analytická chemie. 54 (4): 645A - 657A. doi:10.1021 / ac00241a817.
- ^ stránka produktu od Shun Chia
- ^ A b Van Vaeck, Luc; Adriaens, Annemie; Gijbels, Renaat (1999-04-28). „Statická sekundární hmotnostní spektrometrie iontů: (S-SIMS), část 1. Metodika a strukturní interpretace“. Recenze hmotnostní spektrometrie. 18 (1): 1–47. Bibcode:1999MSRv ... 18 .... 1V. doi:10.1002 / (sici) 1098-2787 (1999) 18: 1 <1 :: aid-mas1> 3.3.co; 2-n.
- ^ Belu, Anna M .; Graham, Daniel J .; Castner, David G. (2003). „Hmotnostní spektrometrie sekundárních iontů s časem letu: techniky a aplikace pro charakterizaci povrchů biomateriálů“. Biomateriály. 24 (21): 3635–3653. doi:10.1016 / S0142-9612 (03) 00159-5. ISSN 0142-9612.
- ^ Benninghoven, Alfred; Hagenhoff, Birgit; Niehuis, Ewald (1993-07-15). „Surface MS: Probing Real World Samples“. Analytická chemie. 65 (14): 630A – 640A. doi:10.1021 / ac00062a002.
- ^ Fenyo D; Wang Q; DeGrasse JA; Padovan JC; Cadene M; Chait BT (2007). „Příprava vzorků MALDI: metoda ultra tenké vrstvy“. J Vis Exp (3): 192. doi:10.3791/192. PMC 2535834. PMID 18978997.
- ^ A b C Xu, Yingda; Bruening, Merlin L .; Watson, J. Throck (2003). "Nespecifické metody čištění na sondě pro vzorky MALDI-MS". Recenze hmotnostní spektrometrie. 22 (6): 429–440. Bibcode:2003MSRv ... 22..429X. doi:10,1002 / mas. 10064. ISSN 0277-7037. PMID 14528495.
- ^ Hillenkamp, Franz; Karas, Michael; Beavis, Ronald C .; Chait, Brian T. (1991). „Maticová laserová desorpce / ionizace hmotnostní spektrometrie biopolymerů“. Analytická chemie. 63 (24): 1193A - 1203A. doi:10.1021 / ac00024a716. ISSN 0003-2700. PMID 1789447.
- ^ Zenobi, Renato; Knochenmuss, Richard (1998). "Tvorba iontů v hmotnostní spektrometrii MALDI". Recenze hmotnostní spektrometrie. 17 (5): 337–366. Bibcode:1998MSRv ... 17..337Z. doi:10.1002 / (SICI) 1098-2787 (1998) 17: 5 <337 :: AID-MAS2> 3.0.CO; 2-S. ISSN 0277-7037.
- ^ Cohen, Steven L .; Chait, Brian T. (1996). "Vliv podmínek maticového roztoku na analýzu peptidů a proteinů MALDI-MS". Analytická chemie. 68 (1): 31–37. doi:10.1021 / ac9507956. ISSN 0003-2700. PMID 8779435.
- ^ Smirnov a kol., Anal. Chem., 76 (10), S. 2958-2965, 2004
- ^ Kussmann, Martin; Nordhoff, Eckhard; Rahbek-Nielsen, Henrik; Haebel, Sophie; Rossel-Larsen, Martin; Jakobsen, Lene; Gobom, Johan; Mirgorodskaya, Ekatarina; Kroll-Kristensen, Anne; Palm‖, Lisbeth; Roepstorff, Peter (1997). „Metody přípravy vzorků pro laserovou desorpci / ionizaci pomocí laserové desorpce / ionizace navržené pro různé peptidové a proteinové analyty“. Journal of Mass Spectrometry. 32 (6): 593–601. Bibcode:1997JMSp ... 32..593K. doi:10.1002 / (SICI) 1096-9888 (199706) 32: 6 <593 :: AID-JMS511> 3.0.CO; 2-D. ISSN 1076-5174.
- ^ Vorm, Ole .; Roepstorff, Peter .; Manne, Matthiasi. (1994). "Vylepšené rozlišení a velmi vysoká citlivost v MALDI TOF maticových povrchů díky rychlému odpařování". Analytická chemie. 66 (19): 3281–3287. doi:10.1021 / ac00091a044. ISSN 0003-2700.
- ^ Trimpin, S .; Keune, S .; Räder, H. J .; Müllen, K. (2006). „MALDI-MS bez obsahu rozpouštědel: Vylepšení ve spolehlivosti a potenciálu MALDI při analýze syntetických polymerů a obrovských organických molekul“. Journal of the American Society for Mass Spectrometry. 17 (5): 661–671. doi:10.1016 / j.jasms.2006.01.007. ISSN 1044-0305. PMID 16540340.
- ^ Ho, CS; Chan MHM; Cheung RCK; Zákon LK; Svítí LCW; Ng KF; Suen MWM; Tai HL (únor 2003). „Elektrosprejová ionizační hmotnostní spektrometrie: principy a klinické aplikace“. Clin Biochem Rev. 24 (1): 3–12. PMC 1853331. PMID 18568044.
- ^ Du L; White RL (listopad 2008). "Vylepšený rovnovážný model rozdělení pro predikci odezvy analytu v elektrosprejové ionizační hmotnostní spektrometrii". J Hmotnostní spektrum. 44 (2): 222–9. Bibcode:2009JMSp ... 44..222D. doi:10,1002 / jms.1501. PMID 19003789.
- ^ Pitt, James J (únor 2009). "Principy a aplikace kapalinové chromatografie - hmotnostní spektrometrie v klinické biochemii". Clin Biochem Rev. 30 (1): 19–34. PMC 2643089. PMID 19224008.
- ^ Bonfiglio, Ryan; King, Richard C .; Olah, Timothy V .; Merkle, Kara (1999). "Účinky metod přípravy vzorků na variabilitu elektrosprejové ionizační odezvy pro modelové sloučeniny léčiva". Rychlá komunikace v hmotnostní spektrometrii. 13 (12): 1175–1185. doi:10.1002 / (SICI) 1097-0231 (19990630) 13:12 <1175 :: AID-RCM639> 3.0.CO; 2-0. ISSN 0951-4198.
- ^ King, Richard; Bonfiglio, Ryan; Fernandez-Metzler, Carmen; Miller-Stein, Cynthia; Olah, Timothy (2000). "Mechanické vyšetřování potlačení ionizace při elektrosprejové ionizaci". Journal of the American Society for Mass Spectrometry. 11 (11): 942–950. doi:10.1016 / S1044-0305 (00) 00163-X. ISSN 1044-0305. PMID 11073257.
- ^ Annesley, T. M. (2003). „Potlačení iontů v hmotnostní spektrometrii“. Klinická chemie. 49 (7): 1041–1044. doi:10.1373/49.7.1041. ISSN 0009-9147. PMID 12816898.
- ^ Pascoe, Rob; Foley, Joe P .; Gusev, Arkady I. (2001). „Snížení efektů potlačení signálu souvisejících s matricemi v elektrosprejové ionizační hmotnostní spektrometrii pomocí on-line dvourozměrné kapalinové chromatografie“. Analytická chemie. 73 (24): 6014–6023. doi:10.1021 / ac0106694. ISSN 0003-2700. PMID 11791574.
- ^ Taylor, Paul J. (2005). „Maticové efekty: Achillova pata kvantitativní vysoce účinné kapalinové chromatografie – elektrospreje – tandemová hmotnostní spektrometrie“. Klinická biochemie. 38 (4): 328–334. doi:10.1016 / j.clinbiochem.2004.11.007. ISSN 0009-9120. PMID 15766734.
- ^ Chen, Huanwen; Venter, Andre; Cooks, R. Graham (2006). "Extrakční elektrosprejová ionizace pro přímou analýzu nezředěné moči, mléka a dalších komplexních směsí bez přípravy vzorku". Chemická komunikace (19): 2042–4. doi:10.1039 / b602614a. ISSN 1359-7345. PMID 16767269.
- ^ Chen, Huanwen; Pan, Zhengzheng; Talaty, Nari; Raftery, Daniel; Cooks, R. Graham (2006). "Kombinace desorpční elektrosprejové ionizační hmotnostní spektrometrie a nukleární magnetické rezonance pro diferenciální metabolomiku bez přípravy vzorku". Rychlá komunikace v hmotnostní spektrometrii. 20 (10): 1577–1584. doi:10,1002 / rcm. 2474. ISSN 0951-4198. PMID 16628593.
- ^ Souverain, Sandrine; Rudaz, Serge; Veuthey, Jean-Luc (2004). „Maticový efekt v LC-ESI-MS a LC-APCI-MS s off-line a on-line extrakčními postupy“. Journal of Chromatography A. 1058 (1–2): 61–66. doi:10.1016 / S0021-9673 (04) 01477-3. ISSN 0021-9673.
- ^ Matuszewski, B. K .; Constanzer, M.L .; Chavez-Eng, C. M. (2003). „Strategies for the Assessment of Matrix Effect in Quantitative Bioanalytical Methods Based on HPLC − MS / MS“. Analytická chemie. 75 (13): 3019–3030. doi:10.1021 / ac020361s. ISSN 0003-2700. PMID 12964746.
