Klidový stav fMRI - Resting state fMRI - Wikipedia
| Klidový stav fMRI | |
|---|---|
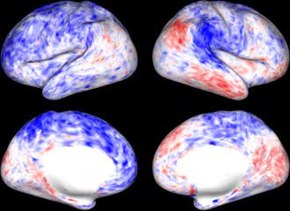
Film o in vivo Tučný signál z kortikální povrch lidského subjektu z HCP, získané pomocí klidového stavu fMRI, předem zpracované pro potlačení šumu v datech[1][2] a přehrávat v reálném čase. Intenzity signálu BOLD jsou zobrazeny na vyhlazeném kortikálním povrchu. V každém bodě na kůra, bílá barva představuje průměrný BOLD signál, zatímco modrá a červená barva představují nižší a vyšší signál než průměrný BOLD signál.[2] | |
| Účel | vyhodnotit regionální interakce, ke kterým dochází v klidovém stavu (mapování mozku) |
Klidový stav fMRI (rsfMRI nebo R-fMRI) je metoda funkční zobrazování magnetickou rezonancí (fMRI), který se používá v mapování mozku vyhodnotit regionální interakce, ke kterým dochází v klidovém nebo negativním stavu úkolu, když se neprovádí explicitní úkol.[3][4] V mozku je identifikována řada stavů klidového stavu, z nichž jeden je výchozí režim sítě.[5] Tyto klidové stavy mozku jsou pozorovány změnami v průtok krve v mozku který vytváří to, co se označuje jako a v závislosti na hladině kyslíku v krvi (BOLD) signál, který lze měřit pomocí fMRI.
Protože mozková aktivita je vnitřní a je přítomen i při absenci externě vyvolaného úkolu, každá oblast mozku bude mít spontánní výkyvy v BOLD signálu. Přístup v klidovém stavu je užitečný k prozkoumání funkční organizace mozku a ke zkoumání, zda je změněna neurologický nebo duševní poruchy. Výzkum funkční konektivity v klidovém stavu odhalil řadu sítí, které se důsledně vyskytují u zdravých subjektů, v různých fázích vědomí a napříč druhy, a představují specifické vzorce synchronní činnosti.[6][7][8]
Základy fMRI
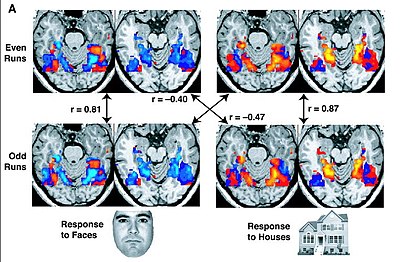
Specifickým je funkční zobrazování magnetickou rezonancí (funkční MRI nebo fMRI) magnetická rezonance (MRI) postup, který měří mozkovou aktivitu detekcí souvisejících změn v průtoku krve. Přesněji řečeno, mozková aktivita se měří prostřednictvím nízkofrekvenčního BOLD signálu v mozku.[9]
Postup je podobný MRI, ale jako základní měřítko se používá změna magnetizace mezi krví bohatou na kyslík a chudou na kyslík. Toto opatření je často poškozeno šumem z různých zdrojů, a proto se k extrakci podkladového signálu používají statistické postupy. Výsledná aktivace mozku může být prezentována graficky barevným kódováním síly aktivace v mozku nebo ve specifické studované oblasti. Technika dokáže lokalizovat aktivitu v milimetrech, ale pomocí standardních technik není lepší než v okně několika sekund.[10]
FMRI se používá jak ve výzkumu, tak v menší míře v klinických podmínkách. Může být také kombinován a doplňován dalšími opatřeními fyziologie mozku, jako je EEG a NIRS.[11][12] Označení arteriální spiny fMRI lze použít jako doplňkový přístup k hodnocení klidových funkcí mozku.[13]
Fyziologický základ
Fyziologická odezva průtoku krve do značné míry rozhoduje o časové citlivosti, o tom, jak dobře lze měřit aktivní neurony v BOLD fMRI. Základní parametr časového rozlišení je vzorkovací frekvence, nebo TR, který určuje, jak často je určitý mozkový plátek vzrušený a může ztratit svoji magnetizaci. TR se mohou lišit od velmi krátkých (500 ms) po velmi dlouhé (3 sekundy). Konkrétně pro fMRI hemodynamická odezva Předpokládá se, že trvá déle než 10 sekund, multiplikativně stoupá (tj. jako podíl aktuální hodnoty), vrcholí ve 4 až 6 sekundách a poté multiplikativně klesá. Změny v systému průtoku krve, vaskulárním systému, integrují reakce na neuronální aktivitu v průběhu času. Protože tato reakce je plynulá nepřetržitá funkce, vzorkování s rychlejšími TR pomáhá pouze mapovat rychlejší fluktuace, jako jsou respirační a srdeční frekvence.[14]
Zatímco fMRI usiluje o měření neuronální aktivity v mozku, BOLD signál může být ovlivněn mnoha dalšími fyziologickými faktory kromě neuronové aktivity. Například fluktuace dýchání a kardiovaskulární cykly ovlivňují BOLD signál měřený v mozku, a proto se je obvykle snaží odstranit během zpracování nezpracovaných dat fMRI. Kvůli těmto zdrojům hluku se objevilo mnoho odborníků, kteří se k myšlence klidového stavu fMRI během raného použití fMRI postavili velmi skepticky. Teprve nedávno se vědci začali domnívat, že měřený signál není artefakt způsobený jinými fyziologickými funkcemi.[15]
Klidový stav funkční konektivita mezi prostorově odlišnými oblastmi mozku odráží opakovanou historii ko-aktivačních vzorců v těchto oblastech, čímž slouží jako míra plasticita.[16]
Dějiny
Bharat Biswal
- V roce 1992 Bharat Biswal zahájil práci jako postgraduální student na The Medical College of Wisconsin pod vedením svého poradce, James S. Hyde, a zjistil, že mozek, i během odpočinku, obsahuje informace o jeho funkční organizaci. Použil fMRI ke studiu toho, jak různé oblasti mozku komunikují, zatímco je mozek v klidu a nevykonává žádnou aktivní úlohu. I když v té době nebyl Biswalův výzkum většinou ignorován a byl přičítán jinému zdroji signálu, jeho klidová neuroimagingová technika byla nyní široce replikována a považována za platnou metodu mapování funkční mozkové sítě. Mapování činnosti mozku, když je v klidu, má mnoho potenciálů pro výzkum mozku a dokonce pomáhá lékařům diagnostikovat různé mozkové choroby.[3]
Marcus Raichle
- Pokusy neurologa Marcus Raichle laboratoř v Lékařská fakulta Washingtonské univerzity a další skupiny ukázaly, že při provádění soustředěného mentálního úkolu je mozková spotřeba energie zvýšena o méně než 5% jeho základní energetické spotřeby. Tyto experimenty ukázaly, že mozek je neustále aktivní s vysokou úrovní aktivity, i když se osoba nezabývá soustředěnou duševní prací (klidový stav). Jeho laboratoř byla primárně zaměřena na hledání základů této odpočinkové činnosti a je připisována mnoha převratnými objevy. Patří mezi ně relativní nezávislost průtoku krve a spotřeby kyslíku během změn v mozkové aktivitě, která poskytovala fyziologický základ fMRI, stejně jako objev dobře známé Výchozí režim Síť.[17]
Konektivita
Funkční
Funkční konektivita je konektivita mezi oblastmi mozku, které sdílejí funkční vlastnosti. Přesněji to lze definovat jako časovou korelaci mezi prostorově vzdálenými neurofyziologickými událostmi, vyjádřenou jako odchylka od statistické nezávislosti napříč těmito událostmi v distribuovaných neuronálních skupinách a oblastech.[18] To platí jak pro studie v klidovém stavu, tak pro studie stavu úlohy. Zatímco funkční konektivita může odkazovat na korelace napříč předměty, běhy, bloky, zkouškami nebo jednotlivými časovými body, funkční konektivita v klidovém stavu se zaměřuje na konektivitu posuzovanou napříč jednotlivými BOLD časovými body během klidových podmínek.[19] Funkční konektivita byla také hodnocena pomocí časových řad perfúze vzorkovaných pomocí perfúzního fMRI označeného jako arteriální spin.[20] MRI s funkční konektivitou (fcMRI), která může zahrnovat fMRI v klidovém stavu a MRI založenou na úlohách, může jednoho dne pomoci poskytnout definitivnější diagnózy poruch duševního zdraví, jako je bipolární porucha a může také pomoci pochopit vývoj a postup posttraumatická stresová porucha stejně jako vyhodnotit účinek léčby.[21] Funkční konektivita byla navržena jako výraz chování sítě, které je základem kognitivní funkce na vysoké úrovni, protože na rozdíl od strukturální konektivity se funkční konektivita často mění v řádu sekund, jako v případě dynamické funkční připojení.
Sítě
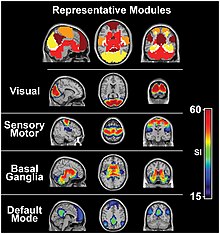
Síť ve výchozím režimu
- The výchozí režim sítě (DMN) je síť oblastí mozku, které jsou aktivní, když je jedinec vzhůru a v klidu.[22] Síť výchozího režimu je propojený a anatomicky definovaný mozkový systém, který se přednostně aktivuje, když se jednotlivci soustředí na interní úkoly, jako je snění, předvídání budoucnosti, získávání vzpomínek a měření perspektiv ostatních.[23] Negativně koreluje s mozkovými systémy, které se zaměřují na vnější vizuální signály. Je to jedna z nejvíce studovaných sítí přítomných v klidovém stavu a je to jedna z nejsnadněji vizualizovaných sítí.[24]
Ostatní klidové státní sítě
- V závislosti na metodě analýzy klidového stavu uvádí studie funkční konektivity řadu neuronové sítě které jsou výsledkem silného funkčního spojení během odpočinku. Mezi klíčové sítě, označované také jako součásti, které jsou uváděny častěji, patří: DMN, smyslové /motor složka, výkonná kontrola složka, až tři různé vizuální komponenty, dvě lateralizované čelní /temenní komponenty, sluchový komponenta a temporální / temenní složka.[25] Jak již bylo uvedeno, tyto sítě v klidovém stavu se skládají z anatomicky oddělených, ale funkčně spojených oblastí, které vykazují vysokou úroveň korelované aktivity BOLD signálu. Zjistilo se, že tyto sítě jsou napříč studiemi celkem konzistentní, navzdory rozdílům v technikách získávání a analýzy dat.[25][26] Důležité je, že většina z těchto složek klidového stavu představuje známé funkční sítě, tj. Oblasti, o nichž je známo, že sdílejí a podporují kognitivní funkce.[7]
Analýza dat
Zpracování údajů
Existuje mnoho programů pro zpracování a analýzu dat fMRI v klidovém stavu. Mezi nejčastěji používané programy patří SPM, AFNI, FSL (zejm. melodický pro ICA), PŘIPOJIT, C-PAC a výpočetní systém Connectome (CCS ).
Metody analýzy
Existuje mnoho metod jak získávání, tak zpracování dat rsfMRI. Nejoblíbenější metody analýzy se zaměřují buď na nezávislé komponenty, nebo na oblasti korelace.
Analýza nezávislých komponent
- Analýza nezávislých komponent (ICA) je užitečný statistický přístup při detekci sítí v klidovém stavu. ICA odděluje signál na nepřekrývající se prostorové a časové složky. Je vysoce datově řízený a umožňuje lepší odstranění hlučných složek signálu (pohyb, drift skeneru atd.). Ukázalo se také, že spolehlivě extrahuje síť ve výchozím režimu i mnoho dalších sítí s velmi vysokou konzistencí.[27][28] ICA zůstává v popředí výzkumných metod.[29]
Regionální analýza
- Mezi další metody pozorování sítí a připojení v mozku patří počáteční mapování d a oblast zájmu (ROI) metody analýzy. V těchto případech signál pouze od určitého voxel nebo shluk voxelů známých jako seed nebo ROI se používají k výpočtu korelací s jinými voxely mozku. To poskytuje mnohem přesnější a podrobnější pohled na specifickou konektivitu v oblastech zájmu mozku.[30][31] Lze také zprůměrovat celkovou konektivitu mezi ROI (například prefrontální kůrou) a všemi ostatními voxely mozku, což poskytuje míru globální mozkové konektivity (GBC) specifickou pro tuto ROI.[32]
Mezi další metody charakterizace sítí v klidovém stavu patří částečná korelace, koherence a částečná koherence, fázové vztahy, dynamické časové deformace vzdálenost, shlukování a teorie grafů.[33][34][35]
Spolehlivost a reprodukovatelnost
Funkční zobrazování magnetickou rezonancí v klidovém stavu (rfMRI) může zobrazovat nízkofrekvenční fluktuace v spontánních činnostech mozku, což představuje oblíbený nástroj pro funkční konektomiku v makrozměrech k charakterizaci mezidividuálních rozdílů v normální funkci mozku, asociací mysli a mozku a různé poruchy. To naznačuje spolehlivost a reprodukovatelnost pro běžně používaná opatření rfMRI odvozená z funkční konektomiky lidského mozku. Tyto metriky mají velký potenciál pro urychlení identifikace biomarkerů pro různá onemocnění mozku, které na prvním místě nazývají potřebu řešit spolehlivost a reprodukovatelnost.[36]
Kombinace zobrazovacích technik
fMRI s EEG
Mnoho odborníků na zobrazování má pocit, že k získání nejlepší kombinace prostorových a časových informací z mozkové činnosti, jak fMRI, tak elektroencefalografie (EEG) by měl být používán současně. Tato duální technika kombinuje dobře zdokumentovanou schopnost EEG charakterizovat určité mozkové stavy s vysokým časovým rozlišením a odhalit patologické vzorce, se schopností fMRI (více nedávno objevená a méně dobře pochopená) zobrazovat dynamiku krve celým mozkem s vysokým prostorovým rozlišením. Až dosud EEG-fMRI byla považována hlavně za techniku fMRI, při které se synchronně získaný EEG používá k charakterizaci mozkové aktivity („stav mozku“) v čase, což umožňuje mapovat (například statistickým parametrickým mapováním) související hemodynamické změny.[37]
Klinická hodnota těchto nálezů je předmětem probíhajících výzkumů, ale nedávné výzkumy naznačují přijatelnou spolehlivost pro studie EEG-fMRI a lepší citlivost ve skeneru s vyšším polem. Mimo oblast epilepsie se EEG-fMRI používá ke studiu mozkových reakcí souvisejících s událostmi (vyvolaných vnějšími podněty) a poskytuje důležité nové poznatky o základní mozkové aktivitě během klidové bdělosti a spánku.[38]
fMRI s TMS
Transkraniální magnetická stimulace (TMS) používá malá a relativně přesná magnetická pole ke stimulaci oblastí kůry bez nebezpečných invazivních postupů. Když tato magnetická pole stimulují oblast kůry, zvyšuje se fokální průtok krve v místě stimulace i ve vzdálených místech anatomicky spojených se stimulovaným místem. Pozitronová emisní tomografie (PET) lze poté použít k zobrazení mozku a změn průtoku krve a výsledky ukazují velmi podobné oblasti konektivity potvrzující sítě nalezené ve studiích fMRI a TMS lze také použít k podpoře a poskytnutí podrobnějších informací o propojených oblastech.[39]
Potenciální úskalí
Potenciálními úskalími při použití rsfMRI k určení funkční integrity sítě je kontaminace signálu BOLD zdroji fyziologického šumu, jako je srdeční frekvence, dýchání,[40][41] a pohyb hlavy.[42][43][44][45] Tyto matoucí faktory mohou často zkreslit výsledky ve studiích, kde jsou pacienti srovnáváni se zdravými kontrolami ve směru předpokládaných účinků, například nižší koherence může být nalezena ve výchozí síti ve skupině pacientů, zatímco skupiny pacientů se také během skenování pohybovaly více . Ukázalo se také, že použití globální regrese signálu může způsobit umělé korelace mezi malým počtem signálů (např. Dvěma nebo třemi).[46] Naštěstí má mozek mnoho signálů.[47]
Současné a budoucí aplikace
Výzkum využívající fMRI v klidovém stavu má potenciál být aplikován v klinickém kontextu, včetně použití při hodnocení mnoha různých onemocnění a duševní poruchy.[48]
Stav nemoci a změny funkční konektivity v klidovém stavu
- Alzheimerova choroba: snížená konektivita[49]
- Mírné kognitivní poruchy: abnormální připojení[50]
- Autismus: změněno připojení[51][52]
- Deprese a účinky antidepresivum léčba: abnormální připojení[53][54][55][56]
- Bipolární porucha a účinky stabilizátory nálady: abnormální připojení a vlastnosti sítě[57][58][59][60]
- Schizofrenie: přerušené sítě[61]
- Porucha pozornosti s hyperaktivitou (ADHD): změněné „malé sítě“ a změny thalamu[62]
- Stárnoucí mozek: narušení mozkových systémů a motorické sítě[49]
- Epilepsie: narušení a snížení / zvýšení konektivity[63]
- Parkinsonova choroba: změněno připojení[64]
- Obsedantně kompulzivní porucha: zvýšení / snížení konektivity[65]
- Porucha bolesti: změněno připojení[66][67]
- Mentální anorexie: změny připojení v kortikolimbických obvodech a ostrovní kůra[68]
Mezi další typy současných a budoucích klinických aplikací fMRI v klidovém stavu patří identifikace skupinových rozdílů v mozkových onemocněních, získávání diagnostických a prognostických informací, longitudinální studie a účinky léčby, shlukování v heterogenních chorobných stavech a předoperační mapování a cílená intervence.[69] Jelikož měření v klidovém stavu nemají žádné kognitivní nároky (místo psychologických experimentů včetně úkolů), lze snadno měřit i kognitivně postižené osoby.
Viz také
Reference
- ^ Smith, Stephen M; Andersson, Jesper; Auerbach, Edward J .; Beckmann, Christian F; Bijsterbosch, Janine; Douaud, Gwenaëlle; Duff, Eugene; Feinberg, David A; Griffanti, Ludovica (15. 10. 2013). „FMRI v klidovém stavu v projektu Human Connectome“. NeuroImage. 80: 144–168. doi:10.1016 / j.neuroimage.2013.05.039. ISSN 1053-8119. PMC 3720828. PMID 23702415.
- ^ A b Bhushan, Chitresh; Chong, Minqi; Choi, Soyoung; Joshi, Anand A .; Haldar, Justin P .; Damasio, Hanna; Leahy, Richard M. (08.07.2016). „Temporal Non-Local Means Filtering Reveals Real-Time Celobrain Cortical Interactions in Resting fMRI“. PLOS ONE. 11 (7): e0158504. Bibcode:2016PLoSO..1158504B. doi:10.1371 / journal.pone.0158504. ISSN 1932-6203. PMC 4938391. PMID 27391481.
- ^ A b Biswal, B. B. (2012). "Klidový stav fMRI: Osobní historie. [Recenze]". NeuroImage. 62 (2): 938–944. doi:10.1016 / j.neuroimage.2012.01.090. PMID 22326802.
- ^ Buckner, RL; Krienen, FM; Yeo, BT (2013). "Příležitosti a omezení MRI vnitřní funkční konektivity". Přírodní neurovědy. 16 (7): 832–837. doi:10.1038 / č. 3423. PMID 23799476.
- ^ Sharaev, Maksim G .; Zavyalova, Viktoria V .; Ushakov, Vadim L .; Kartashov, Sergey I .; Velichkovsky, Boris M. (2016). „Efektivní připojení v síti výchozího režimu: dynamické kauzální modelování dat fMRI v klidovém stavu“. Frontiers in Human Neuroscience. 10: 14. doi:10.3389 / fnhum.2016.00014. PMC 4740785. PMID 26869900.
- ^ Biswal, B. B. (2011). "Funkční konektivita v klidovém stavu". Biologická psychiatrie. 69 (9): 200S. doi:10.1016 / j.biopsych.2011.03.032.
- ^ A b Rosazza, C .; Minati, L. (2011). „Sítě mozku v klidovém stavu: přehled literatury a klinické aplikace“. Neurol Sci. 32 (5): 773–785. doi:10.1007 / s10072-011-0636-r. PMID 21667095.
- ^ Cole, David M .; Smith, Stephen M .; Beckmann, Christian F. (2010). „Pokroky a úskalí v analýze a interpretaci údajů FMRI v klidovém stavu“. Frontiers in Systems Neuroscience. 4: 8. doi:10.3389 / fnsys.2010.00008. PMC 2854531. PMID 20407579.
- ^ DeYoe, E. A .; Bandettini, P .; Neitz, J .; Miller, D .; Winans, P. (1994). "Funkční magnetická rezonance (FMRI) lidského mozku". J Neurosciho metody. 54 (2): 171–187. doi:10.1016/0165-0270(94)90191-0. PMID 7869750.
- ^ Bandettini, P. A. (2009). „Sedm témat ve funkčním zobrazování magnetickou rezonancí“. J Integr Neurosci. 8 (3): 371–403. doi:10.1142 / s0219635209002186. PMC 3143579. PMID 19938211.
- ^ Bandettini, P (2007). "Funkční MRI dnes". Int J Psychofyziologie. 63 (2): 138–145. doi:10.1016 / j.ijpsycho.2006.03.016. PMID 16842871.
- ^ Korhonen, V; et al. (2014). „Synchronní multiscale neuroimagingové prostředí pro kriticky vzorkovanou fyziologickou analýzu mozkových funkcí: koncept hepta-skenování“. Brain Connect. 4 (9): 677–689. doi:10.1089 / brain.2014.0258. PMC 4238249. PMID 25131996.
- ^ Chuang, KH .; et al. (2008). „Mapování funkční konektivity v klidovém stavu pomocí perfúzní MRI“. NeuroImage. 40 (4): 1595–605. doi:10.1016 / j.neuroimage.2008.01.006. PMC 2435272. PMID 18314354.
- ^ Huettel, S. A .; Song, A. W .; McCarthy, G. (2009), Functional Magnetic Resonance Imaging (2. vyd.), Massachusetts: Sinauer, ISBN 978-0-87893-286-3
- ^ Damoiseaux, J. S .; Rombouts, S .; Barkhof, F .; Scheltens, P .; Stam, C. J .; Smith, S.M .; et al. (2006). „Konzistentní sítě v klidovém stavu napříč zdravými subjekty“. Sborník Národní akademie věd Spojených států amerických. 103 (37): 13848–13853. Bibcode:2006PNAS..10313848D. doi:10.1073 / pnas.0601417103. PMC 1564249. PMID 16945915.
- ^ Guerra-Carrillo, B .; Mackey, A. P .; Bunge, S.A. (21. února 2014). „Klidový stav fMRI: Okno do plasticity lidského mozku“. Neurovědec. 20 (5): 522–533. doi:10.1177/1073858414524442. PMID 24561514.
- ^ Fox, M. D .; Snyder, A. Z .; Vincent, J.L .; Corbetta, M .; Van Essen, D. C .; Raichle, M. E. (2005). „Lidský mozek je vnitřně organizován do dynamických antikorelujících funkčních sítí.“. Sborník Národní akademie věd Spojených států amerických. 102 (27): 9673–9678. Bibcode:2005PNAS..102,9673F. doi:10.1073 / pnas.0504136102. PMC 1157105. PMID 15976020.
- ^ Biswal, B. B .; VanKylen, J .; Hyde, J. S. (1997). „Simultánní vyhodnocení signálů toku a BOLD v mapách funkční konektivity v klidovém stavu“. NMR v biomedicíně. 10 (4–5): 165–170. doi:10.1002 / (sici) 1099-1492 (199706/08) 10: 4/5 <165 :: aid-nbm454> 3.0.co; 2-7.
- ^ Friston, K (2009). „Kauzální modelování a konektivita mozku při zobrazování funkční magnetickou rezonancí. [Redakční materiál]“. PLOS Biology. 7 (2): 220–225. doi:10.1371 / journal.pbio.1000033. PMC 2642881. PMID 19226186.
- ^ Fernandez-Seara, MA (2011). „Účinky na klidový průtok krve mozkem a funkční konektivitu vyvolanou metoklopramidem: perfúzní MRI studie u zdravých dobrovolníků“. Br J Pharmacol. 163 (8): 1639–52. doi:10.1111 / j.1476-5381.2010.01161.x. PMC 3166692. PMID 21175574.
- ^ Smith, S. M. (2012). "Budoucnost připojení FMRI". NeuroImage. 62 (2): 1257–1266. doi:10.1016 / j.neuroimage.2012.01.022. PMID 22248579.
- ^ Raichle, M. E. (2015). "Mozek je výchozí režim sítě". Roční přehled neurovědy. 38 (1): 433–447. doi:10.1146 / annurev-neuro-071013-014030. PMID 25938726.
- ^ Greicius, M. D .; Krasnow, B .; Reiss, A. L .; Menon, V. (2003). „Funkční konektivita v klidovém mozku: síťová analýza hypotézy výchozího režimu“. Sborník Národní akademie věd Spojených států amerických. 100 (1): 253–258. Bibcode:2003PNAS..100..253G. doi:10.1073 / pnas.0135058100. PMC 140943. PMID 12506194.
- ^ Buckner, R. L. (2012). "Náhodný objev výchozí sítě mozku". NeuroImage. 62 (2): 1137–1145. doi:10.1016 / j.neuroimage.2011.10.035. PMID 22037421.
- ^ A b Moussa, M. N .; Steen, M. R.; Laurienti, P. J .; Hayasaka, S. (2012). "Konzistence síťových modulů v konektomních datech FMRI v klidovém stavu". PLOS ONE. 7 (8): e44428. Bibcode:2012PLoSO ... 744428M. doi:10.1371 / journal.pone.0044428. PMC 3432126. PMID 22952978.
- ^ Lee, M. H .; Hacker, C. D .; Snyder, A. Z .; Corbetta, M .; Zhang, D. Y .; Leuthardt, E. C .; et al. (2012). „Shlukování sítí v klidovém stavu“. PLOS ONE. 7 (7): 7. Bibcode:2012PLoSO ... 740370L. doi:10.1371 / journal.pone.0040370. PMC 3392237. PMID 22792291.
- ^ Kiviniemi, Vesa J .; Kantola, Juha-Heikki; Jauhiainen, Jukka; Hyvärinen, Aapo; Tervonen, Osmo (2003). "Analýza nezávislých komponent nedeterministických zdrojů signálu fMRI". NeuroImage. 19 (2 Pt 1): 253–260. doi:10.1016 / S1053-8119 (03) 00097-1. PMID 12814576.
- ^ Beckmann, C. F .; DeLuca, M .; Devlin, J. T .; Smith, S. M. (2005). „Vyšetřování konektivity v klidovém stavu pomocí analýzy nezávislých komponent“. Filozofické transakce Královské společnosti B: Biologické vědy. 360 (1457): 1001–1013. doi:10.1098 / rstb.2005.1634. PMC 1854918. PMID 16087444.
- ^ Calhoun, VD; de Lacy, N (listopad 2017). „Deset klíčových pozorování při analýze funkčních zobrazovacích dat MR v klidovém stavu pomocí analýzy nezávislých komponent“. Neuroimagingové kliniky Severní Ameriky. 27 (4): 561–579. doi:10.1016 / j.nic.2017.06.012. PMC 5657522. PMID 28985929.
- ^ Margulies, D. S .; Kelly, A. M. C .; Uddin, L. Q .; Biswal, B. B .; Castellanos, F. X .; Milham, M. P. (2007). "Mapování funkční konektivity přední cingulární kůry". NeuroImage. 37 (2): 579–588. doi:10.1016 / j.neuroimage.2007.05.019. PMID 17604651.
- ^ Van Dijk, KRA; Hedden, T; Venkataraman, A; Evans, KC; Lazar, SW; Buckner, RL (2010). „Vnitřní funkční konektivita jako nástroj pro lidskou konektomiku: teorie, vlastnosti a optimalizace“. Journal of Neurophysiology. 103 (1): 297–321. doi:10.1152 / jn.00783.2009. PMC 2807224. PMID 19889849.
- ^ Cole, Michael W .; Yarkoni, Tal; Repovs, Grega; Anticevic, Alan; Braver, Todd S. (2012-06-27). „Globální konektivita prefrontální kůry předpovídá kognitivní kontrolu a inteligenci“. The Journal of Neuroscience. 32 (26): 8988–8999. doi:10.1523 / JNEUROSCI.0536-12.2012. ISSN 0270-6474. PMC 3392686. PMID 22745498.
- ^ Chang, C .; Glover, G. H. (2010). „Časově-frekvenční dynamika konektivity mozku v klidovém stavu měřená pomocí fMRI“. NeuroImage. 50 (1): 81–98. doi:10.1016 / j.neuroimage.2009.12.011. PMC 2827259. PMID 20006716.
- ^ Faria, A. V .; Joel, S.E .; Zhang, Y. J .; Oishi, K .; van Zjil, P. C. M .; Miller, M. I .; et al. (2012). „Atlasová analýza funkční konektivity v klidovém stavu: Hodnocení reprodukovatelnosti a multimodální korelační studie anatomie a funkce“. NeuroImage. 61 (3): 613–621. doi:10.1016 / j.neuroimage.2012.03.078. PMC 3358461. PMID 22498656.
- ^ Meszlényi, Regina J .; Hermann, Petra; Buza, Krisztian; Gál, Viktor; Vidnyánszky, Zoltán (01.01.2017). „Analýza funkčního připojení fMRI v klidovém stavu pomocí dynamického časového zkreslení“. Frontiers in Neuroscience. 11: 75. doi:10,3389 / fnins.2017.00075. PMC 5313507. PMID 28261052.
- ^ Zuo, XN; Xing, XX (2014). „Test-znovu otestujte spolehlivost měření FMRI v klidovém stavu ve funkční konektomice lidského mozku: perspektiva neurovědy systémů“. Neurovědy a biobehaviorální recenze. 45: 100–118. doi:10.1016 / j.neubiorev.2014.05.009. PMID 24875392.
- ^ Majeed, W .; Magnuson, M .; Keilholz, S. D. (2009). "Spatiotemporální dynamika nízkofrekvenčních fluktuací v BOLD fMRI krysy". Journal of Magnetic Resonance Imaging. 30 (2): 384–393. doi:10,1002 / jmri.21848. PMC 2758521. PMID 19629982.
- ^ Keilholz, S. D .; Magnuson, M .; Thompson, G. (2010). "Hodnocení přístupů k analýze dat na základě dat pro MRI funkční konektivity". Struktura a funkce mozku. 215 (2): 129–140. doi:10.1007 / s00429-010-0276-7. PMID 20853181.
- ^ Fox, M. D .; Halko, M. A .; Eldaief, M. C .; Pascual-Leone, A. (2012). „Měření a manipulace s mozkovou konektivitou pomocí funkční konektivity v klidovém stavu, zobrazování magnetickou rezonancí (fcMRI) a transkraniální magnetickou stimulací (TMS)“. NeuroImage. 62 (4): 2232–2243. doi:10.1016 / j.neuroimage.2012.03.035. PMC 3518426. PMID 22465297.
- ^ Birn, R.M .; Diamond, J. B.; Smith, M. A.; Bandettini, P.A. (2006). "Oddělení fluktuací souvisejících s respiračními variacemi od fluktuací fMRI souvisejících s neuronální aktivitou". NeuroImage. 31 (4): 1536–1548. doi:10.1016 / j.neuroimage.2006.02.048. PMID 16632379.
- ^ Chang, C., Glover, G.H., 2009. Vztah mezi dýcháním, CO (2) na konci přílivu a BOLD signály v fMRI v klidovém stavu. NeuroImage.
- ^ Ing, A; Schwarzbauer, C (2012). "Přístup dvojí ozvěny ke korekci pohybu pro studie funkční konektivity". NeuroImage. 63 (3): 1487–1497. doi:10.1016 / j.neuroimage.2012.07.042. PMID 22846657.
- ^ Van Dijk, K.R.A .; Sabuncu, M.R .; Buckner, R.L. (2012). „Vliv pohybu hlavy na vnitřní funkční konektivitu MRI“. NeuroImage. 59 (1): 431–438. doi:10.1016 / j.neuroimage.2011.07.044. PMC 3683830. PMID 21810475.
- ^ Power, J.D .; Barnes, K.A .; Snyder, A.Z .; Schlaggar, B.L .; Petersen, S.E. (2012). „Falešné, ale systematické korelace ve funkčních propojovacích MRI sítích vznikají z pohybu subjektu“. NeuroImage. 59 (3): 2142–2154. doi:10.1016 / j.neuroimage.2011.10.018. PMC 3254728. PMID 22019881.
- ^ Satterthwaite, T.D .; Wolf, D.H .; Loughead, J .; Ruparel, K .; Elliott, M. A.; Hakonarson, H .; Gur, R.C .; Gur, R.E. (2012). „Dopad pohybu hlavy ve skeneru na několik opatření funkční konektivity: význam pro studie neurového vývoje u mládeže“. NeuroImage. 60 (1): 623–632. doi:10.1016 / j.neuroimage.2011.12.063. PMC 3746318. PMID 22233733.
- ^ Saad, Z.S .; Gotts, S.J .; Murpy, K .; Chen, G .; Jo, H.J .; Martin, A .; Cox, R.W. (2012). „Problémy v klidu: Jak se po globální signální regresi zkreslí korelační vzorce a skupinové rozdíly. Připojení k mozku. 2 (1): 25–32. doi:10.1089 / brain.2012.0080. PMC 3484684. PMID 22432927.
- ^ Cordes, D .; Nandy, R.R. (2006). Msgstr "Odhad vnitřní dimenze dat fMRI". NeuroImage. 29 (1): 145–154. doi:10.1016 / j.neuroimage.2005.07.054. PMID 16202626.
- ^ Holtbernd, F .; Eidelberg, D. (2012). „Funkční mozkové sítě při poruchách pohybu: nedávný pokrok“. Aktuální názor v neurologii. 25 (4): 392–401. doi:10.1097 / wco.0b013e328355aa94. PMC 4554600. PMID 22710361.
- ^ A b Li, R., Wu, X., Chen, K., Fleisher, A. S., Reiman, E. M., & Yao, L. (2012). Změny směrové konektivity mezi sítěmi v klidovém stavu u Alzheimerovy choroby. AJNR Am J Neuroradiol.
- ^ Liang, P .; Wang, Z .; Yang, Y .; Li, K. (2012). „Tři subsystémy dolní mozkové kůry jsou při mírném kognitivním poškození ovlivněny odlišně“. Journal of Alzheimer's Disease. 30 (3): 475–487. doi:10.3233 / JAD-2012-111721. PMID 22451310.
- ^ Müller, R-A .; Shih, P .; Keehn, B .; Deyoe, J .; Leyden, K .; Shukla, D. (2011). „Nespojení, ale jak? Průzkum studií funkční konektivity MRI u poruch autistického spektra“. Mozková kůra. 21 (10): 2233–2243. doi:10.1093 / cercor / bhq296. PMC 3169656. PMID 21378114.
- ^ Vigneshwaran S, Mahanand B. S., Suresh S, Sundararajan N. Identifikace rozdílů v mozkových činnostech a přesná detekce poruchy autistického spektra pomocí zobrazování funkční magnetické rezonance v klidovém stavu: Přístup prostorové filtrace. Lékařská analýza obrazu. 2017;35:375–389. doi:10.1016 / j.media.2016.08.003.
- ^ Anand, A; Li, Y; Wang, Y; Wu, J; Gao, S; Kalnin, A; et al. (2005). „Aktivita a konektivita obvodu regulujícího náladu v depresi: studie funkční magnetické rezonance“. Biologická psychiatrie. 57 (10): 1079–88. doi:10.1016 / j.biopsych.2005.02.021. PMID 15866546.
- ^ Greicius, MD; Flores, BH; Menon, V; Glover, GH; Solvason, HB; Kenna, H; et al. (2007). „Funkční konektivita v klidovém stavu u velké deprese: Abnormálně zvýšené příspěvky z subgenuální cingulární kůry a thalamu“. Biologická psychiatrie. 62 (5): 429–37. doi:10.1016 / j.biopsych.2006.09.020. PMC 2001244. PMID 17210143.
- ^ Anand, Amit; Li, Yu; Wang, Yang; Wu, Jingwei; Gao, Sujuan; Bukhari, Lubna; Mathews, Vincent P; Kalnin, Andrew; Lowe, Mark J (červenec 2005). „Antidepresivní účinek na konektivitu obvodu regulujícího náladu: studie fMRI“. Neuropsychofarmakologie. 30 (7): 1334–1344. doi:10.1038 / sj.npp.1300725. ISSN 1740-634X. PMID 15856081.
- ^ Anand, Amit; Li, Yu; Wang, Yang; Gardner, Kathryn; Lowe, Mark J. (01.07.2007). „Reciproční účinky antidepresivní léčby na aktivitu a konektivitu obvodu regulujícího náladu: studie fMRI“. The Journal of Neuropsychiatry and Clinical Neurosciences. 19 (3): 274–282. doi:10.1176 / jnp.2007.19.3.274. ISSN 0895-0172. PMC 3465666. PMID 17827412.
- ^ Anand, A; Li, Y; Wang, Y; Lowe, MJ; Dzemidzic, M (2009). „Abnormality kortikolimbické konektivity v klidovém stavu u neléčených bipolárních poruch a unipolární deprese“. Psychiatrický výzkum: Neuroimaging. 171 (3): 189–98. doi:10.1016 / j.pscychresns.2008.03.012. PMC 3001251. PMID 19230623.
- ^ Spielberg, Jeffrey M; Beall, Erik B; Hulvershorn, Leslie A; Altinay, Murat; Karne, Harish; Anand, Amit (prosinec 2016). „Poruchy sítě v klidovém stavu související s hypománií a depresí u bipolární poruchy bez léků“. Neuropsychofarmakologie. 41 (13): 3016–3024. doi:10.1038 / npp.2016.112. ISSN 1740-634X. PMC 5101549. PMID 27356764.
- ^ Altinay, Murat I .; Hulvershorn, Leslie A .; Karne, Harish; Beall, Erik B .; Anand, Amit (2015-12-20). „Diferenciální funkční konektivita klidového stavu striatálních podoblastí v bipolární depresi a hypománii“. Připojení k mozku. 6 (3): 255–265. doi:10.1089 / brain.2015.0396. ISSN 2158-0014. PMC 4827275. PMID 26824737.
- ^ Altinay, Murat; Karne, Harish; Anand, Amit (2018). „Účinky klinického zlepšení spojené s monoterapií lithiem na spojení amygdala-ventromediální prefrontální kůry v klidovém stavu u bipolární poruchy“. Journal of afektivní poruchy. 225: 4–12. doi:10.1016 / j.jad.2017.06.047. PMC 5844774. PMID 28772145.
- ^ Venkataraman, A .; Whitford, T. J .; Westin, C. F .; Golland, P .; Kubicki, M. (2012). "Celý mozek v klidovém stavu, abnormality funkční konektivity u schizofrenie". Výzkum schizofrenie. 139 (1–3): 7–12. doi:10.1016 / j.schres.2012.04.021. hdl:1721.1/100215. PMC 3393792. PMID 22633528.
- ^ Uddin, L. Q .; Kelly, A. M. C .; Biswal, B. B .; Margulies, D. S .; Shehzad, Z .; Shaw, D .; et al. (2008). "Síťová homogenita odhaluje sníženou integritu sítě ve výchozím režimu v ADHD." Journal of Neuroscience Methods. 169 (1): 249–254. doi:10.1016 / j.jneumeth.2007.11.031. PMID 18190970.
- ^ Wurina, Zang; Zhao, S. G. (2012). „Studie fMRI v klidovém stavu u epilepsie“. Bulletin neurovědy. 28 (4): 449–455. doi:10.1007 / s12264-012-1255-1. PMC 5561896. PMID 22833042.
- ^ Tessitore, A .; Amboni, M .; Esposito, F .; Russo, A .; Picillo, M .; Marcuccio, L .; et al. (2012). „Připojení mozku v klidovém stavu u pacientů s Parkinsonovou chorobou a zmrazením chůze“. Parkinsonismus a související poruchy. 18 (6): 781–787. doi:10.1016 / j.parkreldis.2012.03.018. PMID 22510204.
- ^ Li, P .; Li, S.F .; Dong, Z. Y .; Luo, J .; Han, H. Y .; Xiong, H. F .; et al. (2012). „Změněné funkční funkční vzory klidového stavu přední prefrontální kůry u obsedantně-kompulzivní poruchy“. NeuroReport. 23 (11): 681–686. doi:10.1097 / wnr.0b013e328355a5fe. PMID 22692554.
- ^ Otti, A; Guendel, H; Wohlschlager, A; Zimmer, C; Noll-Hussong, M (2013). „Frekvenční posuny v síti předního výchozího režimu a výběžkové síti u chronické bolesti“. Psychiatrie BMC. 13: 84. doi:10.1186 / 1471-244x-13-84. PMC 3616999. PMID 23497482.
- ^ Otti, A; Guendel, H; Henningsen, P; Zimmer, C; Wohlschlaeger, AM; Noll-Hussong, M (leden 2013). „Funkční síťové propojení klidových stavových sítí souvisejících s bolestí u somatoformní poruchy bolesti: průzkumná studie fMRI“. J Psychiatrie Neurosci. 38 (1): 57–65. doi:10.1503 / jpn.110187. PMC 3529220. PMID 22894821.
- ^ Gaudio S, Wiemerslage L, Brooks SJ, Schiöth HB (2016). „Systematický přehled studií funkční-MRI v klidovém stavu u mentální anorexie: Důkazy o zhoršení funkční konektivity v kognitivní kontrole a integraci visuospatial a body-signal“. Neurosci Biobehav Rev. 71: 578–589. doi:10.1016 / j.neubiorev.2016.09.032. PMID 27725172.
- ^ Fox, M. D .; Greicius, M. (2010). „Klinické aplikace funkční konektivity v klidovém stavu“. Přední Syst Neurosci. 4: 19. doi:10.3389 / fnsys.2010.00019. PMC 2893721. PMID 20592951.