Molekulární pinzeta - Molecular tweezers
tento článek příliš spoléhá na Reference na primární zdroje. (Července 2018) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |

Molekulární pinzeta, a molekulární klipy, jsou hostiteli molekuly s otevřenými dutinami schopnými vázat molekuly hosta.[3] Otevřená dutina molekulární pinzety může hosty svázat pomocí nekovalentní vazba, která zahrnuje vodíkové vazby, kovová koordinace, hydrofobní síly, van der Waalsovy síly, Interakce π-π a / nebo elektrostatické účinky. Tyto komplexy jsou podmnožinou makrocyklický molekulární receptory a jejich struktura spočívá v tom, že dvě „ramena“, která mezi sebou váží molekulu hosta, jsou spojena pouze na jednom konci, což vede k určité flexibilitě těchto molekul receptoru (model indukovaného přizpůsobení).
Dějiny
Termín „molekulární pinzeta“ poprvé použil Whitlock.[4] Třídu hostitelů vyvinul a popularizoval Zimmerman od poloviny 80. do začátku 90. let[5][6][7] a později Klärner.[8]
Příklady
Některé molekulární pinzety se vážou aromatický Hosté.[1] Tyto molekulární pinzety se skládají z páru anthracen paže držené ve vzdálenosti, která umožňuje aromatickým hostům získat interakce π-π z obou (viz obrázek). Jiné molekulární pinzety mají uvázaný pár porfyriny.[9]
Ještě se váže jiný typ molekulární pinzety fullereny.[2] Takový "buckycatchers „, jsou složeny ze dvou korrannulen kleště, které doplňují povrch konvexní fulleren host (obrázek 2). An asociační konstanta (K.A) 8 600 M−1 byla vypočtena pomocí 1H NMR spektroskopie.
Stoermer a spolupracovníci popsali rozštěpy schopné zachytit molekuly cyklohexanu nebo chloroformu. Je zajímavé, že interakce pí hrály klíčové role při zachycování hostů i rychlosti tvorby rozštěpů.[10]
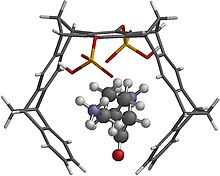
Ve vodě rozpustná fosfátem substituovaná molekulární pinzeta vyrobená ze střídání fenyl a norbornenyl substituenty se vážou na pozitivně nabité alifatické postranní řetězce bazických aminokyselin, jako je např lysin a arginin (Obrázek 3).[11][12] Podobné sloučeniny zvané „molekulární klipy“, jejichž boční stěny jsou spíše ploché než konvexní, raději uzavírají ploché pyridiniové kruhy (například nikotinamidový kruh NAD (P) +) mezi své ploché naftalenové boční stěny (obrázek 4).[13] Tyto vzájemně se vylučující vazebné režimy činí tyto sloučeniny cennými nástroji pro zkoumání kritických biologických interakcí základních aminokyselinových vedlejších řetězců v peptidech a proteinech i NAD (P)+ a podobné kofaktory. Například oba typy sloučenin inhibují oxidační reakce ethanolu pomocí alkohol dehydrogenáza nebo z glukóza-6-fosfátu glukóza-6-fosfátdehydrogenáza,[14] resp.

Molekulární pinzeta, ale ne svorky, účinně inhibuje tvorbu toxických oligomerů a agregátů amyloidogenními proteiny spojenými s různými chorobami. Příklady zahrnují proteiny zapojené do Alzheimerova choroba - amyloidní β-protein (Ap) a tau;[15][16][17] α-synuklein, o kterém se předpokládá, že je příčinou Parkinsonova choroba a další synucleinopathies[18][19][20][21] a je zapojen do poranění míchy;[22] mutantní huntingtin, který způsobuje Huntingtonovu chorobu;[23] ostrůvkový amyloidový polypeptid (amylin), který zabíjí β-buňky pankreatu cukrovka typu 2;[24] transthyretin (TTR), která způsobuje familiární amyloidovou polyneuropatii, familiární amyloidní kardiomyopatii a senilní systémovou amyloidózu;[25] agregace náchylných mutant nádorového supresorového proteinu p53;[26] a spermatické proteiny, jejichž agregace se zvyšuje HIV infekce.[27] Důležité je, že se ukázalo, že molekulární pinzeta je účinná a bezpečná nejen ve zkumavce, ale také na zvířecích modelech různých nemocí,[28][29] což naznačuje, že mohou být vyvinuty jako léky proti chorobám způsobeným abnormální agregací bílkovin, které v současné době nemají žádnou léčbu. Bylo také prokázáno, že ničí membrány obalených virů, jako je HIV, opar a hepatitida C,[27] což z nich dělá dobré kandidáty na vývoj mikrobicidů.
Výše uvedené příklady ukazují potenciální reaktivitu a specificitu těchto molekul. Vazební dutina mezi bočními rameny pinzety se může vyvinout tak, aby se vázala na vhodného hosta s vysokou specificitou, v závislosti na konfiguraci pinzety. Díky tomu je tato celková třída makromolekul skutečně syntetickými molekulárními receptory s důležitou aplikací v biologii a medicíně.[30][31][32]
Viz také
Reference
- ^ A b A. Petitjean; R. G. Khoury; N. Kyritsakas; J. M. Lehn (2004). "Dynamická zařízení. Přepínání tvarů a vázání substrátů v nanomechanických molekulárních pinzetách řízených ionty". J. Am. Chem. Soc. 126 (21): 6637–6647. doi:10.1021 / ja031915r. PMID 15161291.
- ^ A b A. Sygula; F. R. Fronczek; R. Sygula; P. W. Rabideau; M. M. Olmstead (2007). „Double Concave Hydrocarbon Buckycatcher“. J. Am. Chem. Soc. 129 (13): 3842–3843. doi:10.1021 / ja070616p. PMID 17348661.
- ^ Hardouin-Lerouge, M .; Hudhomme, P .; Salle, M. (2011). "Molekulární klipy a pinzety hostující neutrální hosty". Recenze chemické společnosti. 40 (1): 30–43. doi:10.1039 / B915145C. PMID 21038068.CS1 maint: používá parametr autoři (odkaz)
- ^ Chen C.-W .; Whitlock H. W. „Molekulární pinzeta - jednoduchý model bifunkční interkalace,“ J. Am. Chem. Soc. 1978, 100, 4921
- ^ Zimmerman, S. C .; VanZyl, C. M. "Tuhé molekulární pinzety: syntéza, charakterizace a komplexační chemie diacridinu," J. Am. Chem. Soc. 1987, 109, 7894.
- ^ Zimmerman, S. C .; Wu, W. „Tuhá molekulární pinzeta s karboxylovou kyselinou na aktivním místě: výjimečně účinný receptor pro adenin v organickém rozpouštědle,“ J. Am. Chem. Soc. 1989, 111, 8054.
- ^ Zimmerman, S. C. „Tuhá molekulární pinzeta jako hostitel pro komplexaci neutrálních hostů,“ Top. Curr. Chem. 1993, 165, 71.
- ^ F.-G. Klärner & B. Kahlert (2003). "Molekulární pinzeta a klipy jako syntetické receptory. Molekulární rozpoznávání a dynamika v komplexech receptor-substrát". Acc. Chem. Res. 36 (12): 919–932. doi:10.1021 / ar0200448. PMID 14674783.
- ^ X. Huang; N. Fujioka; G. Pescitelli; F. Koehn; R. T. Williamson; K. Nakanishi; N. Berova (2002). „Absolutní konfigurační přiřazení sekundárních aminů hostitelem dimerního zinku a porfyrinu citlivého na CD“. J. Am. Chem. Soc. 124 (17): 10320–10335. doi:10.1021 / ja020520p. PMID 12197735.
- ^ Stoermer, Martin J .; Wickramasinghe, Wasantha A .; Byriel, Karl A .; Hockless, David C. R .; Skelton, Brian W .; Sobolev, Alexandre N .; White, Allan H .; Mak, Jeffrey Y. W .; Fairlie, David P. (08.12.2017). „Stereoelektronické účinky na separaci dienofilů ovlivňují Diels-Alderovu syntézu molekulárních rázů“ (PDF). European Journal of Organic Chemistry. 2017 (45): 6793–6796. doi:10.1002 / ejoc.201701319. ISSN 1099-0690.
- ^ M Fokkens, T Schrader a F-Kl Klrner. Molekulární pinzeta pro lysin a arginin. J. Am. Chem. Soc. 2005; 127: 14415-14421.
- ^ P. Talbiersky; F. Bastkowski; F.-G. Klärner; T. Schrader (2008). „Molekulární svorka a pinzeta zavádějí nové mechanismy inhibice enzymů“. J. Am. Chem. Soc. 130 (30): 9824–9828. doi:10.1021 / ja801441j. PMID 18605724.
- ^ J. Polkowska; F. Bastkowski; T. Schrader; F.-G. Klärner; J. Zienau; F. Koziol; C. Ochsenfeld (2009). „Kombinovaná experimentální a teoretická studie vazebného režimu NAD + závislého na pH pomocí molekulárních klipů rozpustných ve vodě“. J. Phys. Org. Chem. 22 (30): 779–790. doi:10.1002 / poc. 1519.
- ^ M. Kirsch; P. Talbiersky; J. Polkowska; F. Bastkowski; T. Schaller; H. de Groot; F.-G. Klärner; T. Schrader (2009). "Mechanismus účinné inhibice G6PD molekulárním klipem". Angew. Chem. Int. Vyd. 48 (16): 2886–2890. doi:10.1002 / anie.200806175. PMID 19283805.
- ^ S Sinha, DHJ Lopes, Z Du, ES Pang, A Shanmugam, A Lomakin, P Talbiersky, A Tennstaedt, K McDaniel, R Bakshi, PY Kuo, M Ehrmann, GB Benedek, JA Loo, FG Klärner, T Schrader, C Wang a G Bitan. Lysinově specifické molekulární pinzety jsou širokospektrálním inhibitorem agregace a toxicity amyloidních proteinů. J. Am. Chem. Soc. 2011; 133 (42): 16958–16969.
- ^ S Sinha, Z Du, P Maiti, F-G Klärner, T Schrader, C Wang a G Bitan. Srovnání tří inhibitorů sestavení amyloidů: Cukr scyllo-inozitol, Polyfenol Epigallocatechin Gallate a Molekulární pinzeta CLR01. ACS Chem. Neurosci. 2012; 3 (6): 451-458.
- ^ X Zheng, D-Y Liu, F-G Klärner, T Schrader, G Bitan a MT Bowers. Sestavení amyloidového β-proteinu: Účinek molekulární pinzety CLR01 a CLR03. J. Phys. Chem. B, 2015; 119: 4831-4841.
- ^ S Prabhudesai *, S Sinha *, A Attar, A Kotagiri, AG Fitzmaurice, R Lakshmanan, MI Ivanova, JA Loo, F-G Klärner, T Schrader, M Stahl, G Bitan # a JM Bronstein #. Nový "Molekulární pinzeta" Inhibitor neurotoxicity α-synukleinu in vitro a in vivo. Neuroterapeutika. 2012; 9 (2): 464-476.
- ^ S Acharya, BM Safaie, P Wongkongkathep, MI Ivanova, A Attar, F-G Klärner, T Schrader, JA Loo, G Bitan a LJ Lapidus. Molekulární základ pro prevenci agregace α-synukleinu pomocí molekulární pinzety. J. Biol. Chem. 2014; 289 (15): 10727-10737.
- ^ A Lulla, L Barnhill, G Bitan, MI Ivanova, B Nguyen, K O'Donnell, MC Stahl, C Yamashiro, F-G Klärner, T Schrader, A Sagasti a JM Bronstein, Environ. Perspektiva zdraví. 2016; 124: 1766-1775. Archivováno 05.07.2017 na Wayback Machine
- ^ Richter, Franziska; Subramaniam, Sudhakar R .; Magen, Iddo; Lee, Patrick; Hayes, Jane; Attar, Aida; Zhu, Chunni; Franich, Nicholas R .; Bove, Nicholas (06.06.2017). „Molekulární pinzeta zmírňuje motorické deficity u myší s nadměrnou expresí α-synukleinu“. Neuroterapeutika. 14 (4): 1107–1119. doi:10.1007 / s13311-017-0544-9. ISSN 1933-7213. PMC 5722755. PMID 28585223.
- ^ SM Fogerson, AJ van Brummen, DJ Busch, SR Allen, R Roychaudhuri, S Banks, F-G Klärner, T Schrader, G Bitan a JR Morgan, Snížení akumulace synukleinu zlepšuje přežití neuronů po poranění míchy, Exp. Neurol. 2016; 278: 105-115.
- ^ Vöpel, Tobias; Bravo-Rodriguez, Kenny; Mittal, Sumit; Vachharajani, Shivang; Gnutt, David; Sharma, Abhishek; Steinhof, Anne; Fatoba, Oluwaseun; Ellrichmann, Gisa (26.04.2017). „Inhibice agregace Huntingtin Exon-1 molekulární pinzetou CLR01“. Journal of the American Chemical Society. 139 (16): 5640–5643. doi:10.1021 / jacs.6b11039. ISSN 0002-7863. PMC 5506490. PMID 28406616.
- ^ DHJ Lopes, A Attar, G Nair, EY Hayden, Z Du, K McDaniel, S Dutt, K Bravo-Rodriguez, S Mittal, FG Klärner, C Wang, E Sanchez-Garcia, T Schrader a G Bitan (2015) Molecular pinzeta novým mechanismem inhibuje sestavení a toxicitu ostrůvkových amyloidních polypeptidů, ACS Chem. Biol. 2015; 10: 1555-1569.
- ^ N Ferreira, A Pereira-Henriques, A Attar, F-G Klärner, T Schrader, G Bitan, L Gales, MJ Saraiva a MR Almeida. Molekulární pinzeta zaměřená na transthyretinovou amyloidózu. Neuroterapeutika. 2014; 11: 450-461.
- ^ G Herzog, MD Shmueli, L Levi, L Engel, E Gazit, F-G Klärner, T Schrader, G Bitan a D Segal. Lys-specifická molekulární pinzeta, CLR01, moduluje agregaci mutantní DNA vazebné domény p53 a inhibuje její toxicitu, Biochemistry, 2015; 54: 3729–3738.
- ^ A b E Lump, LM Castellano, C Meier, J Seeliger, N Erwin, B Sperlich, CM Stürzel, S Usmani, RM Hammond, J von Einem, G Gerold, F Kreppel, K Bravo-Rodriguez, T Pietschmann, VM Holmes, D Palesch , O Zirafi, D Weissman, A Sowislok, B Wettig, C Heid, F Kirchhoff, T Weil, FG Klärner, T Schrader, G Bitan, E Sanchez-Garcia, R Winter, J Shorter a Jan Münch, Molekulární pinzeta semenné amyloidy a infekce HIV, eLife, 2015; 4: e05397.
- ^ A Attar, C Ripoli, E Riccardi, P Maiti, DD Li Puma, T Liu, J Hayes, MR Jones, K Lichti-Kaiser, F Yang, GD Gale, Ch Tseng, M Tan, CW Xie, JL Straudinger, FG Klärner , T Schrader, SA Frautschy, C Grassi a G Bitan. Ochrana primárních neuronů a myšího mozku před Alzheimerovou patologií molekulární pinzetou. Mozek. 2012; 135 (Pt 12): 3735-3748.
- ^ Attar, W-TC Chan, F-G Klärner, T Schrader a G Bitan. Bezpečnost a farmakologická charakterizace molekulární pinzety CLR01 - širokospektrálního inhibitoru toxicity amyloidních proteinů. BMC Pharm. Tox. 2014; 15 (23): doi: 10.1186 / 2050-6511-15-23.
- ^ F-G Klärner a T Schrader. Aromatické interakce molekulárními pinzetami a sponami v chemických a biologických systémech. Acc. Chem. Res. 2013; 46: 967-978.
- ^ Attar a G Bitan. Narušení samo-montáže a toxicity amyloidogenních proteinových oligomerů pomocí „molekulární pinzety“ - od zkumavky po zvířecí modely, Curr. Pharm. Des. 2014; 20: 2469-2483.
- ^ T Schrader, G Bitan a F-G Klärner, molekulární pinzeta pro lysin a arginin - silné inhibitory patologické agregace proteinů, Chem. Commun. 2016: 52: 11318-11334.
externí odkazy
- Journal of Chemical Education Vybrané molekuly prosinec 2004: Nanoscale molekulární pinzeta a článek[trvalý mrtvý odkaz ]
- Molekulární pinzeta Crystalmaker

